Objetivo: atualização nos dispositivos de “Deep Brain Stimulation” aplicáveis ao parkinson. Abordamos critérios de elegibilidade (devo ou não devo fazer? qual a época adequada?) e inovações como DBS adaptativo (aDBS). Atenção: a partir de maio/20 fui impedido arbitrariamente de compartilhar postagens com o facebook. Com isto este presente blog substituirá o doencadeparkinson PONTO blogspot.com, abrangendo a doença de forma geral.
quinta-feira, 27 de fevereiro de 2025
sexta-feira, 21 de fevereiro de 2025
Pesquisadoras da UFRJ descobrem possível novo tratamento para doença de Parkinson
20 de fevereiro, 2025 - Pesquisadoras da Universidade Federal do Rio de Janeiro (UFRJ) descobriram um potencial novo tratamento da doença de Parkinson. O estudo, publicado na revista científica Molecular Psychiatry e apoiado pela Fundação de Amparo à Pesquisa do Estado do Rio de Janeiro (Faperj), revelou que o medicamento abatacept, já utilizado no tratamento da artrite reumatoide, pode desempenhar um papel crucial contra a doença de Parkinson, enfermidade neurológica degenerativa que afeta principalmente os movimentos.
O trabalho foi conduzido pelas cientistas Claudia Figueiredo, da Faculdade de Farmácia da UFRJ, e Júlia Clarke, do Instituto de Ciências Biomédicas da UFRJ, com colaboração de Yraima Cordeiro e Giselle Passos. O estudo demonstra que o abatacept atua seletivamente no sistema imunológico do cérebro, freando o avanço da doença e até restaurando funções motoras em estudos com animais.
As cientistas identificaram que as células T auxiliares desempenham um papel central no processo inflamatório da doença de Parkinson. Essas células, ao invés de atacarem diretamente os aglomerados da proteína α-sinucleína, liberam sinais químicos que ativam outras células imunológicas, intensificando a inflamação e os danos aos neurônios. A partir dessa descoberta, surgiu a hipótese de que o abatacept poderia ser um tratamento eficaz, já que sua ação reduz seletivamente essas células inflamatórias.
Os resultados da pesquisa confirmaram essa possibilidade. O tratamento reduziu significativamente a presença das células T auxiliares no cérebro, especialmente os subtipos mais inflamatórios, o que resultou na proteção dos neurônios e na melhora da função motora dos animais estudados.
A pesquisa contou com o apoio do Instituto Nacional de Ciência e Tecnologia de Inovação em Medicamentos e Identificação de Novos Alvos Terapêuticos (INCT-Inovamed) e do Centro Nacional de Biologia Estrutural e Bioimagem (Cenabio/UFRJ). Fonte: cremerj.
quarta-feira, 19 de fevereiro de 2025
AskBio faz progresso na avaliação clínica da terapia genética da doença de Parkinson AB-1005
27 de janeiro de 2025 - A empresa iniciou o processo de designação aleatória de participantes inscritos no ensaio clínico de fase 2 controlado por placebo REGENERATE-PD.
A Asklepios BioPharmaceutical (AskBio) iniciou o processo de designação aleatória de participantes inscritos no ensaio clínico de fase 2 controlado por placebo REGENERATE-PD (NCT06285643) avaliando AB-1005 (AAV2-GDNF), uma terapia genética de vetor de vírus adenoassociado experimental sorotipo 2 (AAV2), para o tratamento da doença de Parkinson (DP).1
O estudo randomizado e duplo-cego iniciou as atividades de recrutamento nos Estados Unidos em 2024. Ele está aberto a pacientes com DP em estágio moderado com idade entre 45 e 75 anos. O teste, que será realizado na Alemanha, Polônia e Reino Unido, além dos EUA, deve inscrever cerca de 87 pacientes no total.
“A randomização dos primeiros participantes do REGENERATE-PD é uma notícia positiva para as pessoas que vivem com DP e os médicos que as tratam”, disse o pesquisador principal Rajesh Pahwa, MD, diretor do Parkinson’s Disease and Movement Disorder Center do University of Kansas Medical Center, em uma declaração.1 “Há uma necessidade significativa de terapias neurorestaurativas na DP e ver o avanço de uma importante terapia genética investigacional em um teste clínico de fase 2 dá esperança aos pacientes e à comunidade médica.”
O AB-1005 tem como objetivo administrar um transgene do fator neurotrófico (GDNF) derivado da linhagem de células gliais humanas, com a expectativa de que ele promova a sobrevivência e a diferenciação morfológica de neurônios dopaminérgicos, cuja degeneração está associada à DP.2,3 Ele é administrado por meio de uma injeção neurocirúrgica direta com administração aprimorada por convecção monitorada por ressonância magnética e também deve aumentar a captação de dopamina de alta afinidade dos neurônios em questão.
Os pacientes no braço experimental do REGENERATE-PD receberão uma infusão bilateral guiada por imagem no putâmen de uma dose única de AB-1005, enquanto os pacientes no braço comparador simulado passarão por um procedimento cirúrgico de controle que consiste em furos de rebarba/torção parciais bilaterais sem penetração dural. O CGTLive® cobriu anteriormente o design do ensaio clínico em profundidade, pouco antes de seu início em 11 de junho de 2024.
O AB-1005 foi avaliado anteriormente em um ensaio clínico de fase 1b (NCT04167540) para pacientes com DP. O ensaio de fase 1b atingiu sua data de conclusão primária em 17 de outubro de 2023 e não está mais recrutando novos participantes, mas o acompanhamento de longo prazo está em andamento. Os dados do ensaio de fase 1b foram apresentados mais recentemente no Congresso Internacional de Doença de Parkinson e Distúrbios do Movimento, realizado na Filadélfia, PA, de 27 de setembro a 1º de outubro de 2024.1 A AskBio destacou que, 36 meses após o tratamento, os dados mostraram tendências de melhora em pacientes na coorte de DP moderada na Escala de Classificação da Doença de Parkinson Unificada da Movement Disorder Society (MDS-UPDRS) e diários motores. No mesmo ponto de tempo, os pacientes nesta coorte também demonstraram tendências para reduções nos medicamentos de Parkinson (dose diária equivalente a levodopa [LEDD]). Além disso, a empresa declarou que a maioria dos pacientes nesta coorte tinha um "estado clínico geral estável" — não foi observada muita mudança no MDS-UPDRS, diário motor de DP autorrelatado ou LEDD para esses pacientes. Com relação à segurança, a AskBio relatou que a terapia genética foi bem tolerada e que nenhum evento adverso sério foi considerado relacionado ao AB-1005 em si.
“A AskBio continua a marcar marcos significativos no desenvolvimento clínico da terapia genética investigacional AB-1005 enquanto nos esforçamos para trazer uma terapia genética segura e eficaz para pacientes com DP em estágio moderado”, Canwen Jiang, MD, PhD, diretor de desenvolvimento e diretor médico da AskBio, acrescentou à declaração.1 “Com os participantes do REGENERATE-PD agora sendo randomizados, estamos animados com nosso progresso com o AB-1005 e ansiosos para compartilhar mais atualizações em um fórum científico apropriado conforme o programa avança no próximo ano e além.”
O site irmão do CGTLive, NeurologyLive®, falou anteriormente com Russell Lonser, MD, diretor do Gene Therapy Institute e presidente do departamento de cirurgia neurológica da The Ohio State University, sobre o AB-1005 em maio de 2024.4 Lonser falou sobre os dados mais recentes disponíveis na época e as potenciais implicações dos avanços da terapia genética para o futuro cenário de tratamento de distúrbios neurológicos em geral.
"Acredito que o que a terapia genética nos oferece é uma nova oportunidade de realmente atingir o problema específico da doença em sua essência", disse Lonser ao NeurologyLive. Fonte: cgtlive.
DBS adaptativo pode passar para ensaio clínico fundamental após US$ 14 milhões arrecadados
Com rodada de financiamento, Newronika busca 'validação clínica' do AlphaDBS
18 de fevereiro de 2025 - A Newronika planeja usar os 13,6 milhões de euros (cerca de US$ 14,3 milhões) arrecadados em uma rodada de financiamento para apoiar o que poderia ser um ensaio clínico fundamental de seu sistema adaptativo de estimulação cerebral profunda (DBS), projetado para ajustar o tratamento em tempo real para controlar melhor os sintomas da doença de Parkinson e minimizar os efeitos colaterais.
O anúncio do fechamento da rodada de financiamento da série B seguiu os passos de uma decisão da Food and Drug Administration dos EUA de emitir uma isenção de dispositivo experimental para a Newronika cobrindo seu sistema DBS adaptativo, informou a empresa no início deste mês. Essa isenção permite que um dispositivo experimental seja enviado para uso em um estudo clínico de segurança e eficácia nos EUA.
"Estamos entusiasmados com o forte apoio de investidores novos e existentes", disse Lorenzo Rossi, PhD, cofundador e CEO da Newronika, no comunicado de imprensa mais recente da empresa. "Esta rodada da Série B valida nosso compromisso de transformar a forma como [DBS] é entregue."
Esse "influxo significativo de capital capacitará a Newronika a expandir a validação clínica e a comercialização de seu sistema DBS adaptativo proprietário", afirmou o comunicado.
Ensaio em andamento sobre AlphaDBS administrado como tratamento adaptativo e convencional
Um pequeno estudo clínico (NCT04681534), inaugurado em 2021, está comparando a segurança e a tolerabilidade do sistema AlphaDBS da empresa, como é chamado, administrado como DBS adaptativo e DBS convencional em cerca de 15 pacientes com Parkinson idiopático (causa desconhecida) em locais na Itália, Holanda e Polônia. Os objetivos secundários, também avaliados após um mês de tratamento, dizem respeito à potencial eficácia do dispositivo e incluem alterações desde o início do estudo nos sintomas motores de Parkinson e na discinesia, ou movimentos descontrolados e involuntários. O julgamento deve terminar até o final do ano.
O AlphaDBS recebeu a marca CE na União Europeia, o que significa que atendeu aos requisitos de segurança e saúde estabelecidos.
A rodada de financiamento da série B foi liderada por um novo investidor, a italiana Fondazione ENEA Tech e Biomedical, com contribuições adicionais de investidores existentes: Indaco Venture Partners, Innogest, Wille Finance, TNBT Capital e F3F.
Os sintomas motores do Parkinson resultam da perda de neurônios dopaminérgicos, as células nervosas no cérebro que liberam dopamina, um mensageiro químico envolvido no controle motor. Essa perda pode levar a uma atividade cerebral anormal. O DBS envolve a implantação cirúrgica de fios finos, conhecidos como eletrodos, em áreas específicas do cérebro. Esses eletrodos são conectados a um pequeno dispositivo neuroestimulador normalmente colocado no peito. O dispositivo fornece impulsos elétricos controlados ao cérebro, ajudando a normalizar sua atividade e aliviar os sintomas motores. O DBS adaptativo aumenta a possibilidade de ajustes automáticos de estimulação Ao contrário dos dispositivos convencionais, que fornecem estimulação a uma taxa constante, o sistema AlphaDBS adaptativo da Newronika é um neuroestimulador inteligente projetado para ajustar os sinais elétricos enviados ao cérebro em tempo real. Ele lê os sinais cerebrais em áreas que estão sendo estimuladas e se adapta automaticamente para fornecer a quantidade de corrente necessária para um paciente em determinados momentos. O objetivo é proporcionar um melhor controle dos sintomas motores, minimizando os efeitos colaterais. Como tal, o AlphaDBS pode permitir uma terapia personalizada. “Nosso objetivo é integrar perfeitamente dados neurais em tempo real e aprendizado de máquina em nossos sistemas DBS para criar terapias verdadeiramente personalizadas que superem as capacidades dos dispositivos existentes no mercado”, disse Rossi.
"Com a Newronika e sua plataforma DBS adaptativa, vemos um potencial extraordinário para revolucionar o tratamento de distúrbios do movimento em escala global", disse Maria Cristina Porta, gerente geral da Fondazione ENEA Tech e Biomedical, uma fundação italiana que investe em biotecnologia e dispositivos médicos.
Essa "abordagem inovadora, capaz de neuromodulação personalizada em tempo real, se alinha perfeitamente com nossa visão de apoiar tecnologias médicas disruptivas", acrescentou Porta.
Além de apoiar o que pode ser um ensaio clínico fundamental de segurança e eficácia do AlphaDBS, os fundos arrecadados serão usados para ajudar a desenvolver novos produtos no pipeline da empresa, recrutar especialistas e construir parcerias, relatou Newronika. Fonte: Parkinsonsnewstoday.
A instalação de Kenai impulsionará a pesquisa de substituição de neurônios de Parkinson
A mudança para o Lilly Gateway Labs oferecerá acesso a laboratórios, recursos e experiência
18 de fevereiro de 2025 - A Kenai Therapeutics está montando instalações de pesquisa e laboratório no Lilly Gateway Labs em San Diego, para ajudar no avanço do RNDP-001, sua terapia experimental de reposição de neurônios dopaminérgicos para a doença de Parkinson.
Ao ingressar na Gateway Labs, a Kenai, anteriormente Ryne Biotechnologies, terá acesso a instalações de última geração, juntamente com recursos e experiência da Lilly.
"Somos gratos pela chance de trabalhar ao lado e colaborar com algumas das mentes mais inovadoras do setor enquanto nos preparamos para entrar na clínica com nosso principal candidato, RNDP-001, para o tratamento potencial da doença de Parkinson", disse Nicholas Manusos, CEO da Kenai, em um comunicado à imprensa.
Uma característica fundamental do Parkinson é a perda gradual de neurônios dopaminérgicos, as células nervosas responsáveis pela produção de dopamina, um mensageiro químico envolvido no controle motor. Como resultado, um foco significativo de muitos tratamentos de Parkinson é aumentar a dopamina no cérebro, aliviando assim os sintomas motores associados à doença.
O que é RNDP-001?
RNDP-001 é uma terapia celular experimental projetada para substituir os neurônios produtores de dopamina perdidos no Parkinson. Ele usa células progenitoras de neurônios dopaminérgicos, que são geradas a partir de células-tronco pluripotentes induzidas (iPSCs) que são criadas retirando células maduras da pele ou do sangue de um paciente e reprogramando-as em um estado semelhante a células-tronco. Isso permite que eles se desenvolvam em vários tipos de células, incluindo neurônios produtores de dopamina.
As células são produzidas com antecedência e armazenadas em baixas temperaturas, para estarem disponíveis quando necessário.
As células progenitoras são entregues cirurgicamente diretamente no cérebro do paciente, onde devem se diferenciar em neurônios dopaminérgicos, aumentar a sinalização da dopamina e potencialmente interromper a progressão da doença. O tratamento está sendo desenvolvido tanto para Parkinson hereditário quanto para Parkinson idiopático, ou de causa desconhecida, de formas moderadas a graves.
Estudos pré-clínicos mostram que as células progenitoras sobrevivem e estabelecem conexões em várias regiões do cérebro, inclusive no corpo estriado, que está envolvido no controle motor, onde a sinalização da dopamina é normalmente perdida no Parkinson.
Em um modelo de rato de Parkinson, o transplante de uma grande quantidade de células progenitoras de neurônios dopaminérgicos levou ao aumento da inervação ou ao crescimento de novos nervos, resultando em melhor função motora e maiores taxas de sobrevivência.
O RNDP-001 está sendo desenvolvido em colaboração com o Instituto de Medicina Regenerativa da Califórnia, que concedeu US$ 4 milhões para avançar em seu desenvolvimento. Também é apoiado por financiamento da Fundação Michael J. Fox para Pesquisa de Parkinson.
A Gateway Labs fornece suporte a empresas emergentes de biotecnologia, oferecendo espaço de laboratório, escritórios e salas de conferência, além de ajudar no desenvolvimento científico e acesso a financiamento de capital. Fonte:parkinsonsnewstoday.
Nova parceria para avançar na terapia de reposição celular para Parkinson
Smartcella e Karolinska Institute se unem para desenvolver novos tratamentos
19 de fevereiro de 2025 - A Smartcella, com sede na Suécia, firmou um acordo com uma equipe de pesquisa do Instituto Karolinska para obter os direitos exclusivos de avançar uma terapia de substituição celular para a doença de Parkinson em desenvolvimento clínico e comercialização.
A equipe do Instituto Karolinska, na Suécia, liderada por Johan Ericson, PhD, professor de biologia do desenvolvimento, desenvolveu um novo protocolo que usa células-tronco pluripotentes para produzir células progenitoras de neurônios. Esses progenitores de células nervosas amadurecem em neurônios produtores de dopamina - células nervosas que são gradualmente perdidas no Parkinson.
Em estudos pré-clínicos, onde as células foram implantadas no cérebro de um modelo de rato com Parkinson, as células progenitoras foram capazes de gerar neurônios dopaminérgicos e aliviar os sintomas motores associados à doença.
"A pesquisa de Johan em torno dos neurônios produtores de dopamina mostra uma clara melhoria em comparação com os métodos existentes", disse Niklas Prager, CEO da Smartcella, em um comunicado à imprensa da empresa. "Ao combinar o protocolo de Johan, que tem melhores resultados e eficácia, com nossas [boas práticas de fabricação] ... e recursos de desenvolvimento de processos, teremos uma vantagem em preencher a lacuna entre laboratórios e clínicas."
Ericson, que disse que "os resultados pré-clínicos que temos até agora são realmente encorajadores", observou que a equipe está ansiosa para avançar na terapia.
"Estamos confiantes de que nossa abordagem translacional é uma grande promessa para o estabelecimento de um produto celular competitivo e terapeuticamente [altamente] eficaz para tratar a doença de Parkinson no futuro", disse Ericson, que também observou que a equipe de pesquisa "adaptou o processo de fabricação de células em um formato escalável" que ajudará em seu desenvolvimento.
"Com o desenvolvimento do processo, os recursos de expansão e o conhecimento do Smartcella, seremos capazes de acelerar o caminho [para] estudos clínicos em humanos", disse Ericson.
A doença de Parkinson é causada pela disfunção progressiva e morte de neurônios dopaminérgicos, as células nervosas que produzem dopamina, em uma região do mesencéfalo chamada substância negra. A dopamina é um neurotransmissor, ou molécula de sinalização, envolvida no controle motor.
À medida que a doença de Parkinson progride, os pacientes experimentam uma deterioração gradual de suas funções motoras. Com o tempo, a eficácia dos tratamentos disponíveis, que visam principalmente aliviar esses sintomas, tende a diminuir.
As terapias baseadas em células surgiram como uma opção potencial de tratamento para o Parkinson, com o objetivo de substituir os neurônios dopaminérgicos perdidos. Essas terapias usam células-tronco pluripotentes, que possuem a capacidade única de se diferenciar em vários tipos de células, incluindo neurônios dopaminérgicos.
Estamos confiantes de que nossa abordagem translacional é uma grande promessa para o estabelecimento de um produto celular competitivo e terapeuticamente [altamente] eficaz para tratar a doença de Parkinson no futuro. … Com o desenvolvimento do processo, os recursos de expansão e o conhecimento do Smartcella, seremos capazes de acelerar o caminho para estudos clínicos em humanos.
A equipe de Ericson desenvolveu uma tecnologia baseada em células-tronco pluripotentes que difere de outros protocolos usados para obter neurônios dopaminérgicos de células-tronco. Sua abordagem usa ácido retinóico, uma molécula envolvida no desenvolvimento neural.
De acordo com os pesquisadores, seu protocolo aumenta o rendimento de neurônios dopaminérgicos após o transplante, resultando em transplantes menores com características marcantes dos neurônios dopaminérgicos existentes no cérebro.
Prager chamou o novo acordo com a equipe de pesquisa de "uma adição importante ao nosso pipeline de projetos".
"A perspectiva de fornecer terapias alogênicas [derivadas de doadores] inovadoras e seguras para pacientes com doença de Parkinson, com potencial para transformar suas vidas, é inovadora e cada vez mais ao alcance", disse Prager. Fonte: parkinsonsnewstoday.
Como as gerações futuras verão o DBS para a doença de Parkinson?
O conhecimento e os tratamentos médicos tendem a mudar drasticamente ao longo do tempo
19 de fevereiro de 2025 - Às vezes penso nas estranhas práticas médicas que foram usadas há centenas de anos para tratar doenças e como essas estratégias se comparam às práticas de hoje.
No século 19, as transfusões de leite eram consideradas um substituto adequado para as transfusões de sangue. (Embora alguns pacientes tenham sobrevivido ao procedimento, a maioria morreu.) O clorofórmio, agora conhecido por causar depressão respiratória, foi usado para tratar a asma. Então, não muito tempo atrás, as condições de saúde mental eram tratadas com procedimentos como lobotomias. E a lista continua.
É fácil olhar para esses métodos com olhos arregalados e de boca aberta, mas os cientistas da época não tinham motivos para duvidar da validade de seus experimentos. Por que o leite no sangue não melhoraria a saúde de alguém? Afinal, era exatamente o que ajudava os bebês a se transformarem em adultos.
Enquanto minha mente gira com percalços históricos, me pergunto quais práticas contemporâneas obterão respostas semelhantes das gerações futuras. A estimulação cerebral profunda (DBS) será percebida como uma falha estranha e infeliz do passado? Hoje, muitas pessoas com doença de Parkinson veem o procedimento como um milagre.
Meu pai até passou por uma cirurgia DBS em 2019, e pequenos eletrodos foram colocados em sua cabeça para interromper sua discinesia. E funcionou! De fato, de acordo com a fabricante de dispositivos médicos Medtronic, 85% a 89% das pessoas com Parkinson experimentam com melhora clinicamente significativa com seu dispositivo DBS.
Uma rápida pesquisa em fóruns públicos sobre a doença de Parkinson traz todos os tipos de resultados diferentes, desde hardware misterioso que promete revolucionar o tratamento de doenças até ervas e especiarias que prometem controlar tremores. Talvez alguns desses tópicos de discussão se tornem os horrores de ontem. Talvez não.
A boa notícia é que é relativamente fácil me tirar dessas espirais de pensamento sobre o passado. Claro, contemporaneamente, os profissionais médicos provavelmente estão cometendo alguns erros. Mas a realidade é que os cientistas fizeram grandes avanços no tratamento de condições como o Parkinson no século passado. E embora a maioria dos relatos sugira que estamos fazendo a transição da "Era da Informação" para a "Era da Inteligência", tenho esperança de que continuaremos a progredir na medicina.
Eu realmente preferiria uma cura para meu pai em vez de um tratamento, mas às vezes tenho que me lembrar de que não faz nem 70 anos que a levodopa começou a melhorar a vida dos pacientes em primeiro lugar. Talvez eu devesse apenas ser grato que os profissionais médicos não estejam mais usando cocaína para tratar a febre do feno. Porque, nossa — isso é simplesmente bobo. Fonte: Parkinsons News Today.
AskBio recebe designação de terapia avançada de medicina regenerativa da FDA para terapia genética experimental da doença de Parkinson
19 de fev de 2025 - A designação de Terapia Avançada de Medicina Regenerativa (RMAT) segue os dados de 36 meses da Fase Ib
O estudo demonstrou perfil de segurança favorável e tendências positivas contínuas nas medidas de resultados clínicos avaliados da terapia gênica experimental AB-1005 (anteriormente conhecida como AAV2-GDNF) sem eventos adversos graves relacionados ao produto.
Inscrição em andamento para o ensaio clínico de Fase II REGENERATE-PD do AB-1005, uma terapia genética experimental do fator neurotrófico derivado da linha de células gliais (GDNF) para o tratamento da doença de Parkinson em estágio moderado.
A AskBio Inc. (AskBio), uma empresa de terapia genética de propriedade integral e operada de forma independente como subsidiária da Bayer AG, anunciou hoje que a terapia genética experimental AB-1005 para o tratamento da doença de Parkinson (DP) recebeu a designação de Terapia Avançada de Medicina Regenerativa (RMAT) da Food and Drug Administration (FDA) dos Estados Unidos.
"A decisão da FDA de conceder a designação RMAT ao AB-1005 é uma notícia empolgante para as pessoas que vivem com a doença de Parkinson e seus entes queridos", disse Gustavo Pesquin, CEO da AskBio. "Este marco pode potencialmente acelerar o desenvolvimento de nosso importante programa de terapia genética investigativa e destaca nossos dados promissores e o potencial do AB-1005 para pacientes e a comunidade médica. Estamos ansiosos para trabalhar em estreita colaboração com o FDA para acelerar nosso programa."
A FDA determinou que o AB-1005, uma terapia genética experimental destinada a retardar a progressão da doença e melhorar os resultados motores em pacientes com DP, atendeu aos critérios para designação de RMAT. Esta decisão segue uma revisão das informações e dados fornecidos pela AskBio, incluindo evidências clínicas do estudo aberto e não controlado de Fase Ib do AB-1005.
Os dados da Fase Ib de 36 meses da AskBio mostraram que a administração de AB-1005 foi bem tolerada, sem eventos adversos graves relacionados ao produto. 1 Além disso, a coorte de DP moderada mostrou tendências de melhora ou estabilidade em várias escalas clínicas relevantes para a DP em 36 meses em comparação com a linha de base, incluindo a Escala Unificada de Avaliação da Doença de Parkinson da Sociedade de Distúrbios do Movimento (MDS-UPDRS) e diários motores de DP auto-relatados, juntamente com tendências nas reduções nos medicamentos para Parkinson (dose diária equivalente a levodopa [LEDD]). 1 A maioria dos participantes da coorte de DP leve mostrou um estado clínico geral estável com pouca alteração no MDS-UPDRS, o diário motor de DP auto-relatado, ou LEDD. 1
RMAT é uma designação concedida pelo FDA para terapias regenerativas, incluindo terapias genéticas, sendo desenvolvidas para tratar, modificar, reverter ou curar doenças ou condições graves ou com risco de vida. 2 Os produtos experimentais que recebem esta designação devem ter produzido evidências clínicas preliminares indicando que podem ter o potencial de atender às necessidades médicas não atendidas de tais doenças ou condições. 2 O RMAT fornece aos destinatários acesso aprimorado ao FDA, que pode incluir orientação intensiva sobre o desenvolvimento eficiente de medicamentos, revisão contínua do Pedido de Licença Biológica (BLA) e outras ações para agilizar a revisão. algarismo
"A designação RMAT para AB-1005 ressalta a alta necessidade médica não atendida e o potencial dessa terapia genética experimental para fazer a diferença para pacientes com doença de Parkinson", disse Christian Rommel, vice-presidente executivo, chefe global de pesquisa e desenvolvimento e membro da equipe de liderança farmacêutica da Bayer. "Este é o exemplo mais recente do que pode ser alcançado por meio do compromisso conjunto da AskBio e da Bayer de oferecer inovação revolucionária para os pacientes."
Os primeiros participantes do ensaio clínico AB-1005 Fase II REGENERATE-PD foram randomizados nos Estados Unidos, e o estudo está atualmente recrutando. 3 Espera-se que locais de estudo adicionais nos Estados Unidos, Alemanha, Polônia e Reino Unido sejam abertos para inscrições no primeiro semestre de 2025. 3
O AB-1005 não foi aprovado por nenhuma autoridade reguladora e sua eficácia e segurança não foram totalmente estabelecidas ou avaliadas. (...)
About the AB-1005 Phase Ib trial
Neste estudo de Fase Ib, multicêntrico, multicêntrico, aberto e não controlado, 11 pacientes receberam AB-1005 ao putâmen por meio de uma entrega bilateral única com convecção aprimorada. Os pacientes foram inscritos em duas coortes, leve (6 pacientes) e moderada (5 pacientes), com base na duração e estágio de sua DP. O objetivo desta investigação foi avaliar a segurança e o potencial efeito clínico do AB-1005 entregue ao putâmen em pacientes com DP precoce/leve ou moderada. Os desfechos avaliados em 36 meses foram a incidência de Eventos Adversos Emergentes do Tratamento (TEAEs) relatados pelos pacientes ou avaliados clinicamente por exames físicos e neurológicos, sintomas motores relatados pela Escala Unificada de Avaliação da Doença de Parkinson da Movement Disorder Society (MDS-UPDRS) e autoavaliações do Diário Motor da DP, sintomas não motores da DP e integridade da rede dopaminérgica cerebral medida pelo DaTSCAN.1 Essas avaliações continuarão por até cinco anos. Para obter mais informações, visite clinicaltrials.gov (NCT#04167540 ou askbio.com). Fonte: morningstar.
Estimulação cerebral profunda sem fio reverte a doença de Parkinson em camundongos
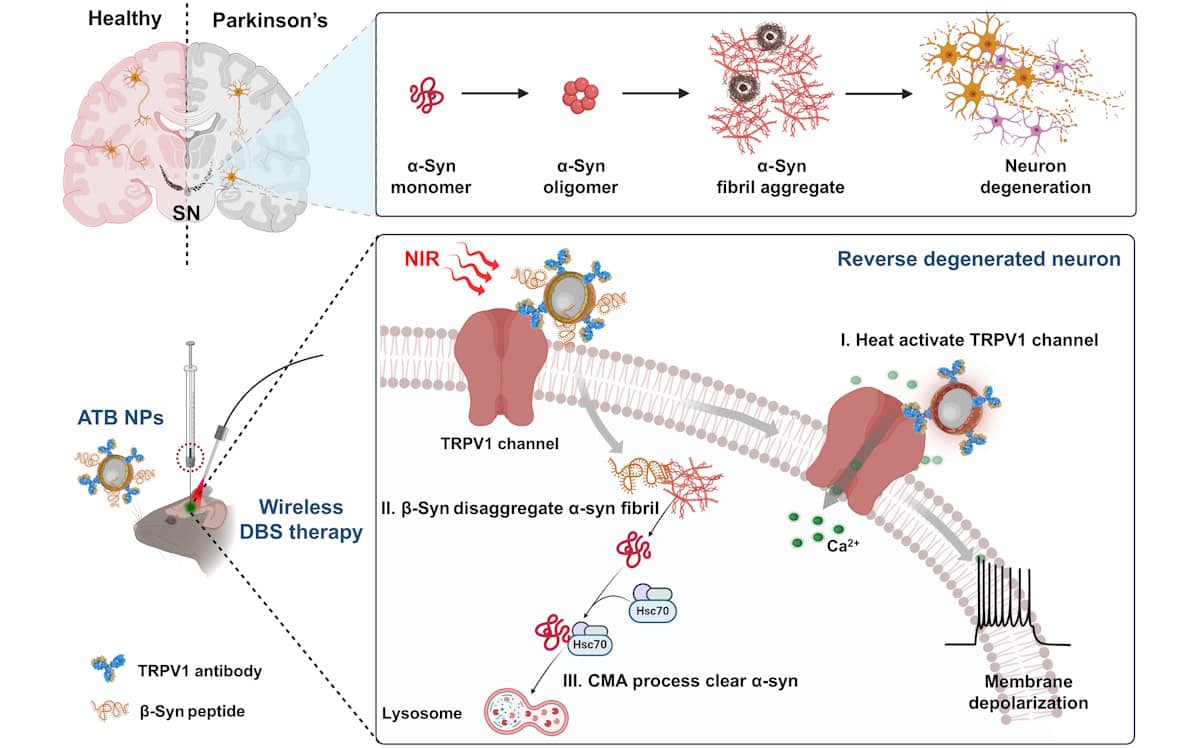
19 Fev 2025 - DBS mediado por nanopartículas reverte os sintomas da doença de Parkinson
A irradiação NIR pulsada DBS (I) mediada por nanopartículas desencadeia a ativação térmica dos canais TRPV1. (II, III) A liberação do peptídeo β-syn induzida por NIR nos neurônios desagrega as fibrilas α-syn e ativa termicamente a autofagia para limpar as fibrilas. Esta terapia reverte efetivamente os sintomas da doença de Parkinson. Criado usando BioRender.com. (Cortesia: CC BY-NC / Science Advances 10.1126 / sciadv.ado4927)
Um sistema de estimulação cerebral profunda (DBS) fototérmico baseado em nanopartículas reverteu com sucesso os sintomas da doença de Parkinson em camundongos de laboratório. Em desenvolvimento por pesquisadores em Pequim, China, o DBS injetável e sem fio não apenas reverteu a degeneração dos neurônios, mas também aumentou os níveis de dopamina, eliminando o acúmulo de fibrilas nocivas ao redor dos neurônios da dopamina. Após o tratamento com DBS, os camundongos doentes exibiram um comportamento locomotor quase comparável ao dos camundongos controle saudáveis.
A doença de Parkinson é um distúrbio cerebral crônico caracterizado pela degeneração dos neurônios produtores de dopamina e a subsequente perda de dopamina em regiões do cérebro. Os tratamentos atuais de DBS se concentram na amplificação da sinalização e produção de dopamina e podem exigir a implantação permanente de eletrodos no cérebro. Outra abordagem sob investigação é a optogenética, que envolve modificação genética. Ambas as técnicas aumentam os níveis de dopamina e reduzem os sintomas motores parkinsonianos, mas não restauram os neurônios degenerados para interromper a progressão da doença.
A equipe de pesquisa, do Centro Nacional de Nanociência e Tecnologia da Academia Chinesa de Ciências, levantou a hipótese de que o receptor sensível ao calor TRPV1, que é altamente expresso em neurônios dopaminérgicos, poderia servir como um alvo modulador para ativar neurônios dopaminérgicos na substância negra do mesencéfalo. Esta região contém uma grande concentração de neurônios dopaminérgicos e desempenha um papel crucial na forma como o cérebro controla o movimento corporal.
Estudos anteriores mostraram que a degeneração dos neurônios é impulsionada principalmente por fibrilas de α-sinucleína (α-syn) que se agregam na substância negra. O tratamento bem-sucedido, portanto, depende da remoção desse acúmulo, o que requer o reinício do processo autofágico intracelular (no qual uma célula se decompõe e remove componentes desnecessários ou disfuncionais).
Como tal, o investigador principal Chunying Chen e colegas pretendiam desenvolver um sistema terapêutico que pudesse reduzir o acúmulo de α-syn desagregando simultaneamente as fibrilas α-syn e iniciando o processo autofágico. Seu nanossistema DBS de três componentes, denominado ATB (Au@TRPV1@β-syn), combina nanopartículas de ouro fototérmicas, anticorpos TRPV1 ativadores de neurônios dopaminérgicos e peptídeos de β-sinucleína (β-syn) que quebram as fibrilas α-syn.
As nanopartículas ATB ancoram os neurônios da dopamina através do receptor TRPV1 e, agindo como nanoantenas, convertem a irradiação pulsada do infravermelho próximo (NIR) em calor. Isso ativa o receptor TRPV1 sensível ao calor e restaura os neurônios dopaminérgicos degenerados. Ao mesmo tempo, as nanopartículas liberam peptídeos β-syn que eliminam o acúmulo de fibrilas α-syn e estimulam a autofagia intracelular.
Os pesquisadores primeiro testaram o sistema in vitro em modelos celulares da doença de Parkinson. Eles verificaram que, sob irradiação a laser NIR, as nanopartículas de ATB ativam neurônios por meio de estimulação fototérmica, agindo no receptor TRPV1, e que as nanopartículas neutralizaram com sucesso a morte induzida por fibrila pré-formada α-syn (PFF) de neurônios dopaminérgicos. Nos ensaios de viabilidade celular, a morte dos neurônios foi reduzida de 68% para zero após o tratamento com nanopartículas de ATB.
Em seguida, Chen e colegas investigaram camundongos com doença de Parkinson induzida por PFF. O tratamento DBS começa com a injeção estereotáxica das nanopartículas de ATB diretamente na substância negra. Eles selecionaram essa abordagem em vez da administração sistêmica porque fornece direcionamento preciso, evita a barreira hematoencefálica e atinge uma alta concentração local de nanopartículas com uma dose baixa - potencialmente aumentando a eficácia do tratamento.
Após a injeção de nanopartículas ou solução salina, os camundongos foram submetidos à irradiação NIR pulsada uma vez por semana durante cinco semanas. A equipe então realizou uma série de testes para avaliar as habilidades motoras dos animais (após uma semana de treinamento), comparando o desempenho de camundongos PFF tratados e não tratados, bem como de camundongos de controle saudáveis. Isso incluiu o teste da vara rotativa, que mede o tempo até que o animal caia de uma haste rotativa que acelera de 5 a 50 rpm em 5 minutos, e o teste da vara, que registra o tempo para os ratos rastejarem por uma vara de 75 cm de comprimento.
Resultados de testes motores em camundongos
Motor tests Results of (left to right) rotarod, pole and open field tests, for control mice, mice with PFF-induced Parkinson’s disease, and PFF mice treated with ATB nanoparticles and NIR laser irradiation. (Courtesy: CC BY-NC/Science Advances 10.1126/sciadv.ado4927)
A equipe também realizou um teste de campo aberto para avaliar a atividade da locomotiva e o comportamento exploratório. Aqui, os ratos são livres para se mover em uma área de 50 x 50 cm, enquanto seus caminhos de movimento e o número de vezes que cruzam um quadrado central são registrados. Em todos os testes, os camundongos tratados com nanopartículas e irradiação superaram significativamente os controles não tratados, com desempenho quase comparável ao de camundongos saudáveis.
A visualização dos neurônios dopaminérgicos via imuno-histoquímica revelou uma redução nos neurônios em camundongos tratados com PFF em comparação com os controles. Essa perda foi revertida após o tratamento com nanopartículas. As avaliações de segurança determinaram que o tratamento não causou toxicidade bioquímica e que o calor gerado pelas nanopartículas de ATB irradiadas com NIR não causou nenhum dano considerável aos neurônios dopaminérgicos.
Oito semanas após o tratamento, nenhum dos camundongos apresentou toxicidades. As nanopartículas de ATB permaneceram estáveis na substância negra, com apenas algumas partículas migrando para o líquido cefalorraquidiano. Os pesquisadores também relatam que as partículas não migraram para o coração, fígado, baço, pulmão ou rim e não foram encontradas no sangue, urina ou fezes.
Chen diz ao Physics World que, tendo descoberto as propriedades neuroprotetoras dos aglomerados de ouro em modelos da doença de Parkinson, os pesquisadores agora estão investigando estratégias terapêuticas baseadas em aglomerados de ouro. Sua pesquisa atual se concentra na engenharia de nanocompósitos multifuncionais de cluster de ouro capazes de direcionar simultaneamente a agregação de α-syn, mitigando o estresse oxidativo e promovendo a regeneração do neurônio dopaminérgico. Fonte: physicsworld.
segunda-feira, 17 de fevereiro de 2025
A propagação da α-sinucleína patológica do rim para o cérebro pode contribuir para a doença de Parkinson
23 Janeiro 2025 - Resumo
A patogênese das doenças com corpos de Lewy (LBDs), incluindo a doença de Parkinson (DP), envolve a agregação de α-sinucleína (α-Syn) que se origina em órgãos periféricos e se espalha para o cérebro. A incidência de DP é aumentada em indivíduos com insuficiência renal crônica, mas os mecanismos subjacentes permanecem desconhecidos. Aqui observamos depósitos de α-Syn nos rins de pacientes com LBDs e no rim e no sistema nervoso central de indivíduos com doença renal terminal sem LBDs documentadas. Em camundongos machos, descobrimos que o rim remove α-Syn do sangue, que é reduzido na insuficiência renal, causando deposição de α-Syn no rim e subsequente disseminação para o cérebro. A injeção intrarrenal de fibrilas α-Syn induz a propagação da patologia α-Syn do rim para o cérebro, que é bloqueado pela denervação renal. A deleção de α-Syn nas células sanguíneas alivia a patologia em camundongos transgênicos α-Syn A53T. Assim, o rim pode atuar como um local de iniciação para a disseminação patogênica do α-Syn, e a função renal comprometida pode contribuir para o aparecimento de LBDs. Fonte: nature.