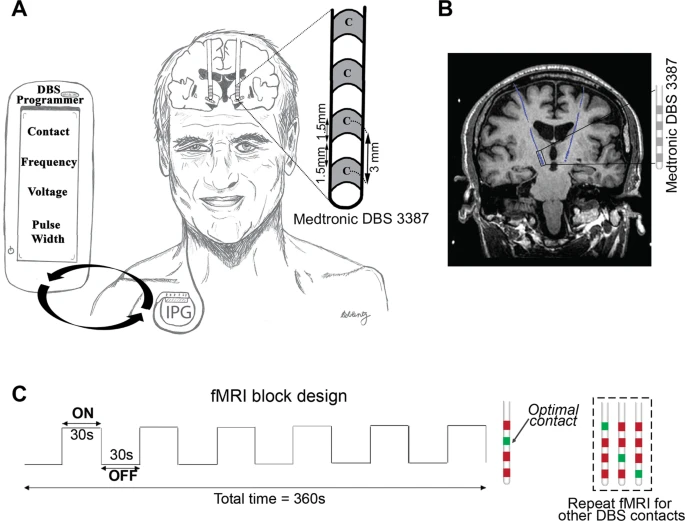
Você pode ver as posições anatômicas de dois eletrodos de estimulação cerebral. As estruturas anatômicas relevantes para a estimulação cerebral profunda na doença de Parkinson são mostradas em cores. As posições dos eletrodos foram determinadas com base em dados de imagens radiológicas individuais. O recém-desenvolvido software StimFit usa essas informações para calcular sugestões para configurações de estimulação eficazes. © Charité | Jan Roediger
A estimulação cerebral profunda (DBS) é uma opção de tratamento estabelecida para pacientes que sofrem da doença de Parkinson. Em um procedimento neurocirúrgico, dois eletrodos são implantados no cérebro para estimular permanentemente regiões específicas do cérebro. Definir os parâmetros de estimulação, no entanto, é um processo complexo. Uma equipe de pesquisa da Charité – Universitätsmedizin Berlin desenvolveu um algoritmo que pode aumentar a eficiência. Em seu estudo, publicado no The Lancet Digital Health*, os pesquisadores foram capazes de mostrar que as configurações de parâmetros sugeridas por um algoritmo recém-desenvolvido levaram à melhora dos sintomas motores comparáveis ao tratamento padrão.
A
doença de Parkinson é a segunda doença neurodegenerativa mais
comum depois da doença de Alzheimer. Na Alemanha, cerca de 400.000
pessoas são afetadas e, devido ao envelhecimento demográfico, os
números estão aumentando. Além do tremor parkinsoniano, um tremor
involuntário dos membros, um dos sintomas que afeta principalmente
os pacientes é o controle motor prejudicado. "Os pacientes se
sentem rígidos, acham mais difícil iniciar e parar os movimentos,
movem-se mais lentamente e têm uma marcha instável, que pode levar
a quedas", diz o Prof. Dr. Andrea Kühn, chefe da Unidade de
Distúrbios do Movimento e Neuromodulação do Departamento de
Neurologia e Neurologia Experimental do Charité. “Ainda não há
cura para a doença de Parkinson, mas a estimulação cerebral
profunda pode melhorar significativamente muitos sintomas,
especialmente os sintomas motores”.
A estimulação cerebral
profunda (DBS) envolve um procedimento cirúrgico durante o qual dois
eletrodos são implantados no cérebro do paciente. Esses eletrodos
emitem impulsos elétricos fracos e curtos que estimulam as
respectivas regiões cerebrais de maneira direcionada e contínua.
Fios que passam sob a pele conectam os eletrodos a um marca-passo na
cavidade torácica, que é usado para definir um grande número de
diferentes parâmetros de estimulação. Esses parâmetros podem ser
adaptados individualmente aos sintomas do paciente com Parkinson.
Três meses após o procedimento cirúrgico, os pacientes chegam ao
centro DBS por vários dias, durante os quais diferentes
configurações de estimulação são testadas para otimizar o
benefício do tratamento. “As configurações de estimulação são
ajustadas em nosso distúrbio de movimento especial. Para encontrar
uma boa configuração, testamos os respectivos efeitos e efeitos
colaterais de estimular os diferentes contatos do eletrodo
regularmente”, diz o Prof. Kühn. “Desenvolvemos o algoritmo
StimFit para tornar esse processo mais eficiente e, em última
análise, mais confortável para os pacientes”, diz Jan Roediger,
principal autor do estudo e também parte da Unidade de Distúrbios
do Movimento e Neuromodulação do Departamento de Neurologia e
Neurologia Experimental de Charité.
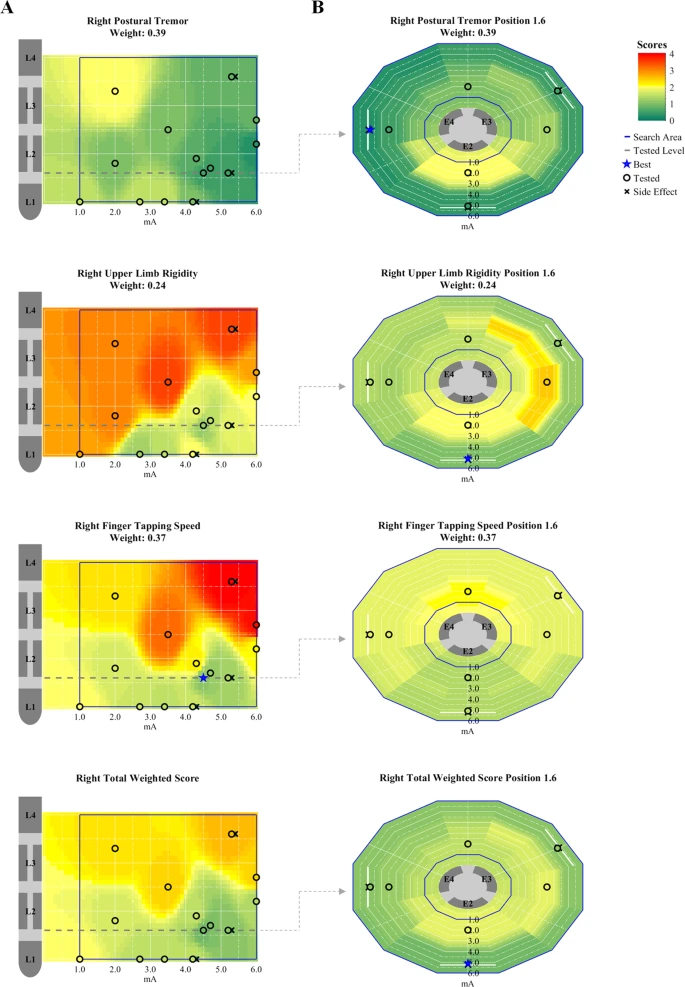
Com base em dados de
imagem radiológica do cérebro do paciente, o algoritmo calcula
sugestões para uma configuração de estimulação individual que
deve levar a uma melhora nos sintomas. Entre os parâmetros mais
importantes que precisam ser considerados estão a intensidade da
corrente e o posicionamento preciso das áreas de entrega de
estímulos dos eletrodos. "Usamos o software de código aberto
Lead-DBS, outro desenvolvimento da Charité, para determinar a
posição exata dos eletrodos no cérebro com base em dados de imagem
e incluí-los no algoritmo", diz Jan Roediger. “O próximo
passo foi treinar nosso algoritmo com um conjunto de dados de mais de
600 configurações de estimulação, dados de imagem associados e
efeitos na sintomatologia”.
Para descobrir se as
configurações sugeridas pelo StimFit podem competir com aquelas
determinadas por meio de testes clínicos, a equipe de pesquisa
realizou um estudo com 35 pacientes com doença de Parkinson. Ambos
os tipos de configurações de estimulação – as configurações
individuais criadas pelo teste clínico tradicional (procedimento
padrão de atendimento) e as configurações baseadas em algoritmos –
foram testadas sucessivamente. Nem os participantes do estudo nem os
profissionais médicos sabiam a ordem em que as configurações de
estimulação foram aplicadas. Posteriormente, a melhora motora em
ambas as condições de estimulação foi avaliada e comparada,
respectivamente. “A mobilidade geral dos pacientes e também sua
marcha melhoraram igualmente bem com os dois tipos de configurações
de estimulação”, diz o Prof. Kühn. “Este é um resultado
verdadeiramente promissor. Algoritmos baseados em imagem podem
simplificar significativamente a prática clínica de THS na doença
de Parkinson e outros distúrbios do movimento no futuro. Isso nos
permitiria aproveitar os últimos avanços técnicos de forma mais
completa, incluindo eletrodos multicontato para estimulação
direcional.”
A expressão dos sintomas de Parkinson, como
imobilidade, distúrbios da marcha ou tremor involuntário, varia de
pessoa para pessoa e deve ser considerada ao definir os estimuladores
cerebrais. Os pesquisadores planejam levar esse fato em consideração
na otimização técnica adicional do algoritmo. Eles também estão
trabalhando no desenvolvimento de modelos que podem prever a
probabilidade de efeitos colaterais com mais precisão. Isso os
ajudará a melhorar as configurações de estimulação baseadas em
algoritmos e o resultado terapêutico futuro, além de abrir caminho
para novos ensaios clínicos. Original em inglês, tradução Google,
revisão Hugo. Fonte: Charite.