Descobertas reforçam o
papel crucial do eixo intestino-cérebro no desenvolvimento da doença
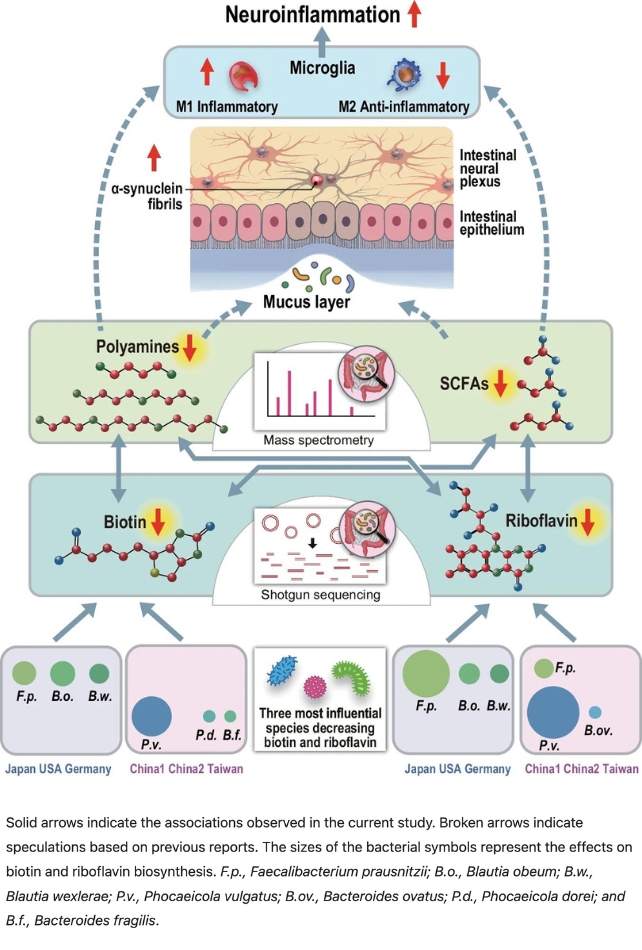
Esta ilustração
mostra em detalhes uma variedade de bactérias.
4 de novembro de 2025 -
Pessoas com doença de Parkinson apresentam uma abundância aumentada
da bactéria oral Streptococcus mutans — normalmente encontrada na
boca e associada a cáries dentárias — em seu intestino, de acordo
com um novo estudo envolvendo pacientes e um modelo em camundongos.
Uma vez estabelecidas
no intestino, essas bactérias — chamadas de S. mutans — podem
produzir metabólitos, como o propionato de imidazol, que viajam até
o cérebro e causam a perda de neurônios dopaminérgicos. A perda
desses neurônios, ou células nervosas, impulsiona o desenvolvimento
da doença de Parkinson.
Essas descobertas,
segundo os pesquisadores, reforçam ainda mais a importância do
chamado eixo intestino-cérebro no desenvolvimento da doença de
Parkinson. Os resultados da pesquisa também identificam novos alvos
terapêuticos potenciais para a doença de Parkinson, relacionados às
bactérias intestinais, segundo a equipe.
O estudo, intitulado "A
produção microbiana intestinal de propionato de imidazol impulsiona
as patologias da doença de Parkinson", foi publicado na revista
Nature Communications. A equipe internacional de pesquisadores foi
liderada conjuntamente por Yunjong Lee, PhD, da Faculdade de Medicina
da Universidade Sungkyunkwan, e Ara Koh, PhD, da Universidade de
Ciência e Tecnologia de Pohang, na República da Coreia, juntamente
com dois doutorandos, um de cada universidade.
"Nosso estudo
fornece uma compreensão mecanística de como os micróbios orais no
intestino podem influenciar o cérebro e contribuir para o
desenvolvimento da doença de Parkinson", disse Koh em um
comunicado à imprensa da universidade detalhando as descobertas do
estudo.
"Ele destaca o
potencial de direcionar a microbiota intestinal como uma estratégia
terapêutica, oferecendo uma nova direção para o tratamento da
doença de Parkinson", acrescentou Koh.
Descobertas ressaltam o
'papel crucial' do eixo intestino-cérebro no desenvolvimento da
doença
Pessoas com doença de
Parkinson apresentam uma abundância aumentada da bactéria oral
Streptococcus mutans — normalmente encontrada na boca e associada a
cáries nos dentes — em seu intestino, de acordo com um novo estudo
envolvendo pacientes e um modelo de camundongo.
Uma vez estabelecidas
no intestino, essas bactérias — chamadas de S. mutans — podem
produzir metabólitos, como o propionato de imidazol, que viajam até
o cérebro e causam a perda de neurônios dopaminérgicos. A perda
desses neurônios, ou células nervosas, impulsiona o desenvolvimento
da doença de Parkinson.
Essas descobertas,
segundo os pesquisadores, reforçam ainda mais a importância do
chamado eixo intestino-cérebro no desenvolvimento da doença de
Parkinson. Os resultados da pesquisa também identificam novos alvos
terapêuticos potenciais para a doença de Parkinson, relacionados às
bactérias intestinais, de acordo com a equipe.
O estudo, intitulado "A
produção microbiana intestinal de propionato de imidazol impulsiona
as patologias da doença de Parkinson", foi publicado na revista
Nature Communications. A equipe internacional de pesquisadores foi
liderada conjuntamente por Yunjong Lee, PhD, da Faculdade de Medicina
da Universidade Sungkyunkwan, e Ara Koh, PhD, da Universidade de
Ciência e Tecnologia de Pohang, na República da Coreia, juntamente
com dois doutorandos, um de cada universidade.
"Nosso estudo
fornece uma compreensão mecanística de como os micróbios orais no
intestino podem influenciar o cérebro e contribuir para o
desenvolvimento da doença de Parkinson", disse Koh em um
comunicado à imprensa da universidade detalhando as descobertas do
estudo.
"Ele destaca o
potencial de direcionar a microbiota intestinal como uma estratégia
terapêutica, oferecendo uma nova direção para o tratamento da
doença de Parkinson", acrescentou Koh.
Microbioma intestinal
de pacientes revela perfil bacteriano único
Há evidências
crescentes de que o microbioma intestinal — os bilhões de
bactérias, vírus e outros micróbios que vivem no intestino —
desempenha um papel no desenvolvimento da doença de Parkinson. Por
exemplo, a microbiota intestinal é alterada em pessoas com
Parkinson, e aglomerados tóxicos da proteína alfa-sinucleína, uma
característica da doença, parecem se originar no intestino e depois
se espalhar para o cérebro.
“No entanto, os
micróbios específicos que contribuem para as principais
características patológicas [causadoras da doença] da DP [doença
de Parkinson] ainda não foram identificados”, escreveram os
pesquisadores.
Cientistas identificam
Streptococcus mutans como bactéria oral chave na doença de
Parkinson
Um estudo recente de
amostras fecais de pessoas com e sem Parkinson ajudou a fornecer uma
compreensão abrangente dos micróbios que estão anormalmente baixos
ou altos em pessoas com Parkinson.
Agora, a equipe de
pesquisa confirmou esses dados e descobriu que a S. mutans —
bactéria normalmente encontrada na boca humana e associada à cárie
dentária — apresenta uma das maiores associações com a doença
de Parkinson.
A S. mutans produz uma
enzima chamada urocanato redutase (UrdA), que participa de uma reação
que produz uma substância química chamada propionato de imidazol
(ImP). O ImP tem recebido considerável atenção como alvo
terapêutico em diversas doenças.
Neste estudo, os
pesquisadores examinaram dados genéticos de 491 pessoas com
Parkinson e 234 idosos saudáveis, que serviram como grupo de
controle. A equipe descobriu que os níveis de UrdA eram
significativamente maiores nos pacientes com Parkinson. Em comparação
com o grupo de controle, os pacientes também apresentaram níveis
mais elevados de ImP no sangue, conforme demonstraram os dados.
Em camundongos,
descobriu-se que S. mutans se estabelece no intestino e prospera
Para investigar
especificamente se S. mutans poderia contribuir para a doença de
Parkinson, os pesquisadores introduziram a bactéria no intestino de
camundongos livres de germes. Apesar de ser tipicamente uma bactéria
oral, S. mutans se estabeleceu com sucesso no intestino,
especialmente no intestino grosso — e prosperou nele, observaram os
pesquisadores.
Além disso, esses
camundongos apresentaram perda seletiva de neurônios dopaminérgicos
no cérebro. Essas células nervosas produzem um mensageiro químico
chamado dopamina e são progressivamente perdidas na doença de
Parkinson.
A bactéria também
causou inflamação no cérebro e anormalidades em células de
suporte em forma de estrela chamadas astrócitos. Os níveis de ImP
aumentaram tanto no sangue quanto no cérebro dos camundongos somente
quando S. mutans estava presente, sugerindo que o ImP produzido no
intestino pode viajar pela corrente sanguínea até o cérebro.
Nossos resultados
destacam o papel crucial do propionato de imidazol microbiano
derivado do intestino como um mediador chave nos mecanismos da doença
de Parkinson e indicam potenciais opções terapêuticas direcionadas
ao eixo intestino-cérebro.
Para confirmar o papel
da UrdA, os pesquisadores modificaram a Escherichia coli — uma
bactéria comum que normalmente habita o intestino — para produzir
a enzima. Camundongos portadores dessas E. coli no intestino
desenvolveram uma perda semelhante de neurônios dopaminérgicos,
inflamação cerebral e sintomas motores, sugerindo que a UrdA
sozinha é suficiente para causar esses efeitos.
A equipe também
descobriu que o S. mutans, por meio da produção de ImP derivada da
UrdA, ativou um complexo de proteínas de sinalização chamado
mTORC1, que detecta a presença de proteínas mal dobradas que tendem
a formar aglomerados tóxicos. O bloqueio do mTORC1 reduziu a
inflamação e os danos aos neurônios no cérebro, além de aliviar
os sintomas motores, de acordo com os pesquisadores.
“Nossos resultados
reforçam o papel crucial do propionato de imidazol microbiano
derivado do intestino como um mediador chave nos mecanismos da doença
de Parkinson e indicam potenciais opções terapêuticas direcionadas
ao eixo intestino-cérebro”, concluíram os pesquisadores.
Ainda assim, a equipe
observou que grande parte de suas descobertas provém de um modelo
murino da doença. Portanto, são necessários mais estudos. Fonte: Parkinson´snewstoday.