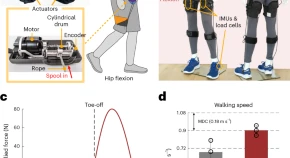
Uma pessoa vai dar um passo, mas, de repente, congela. A sensação é como se os pés tivessem ficado presos ao chão.
170720 - Esta é uma consequência frequente da doença de
Parkinson, o chamado "congelamento da marcha". Pesquisadores estimam que mais de um terço das pessoas com a doença têm este sintoma, que é uma causa frequente de quedas, dependência e má qualidade de vida.
Uma equipe da Universidade de São Paulo (USP), liderada pela pesquisadora Carla da Silva Batista e supervisionada por Carlos Ugrinowitsch, da Escola de Educação Física e Esporte da universidade, publicou em junho os resultados de um estudo clínico que mostrou a eficácia de um protocolo de treinamento para tratar do congelamento da marcha.
O estudo dividiu 32 pessoas com
Parkinson em dois grupos: um passou por fisioterapia tradicional (15 pessoas) e outro, um treino específico proposto pelos pesquisadores (17). Este combina exercícios de sobrecarga, coordenação motora, cognição e instabilidade com bolas e pranchas — sim, cair também fez parte do treinamento pelo qual os pacientes passaram por 12 semanas, em um total de 36 sessões.
O segundo grupo, que passou pelo treinamento específico, teve resultados melhores em vários critérios, observados em questionários respondidos pelos próprios pacientes, por avaliação médica do quadro e também por ressonância magnética (veja detalhes dos resultados abaixo).
"Construímos um conjunto de exercícios complexos, porque a complexidade induz à neuroplasticidade — que é a adaptação do cérebro a novos estímulos", explicou Carla Batista à BBC News Brasil, destacando que os problemas vividos por quem sofre do congelamento estão relacionados a uma parte do cérebro chamada região locomotora mesencefálica.
A neuroplasticidade cerebral se expressa, por exemplo, na formação de neurônios e sinapses, conexões entre eles.
"No treinamento específico para o congelamento da marcha, combinamos tarefas concomitantes, exercícios de coordenação, força e equilíbrio. Também trabalhamos o medo de cair, às vezes induzindo à queda — e os pacientes relataram não só melhora nos movimentos, mas também na percepção do medo."
 |
| Combinação de exercícios de equilíbrio, força e cognição mostrou bons resultados para tratar do chamado congelamento da marcha GETTY IMAGES |
Os resultados dos testes com os 32 participantes, todos tratados na Faculdade de Medicina da USP, foram publicados mês passado no Movement Disorders, periódico de sociedade internacional dedicada ao
Parkinson.
Carla Batista aparece com autora principal, ao lado de colegas da USP, da Universidade Federal do ABC, e também de universidades no exterior, fruto de períodos de estudo dela nos Estados Unidos. Ela fez parte do doutorado na Northwestern University e agora pós-doutorado na Oregon Health and Science University, nos dois casos com bolsas da Fundação de Amparo à Pesquisa do Estado de São Paulo (Fapesp).
O estudo publicado no Movement Disorders é do tipo clínico randomizado controlado (RCT, na sigla em inglês) — que envolve pacientes (clínico), divididos aleatoriamente (randomizado) em grupos, um deles usando o tratamento sob teste. Os experimentos, nesse caso, foram realizados entre junho de 2018 e abril de 2019.
Pelos relatos dos participantes, o grupo que participou do treino específico apontou maior melhora do que o grupo que seguiu a fisioterapia tradicional no congelamento da marcha em si (melhora de 20% vs. melhora de 1%) e na qualidade de vida (melhora de 23% vs. piora de 9%).
Na ressonância magnética, foi possível observar também a reativação das áreas do cérebro relacionadas ao congelamento da marcha. O modelo de análise de imagens de ressonância magnética usado neste estudo foi desenvolvido por equipes da USP e de pesquisadores dos EUA e Inglaterra, conforme apresentado em um artigo anterior, de 2017.
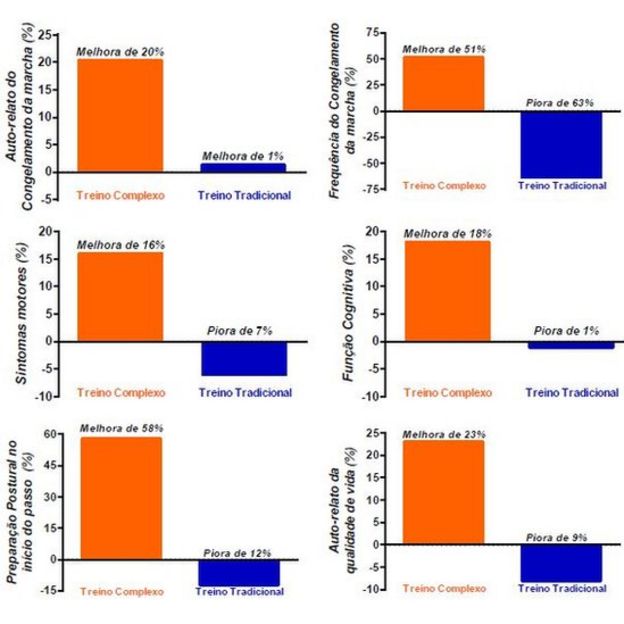 |
Gráficos enviados pela equipe à BBC News Brasil mostram diferentes indicadores em que treino complexo se mostrou superior
|
Já exames — ou seja, uma avaliação técnica e objetiva, e não relatos dos pacientes —, indicaram melhora de 51% na frequência do congelamento da marcha entre os que passaram por tratamento específico (versus piora de 63% na terapia tradicional) e, na chamada preparação postural no início do passo, melhora de 58% versus piora de 12%, segundo o estudo.
A preparação postural é um indicador importante, pois o congelamento da marcha normalmente ocorre no início do passo ou na virada do corpo, possivelmente por anormalidades motoras e cognitivas na configuração que precede o movimento.
O que uma pessoa que tem congelamento da marcha pode fazer hoje?
Entre os sintomas de
Parkinson, estão ainda rigidez nos músculos, lentidão nos movimentos corporais, tremores e perda de equilíbrio.
De acordo com Carla Batista, o congelamento pode durar de segundos a dois minutos. Há remédios e até uma cirurgia, de estimulação cerebral profunda, que são usados para tratar do congelamento da marcha — mas, segundo a pesquisadora, até hoje, os resultados destes tratamentos são considerados inconclusivos.
"Com nossa proposta de tratamento, estamos apostando em uma terapia de baixo custo — na comparação com uma cirurgia, por exemplo — e que é eficaz em modificar a doença, seja diminuindo, retardando ou até prevenindo o aparecimento do congelamento da marcha. No futuro, a terapia poderia ser incorporada pelo Sistema Único de Saúde, por exemplo", apontou.
Agora, um próximo passo previsto para testar o tratamento será fazer um estudo clínico com número maior de pessoas e, possivelmente, envolvendo pessoas que tenham
Parkinson mas não congelamento da marcha. A ideia é verificar se o treino específico desenvolvido pela equipe e aplicado durante dois anos é capaz de prevenir o aparecimento do sintoma.
Enquanto o tratamento não passa por esta nova validação e diante das incertezas atuais sobre remédios e cirurgias existentes, Batista diz que o paciente que passar pelo congelamento deve respirar fundo e depois tentar levantar a ponta do pé, seguida pelo calcanhar. Depois de respirar fundo, a pessoa pode tentar também balançar o corpo, jogando-o de um lado para o outro, até que venha um "gatilho" que dispara o movimento do passo.
 |
| Conhecida por seus sintomas motores, como tremor nas mãos, doença de Parkinson tem alcance mais amplo pouco a pouco descoberto, diz pesquisadora Direito de imagem GETTY IMAGES |
Graduada em educação física, Batista fez também seu doutorado na USP sobre o
Parkinson — ela também testou um protocolo de exercícios em pacientes com quadros leves a moderados, mostrando que este foi superior à fisioterapia tradicional e ao uso de remédios no alívio de diversos sintomas motores e não motores, como a capacidade cognitiva. Já no trabalho atual, que resultou no artigo recém-publicado, ela e sua equipe focaram especificamente no congelamento da marcha e em pessoas com quadros mais severos.
Um estudo publicado em 2018 na revista científica Lancet estimou que, no mundo, 6,1 milhões de pessoas viviam com
Parkinson em 2016. Para o Brasil, o número estimado foi de 128.836 (*).
O número global aumentou desde 1990, quando havia cerca de 2,5 milhões de pessoas com a doença. Mas, desde então, não foi somente a dimensão quantitativa da doença que mudou.
"Antes, acreditava-se que o
Parkinson afetasse somente indivíduos a partir da meia idade e na função motora — levando a músculos mais fracos, tremor… Hoje, entendemos que não se trata apenas de uma desordem motora, mas também cognitiva, gastrointestinal, cardiovascular… E temos evidências também de que pessoas acima dos 20 anos já podem ser afetadas", diz a pesquisadora.
Original em inglês, tradução Google, revisão Hugo. Fonte:
BBC.
(*) No mínimo 200 mil pessoas.