DBS controlado por corrente versus DBS controlado por tensão
Antecedentes do Estudo
A estimulação cerebral profunda (DBS) é um tratamento cirúrgico usado para aliviar alguns dos mais debilitantes sintomas de doença de
Parkinson avançada (DP). O tratamento ajuda a controlar os sintomas motores de DP usando um sistema médico DBS implantado cirurgicamente, um dispositivo que envia estimulação elétrica através de eletrodos (condutores metálicos) para partes específicas do cérebro que controlam o movimento.
Atualmente, dois tipos de sistemas DBS estão disponíveis para terapia DBS:
Sistemas controlados por tensão (VC): Sistemas DBS que controlam a estimulação do cérebro, ajustando os volts, ou a força que "empurra" a eletricidade do dispositivo.
Sistemas controlados pela corrente (CC): sistemas DBS que controlam a estimulação do cérebro, ajustando a corrente, ou a taxa que a eletricidade flui do dispositivo.
Embora a terapia DBS tradicionalmente use sistemas de tensão controlada, uma grande preocupação com VC na estimulação é que o acúmulo de tecido nos eletrodos pode causar alterações de resistência. Alteram a tensão (ou "intensidade") da estimulação que atinge o cérebro. Como resultado, pacientes com os sistemas VC podem:
Experienciar efeitos secundários indesejados devido a sobre-estimulação
Necessidade de que suas configurações de estimulação sejam reprogramadas várias vezes para sentir os benefícios do DBS.
No entanto, um estudo recente realizado por pesquisadores da Cleveland Clinic em Ohio estabeleceu que o uso de sistemas DBS controlados pela corrente podem minimizar as flutuações de tensão produzidas com alterações de resistência e - como resultado - ajudam a reduzir os efeitos colaterais da terapia DBS e o tempo necessário para programar cada dispositivo. Esta sugestão é baseada numa análise comparativa das flutuações de tensão que ocorrem durante o DBS controlado por tensão e por corrente.
Objetivo do Estudo
O objetivo do estudo foi examinar as flutuações nas tensões produzidas no cérebro durante o DBS controlado por tensão e corrente e para avaliar as vantagens potenciais de usar sistemas CC em vez de sistemas VC.
Durante o estudo, os pesquisadores compararam as tensões produzidas nos cérebros em dois laboratórios, primatas durante DBS controlado por tensão e corrente. Esses primatas incluíam dois
macacos, variando de 8 a 10 anos de idade e pesando aproximadamente 11-13lbs.
Métodos de Estudo
A fim de avaliar as vantagens potenciais da utilização de sistemas controlados por corrente para a terapia DBS, os pesquisadores usaram os seguintes métodos:
Primeiro, para entregar a terapia DBS aos cérebros dos macacos, os pesquisadores implantaram 3 eletrodos de DBS em regiões do cérebro de cada macaco (ou seja, globus Pálido, núcleo subtalâmico e regiões do tálamo do cérebro).
Em seguida, para monitorar a tensão de estimulação produzida no cérebro, os pesquisadores implantaram eletrodos de gravação de 2 mm de distância de cada eletrodo DBS. Esses eletrodos de gravação incluíam:
Eletrodos de gravação de canal único com um local de gravação
Eletrodos de gravação multicanal com vários locais de gravação.
Depois, para comparar as flutuações de tensão produzidas durante a tensão do DBS controlado pela corrente, os pesquisadores conectaram os eletrodos DBS de cada macaco a um VC e CC e conduziram as seguintes experiências examinando:
1. Mudanças de tensão após a implantação do eletrodo DBS: Para examinar como o acúmulo de tecido após o implante do eletrodo pode afetar as tensões produzidas durante o controle da voltagem no DBS, os pesquisadores:
Compararam as tensões máximas (máximas) registradas no cérebro de cada macaco.
No dia 1 e dia 7 após a implantação.
2. Mudanças de tensão durante DBS controlado por tensão: Para examinar como a estimulação contínua pode afetar as tensões produzidas durante DBS de tensão controlada, os pesquisadores:
Realizaram um conjunto de quatro experimentos para comparar as tensões de pico registradas no cérebro de cada macaco durante 60 minutos de estimulação de VC.
3. Mudanças de tensão ao longo do curso de DBS controlado por tensão versus controle de corrente:
Para examinar as diferenças nas flutuações de tensão produzidas ao longo do controle por tensão e controlada por corrente DBS, os pesquisadores:
Conduziram um conjunto de três experimentos para comparar as tensões de pico registradas após a estimulação inicial (1-segundo) de VC e CC e após contínua (60-Minuto) VC e estimulação CC.
Por fim, para monitorar as alterações de resistência relacionadas ao tecido que poderiam afetar as tensões registradas, durante cada experimento, os pesquisadores mediram:
A resistência elétrica de cada eletrodo DBS várias vezes durante cada experimento
A resistência elétrica dos eletrodos de gravação no início e no final de cada experimento.
Resultados do Estudo
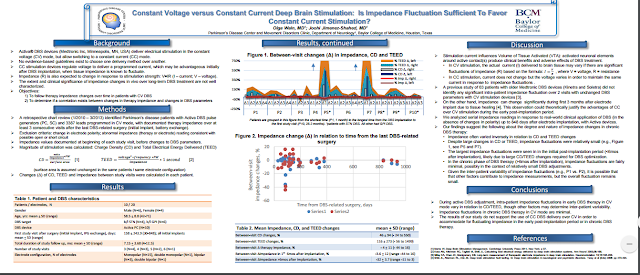
Em resposta às potenciais vantagens da utilização de sistemas controlados por corrente, os dados do estudo sugerem que - ao contrário da estimulação VC - voltagens produzidas no cérebro, durante o DBS controlado pela corrente são minimamente afetados por alterações de resistência relacionadas com os tecidos. Esta sugestão foi baseada em uma análise das mudanças de resistência e flutuações de tensão nos cérebros de dois macacos: 1) após a implantação do eletrodo DBS, 2) durante a fase contínua do DBS controlado por tensão, e 3) ao longo de DBS controlado por tensão versus controlado por corrente.
De acordo com as alterações de resistência relacionadas ao tecido e as gravações de voltagem no cérebro de cada macaco, os pesquisadores descobriram que:
Do dia 1 ao dia 7 após a implantação do eletrodo DBS:
O pico de tensão produzido no cérebro durante a tensão controlada do DBS diminuiu uma média de 38,6 ± 10,6%
A resistência elétrica dos eletrodos DBS aumentou em média de 298 ± 136%.
Durante 60 minutos de DBS de tensão contínua controlada:
O pico de tensão produzido no cérebro aumentou rapidamente durante os primeiros 10-15min de
Estimulação, aumentando em média 19,3 ± 6,2% após uma hora cheia de estimulação de VC
A resistência elétrica dos eletrodos DBS diminuiu rapidamente durante os primeiros 10-15min de estimulação, diminuindo em média 47,9 ± 16,7% após uma hora cheia de estimulação VC.
Durante o curso de DBS inicial (de 1 segundo) a contínuo (60 minutos) controlado por tensão e
DBS de corrente controlada:
O pico de tensão produzido no cérebro durante a tensão controlada no DBS aumentou significativamente em média de 54,8 ± 54,5%
O pico de tensão produzido no cérebro durante a corrente controlada no DBS aumentou minimamente por uma média de 6,5 ± 1,1%
A resistência elétrica dos eletrodos DBS diminuiu em média de 48,9 ± 30,1%.
Em conjunto, estes achados sugerem que: 1) o acúmulo de tecido após a implantação do eletrodo DBS causa um aumento na resistência do eletrodo que corresponde a uma diminuição nas tensões produzidas. Durante o DBS controlada por tensão, 2) a estimulação contínua através de elétrodos DBS inverte parte do acúmulo de tecido e provoca uma diminuição da resistência do eletrodo que corresponde a um aumento nas tensões produzidas durante o DBS controlado por tensão, e 3) As variações de tensão observadas ao longo da DBS controlada por tensão são reduzidas durante o DBS controlado pela corrente.
Discussão do Estudo e Implicações
Enquanto tecido ao redor dos eletrodos DBS naturalmente mudam como resultado da reação do corpo a um implante ou como consequência de uma estimulação prolongada, estas alterações do tecido podem alterar a resistência elétrica dos eletrodos DBS e produzir flutuações de tensão no DBS que podem contribuir para:
O aparecimento de efeitos secundários indesejados durante a estimulação DBS
Dificuldades na programação clínica de sistemas DBS.
Em geral, o estudo descobriu que as alterações na resistência do eletrodo DBS afeta voltagens produzidas no cérebro durante a DBS controlada por tensão. No entanto, essas flutuações de tensão podem ser minimizadas com o uso de DBS de corrente controlada. Este resultado é evidente pela variabilidade significativa das tensões produzidas nos cérebros dos macacos durante a estimulação de VC, e, em contraste, a estabilidade relativa das tensões produzidas no cérebros dos macacos durante a estimulação CC.
Com base nesses resultados, os pesquisadores recomendam que os sistemas controlados por corrente sejam substituídos por sistemas controlados por tensão como padrão, como hardware clínico para terapia DBS.
A adoção de sistemas CC podem oferecer três vantagens sobre os sistemas VC: 1) permitir uma
comparação precisa das configurações de estimulação entre os pacientes com DP, 2) reduzir as
indesejadas variáveis quando pesquisados os benefícios comportamentais e funcionais / efeitos colaterais da estimulação elétrica, e 3) fornecer um efeito de estimulação mais confiável durante a programação do hardware DBS. Contudo, o estudo foi realizado apenas em um modelo animal e envolveu apenas um pequeno número de indivíduos, Estudos adicionais devem ser conduzidos para explorar as vantagens potenciais do DBS numa amostra de estudo humano maior.
Original em inglês, tradução Google, revisão Hugo. Fonte:
dbs 4PD.
Ou seja: A estimulação por voltagem pode a médio e longo prazos provocar o aumento da resistência elétrica no entorno do eletrodo, levando a ser entregue ao alvo, voltagem inferior à programada. Este aumento de resistência pelo espessamento dos tecidos junto aos eletrodos não influenciaria muito na estimulação por corrente. Lembrando que os estimuladores, ora em desuso, Kinetra da Medtronic, não permitiam a estimulação por corrente (CC). Já tal opção é presente nos Activa SD e Activa RC. Os estimuladores da Abbott (ex St Jude) desconheço se possibilitam estimulação por ambos, tensão (VC) e corrente (CC), até onde sabia não teriam a opção tensão - voltagem (VC). O que, sem dúvida é uma desvantagem. Converse com seu médico.