Objetivo: atualização nos dispositivos de “Deep Brain Stimulation” aplicáveis ao parkinson. Abordamos critérios de elegibilidade (devo ou não devo fazer? qual a época adequada?) e inovações como DBS adaptativo (aDBS). Atenção: a partir de maio/20 fui impedido arbitrariamente de compartilhar postagens com o facebook. Com isto este presente blog substituirá o doencadeparkinson PONTO blogspot.com, abrangendo a doença de forma geral.
segunda-feira, 28 de agosto de 2023
Nilotinibe da KeifeRx para doença de Parkinson: probabilidade de aprovação
terça-feira, 28 de dezembro de 2021
Há descobertas promissoras para o tratamento do Parkinson
Por Mariza Tavares
Dois estudos indicam caminhos que podem levar a um novo patamar de intervenção terapêutica
28/12/2021 - Rio de Janeiro - Como prometi no domingo, a última semana de 2021 será dedicada a boas notícias. Para os pacientes com Doença de Parkinson, que ocupa o segundo lugar entre as desordens neurodegenerativas mais frequentes, há o que se comemorar. A enfermidade, que começa a se manifestar por volta dos 60 anos e é mais comum entre os homens, afeta a capacidade do cérebro de controlar os movimentos, levando a tremores, rigidez muscular e alterações de marcha e equilíbrio.
Pesquisadores da Universidade de Northwestern e do Centro Médico Weill Cornell, ambos nos Estados Unidos, e do Instituto de Biomedicina de Sevilha apresentaram um estudo promissor com camundongos que pode beneficiar quem se encontra num estágio avançado da doença. Nessa fase, o tratamento com a substância levodopa, que aumenta a quantidade de dopamina – neurotransmissor que ajuda a aliviar os sintomas do Parkinson – não apresenta a mesma eficácia. A nova terapia modificou geneticamente cobaias tendo como alvo a área do cérebro chamada substância negra, que é crucial para o controle motor, e restaurou a capacidade dos neurônios da região de converter a levodopa em dopamina.
A Doença de Parkinson afeta a capacidade do cérebro de controlar os movimentos, levando a tremores, rigidez muscular, lentidão de movimentos e alterações de marcha e equilíbrio — Foto: StockSnap para Pixabay
Na Universidade de Georgetown (EUA), os cientistas fizeram uma descoberta inesperada ao se deparar com o mau funcionamento da barreira hematoencefálica (BHE) em alguns pacientes com Parkinson. Essa barreira é formada por células endoteliais alinhadas com os capilares e forma uma estrutura que funciona como um “filtro”, permitindo a entrada de moléculas essenciais e dificultando que substâncias prejudiciais atinjam o sistema nervoso central e o líquido cefalorraquidiano. Nos casos analisados, a barreira tinha um comportamento anômalo: não deixava as toxinas saírem do cérebro e impedia os nutrientes de entrar. Num estudo com 75 participantes com Parkinson severo, eles foram tratados com a substância nilotinibe, normalmente utilizada em casos de leucemia mieloide crônica. Ao fim de 27 meses, a droga havia se mostrado eficiente em deter o declínio motor dessas pessoas, mas os cientistas ainda puderam festejar uma segunda descoberta. A análise epigenômica do líquido cefalorraquidiano dos indivíduos apontou que a nilotinibe também desativava uma proteína (DDR1) que era responsável por minar a capacidade da barreira hematoencefálica de funcionar corretamente. Quando a DDR1 era “neutralizada”, o “filtro” passava a funcionar e o nível de inflamação diminuía a ponto de o neurotransmissor dopamina voltar a ser produzido. Esse achado, publicado na revista científica “Neurology Genetics”, pode levar a um novo patamar de intervenção terapêutica. Na indústria farmacêutica, o que foi feito com a nilotinibe – testar medicamentos que já existem para avaliar sua eficácia contra outras doenças – chama-se reposicionamento de fármacos.
A Academia Norte-americana de Neurologia (AAN em inglês) divulgou recentemente uma atualização das recomendações da entidade para o uso de medicamentos dopaminérgicos – o documento anterior era de 2002. “Revisamos os estudos sobre a eficácia e os possíveis riscos dos medicamentos usados no manejo dos sintomas nos estágios iniciais da doença e avaliamos que, mesmo com os efeitos colaterais que toda droga apresenta, a levodopa é a melhor opção”, afirmou a médica Tamara Pringsheim, principal autora do trabalho. Ainda assim, a revisão feita pelos médicos da entidade fez a ressalva de que a levodopa tem mais chances de provocar discinesia (movimentos involuntários do rosto, braços, pernas ou tronco) nos cinco primeiros anos do tratamento. Para contornar o problema, a dose prescrita deve ser a mais baixa possível para chegar ao melhor custo/benefício. Fonte: G1.
terça-feira, 30 de novembro de 2021
Uma nova pesquisa destaca a causa potencial do Parkinson
30112021 - Um defeito na barreira hematoencefálica pode desempenhar um papel na doença de Parkinson, de acordo com a descoberta de uma pesquisa inovadora.
Pesquisadores do Georgetown University Medical Center dizem que sua descoberta, detalhada em um estudo publicado no início deste mês na Neurology Genetics, sugere que as paredes dos vasos sanguíneos, chamadas de barreira hematoencefálica, não funcionam corretamente em alguns pacientes com Parkinson.
Quando está funcionando corretamente, a barreira hematoencefálica atua como um filtro, mantendo as toxinas do lado de fora, enquanto permite que os nutrientes cheguem ao cérebro. Quando a barreira falha, entretanto, as toxinas ficam presas no cérebro, impedindo a entrada de glicose e outros nutrientes. Uma barreira disfuncional também permite que células inflamatórias e moléculas do corpo entrem no cérebro e causem danos.
"Ainda há muito trabalho a ser feito, mas apenas saber que o sistema vascular cerebral de um paciente está desempenhando um papel significativo na progressão da doença é uma descoberta muito promissora", disse o autor do estudo, Charbel Moussa, em um comunicado da universidade.
De acordo com o comunicado à imprensa, a pesquisa pode levar a novos tratamentos para a doença de Parkinson e pode ajudar a explicar as descobertas anteriores de que o medicamento nilotinibe, um medicamento para leucemia, estava relacionado a uma redução nos problemas de movimento e um aumento na qualidade de vida em pacientes com Parkinson.
"Até onde sabemos, este é o primeiro estudo a mostrar que a barreira hematoencefálica do corpo oferece potencialmente um alvo para o tratamento da doença de Parkinson", disse Moussa.
A nova descoberta vem de um ensaio clínico que apresentou uma análise abrangente do genoma de 75 pacientes com doença de Parkinson grave. Os resultados foram comparados antes e depois de receber tratamento off-label com nilotinibe ou placebo.
"O nilotinibe não apenas ativa o sistema de eliminação de lixo do cérebro para eliminar as proteínas tóxicas ruins, mas também parece reparar a barreira hematoencefálica para permitir que este lixo tóxico deixe o cérebro e os nutrientes entrem", disse Moussa.
“Acredita-se que a doença de Parkinson geralmente envolve déficits mitocondriais ou de energia que podem ser causados por toxinas ambientais ou pelo acúmulo de proteínas tóxicas. Nunca foi identificada como uma doença vascular”, acrescentou. Original em inglês, tradução Google, revisão Hugo. Fonte: AJC. Veja também aqui: MONDAY, Nov. 29, 2021 - New Insights Into What Might Drive Parkinson's Disease.
quinta-feira, 25 de novembro de 2021
Defeitos vasculares associados à progressão da doença de Parkinson
Descoberta publicada na revista “Neurology Genetics”
24 novembro 2021 | Investigadores da Universidade de Georgetown, nos Estados Unidos da América, identificaram um defeito vascular comum em doentes com doença de Parkinson moderadamente grave.
A investigação sugeriu que a barreira hematoencefálica, que protege o cérebro contra toxinas e permite a passagem de nutrientes para o mesmo, não funciona corretamente em alguns doentes com doença de Parkinson.
Os investigadores explicaram que esta proíbe as toxinas de saírem do cérebro e inibe a entrada de nutrientes como a glicose, no entanto, uma barreira disfuncional permite que células e moléculas inflamatórias do corpo entrem e danifiquem o cérebro.
Os investigadores sequenciaram o genoma inteiro do líquido cefalorraquidiano de 75 doentes com Parkinson, antes e depois do tratamento com um medicamento para a leucemia, o nilotinibe, ou um placebo.
A investigação mostrou que o nilotinibe inativou uma proteína chamada DDR1 que estava a destruir o funcionamento da barreira do cérebro. Quando a DDR1 foi inibida, o transporte normal das moléculas foi retomado e a inflamação diminuiu ao ponto de a dopamina, o neurotransmissor esgotado pela doença, ser novamente produzida.
Os investigadores concluíram que esta descoberta forneceu um novo potencial alvo para o tratamento da doença de Parkinson. Fonte: Alert.
domingo, 14 de novembro de 2021
Defeitos vasculares parecem estar subjacentes à progressão da doença de Parkinson
November 13, 2021 - Vascular defects appear to underlie the progression of Parkinson's disease.
Resumo: Em uma descoberta inesperada, os pesquisadores identificaram o que parece ser um defeito vascular significativo em pacientes com doença de Parkinson moderadamente grave. A descoberta pode ajudar a explicar um resultado anterior do mesmo estudo, no qual o medicamento nilotinibe foi capaz de interromper o declínio motor e não motor (cognição e qualidade de vida) em longo prazo. (...)
quarta-feira, 22 de setembro de 2021
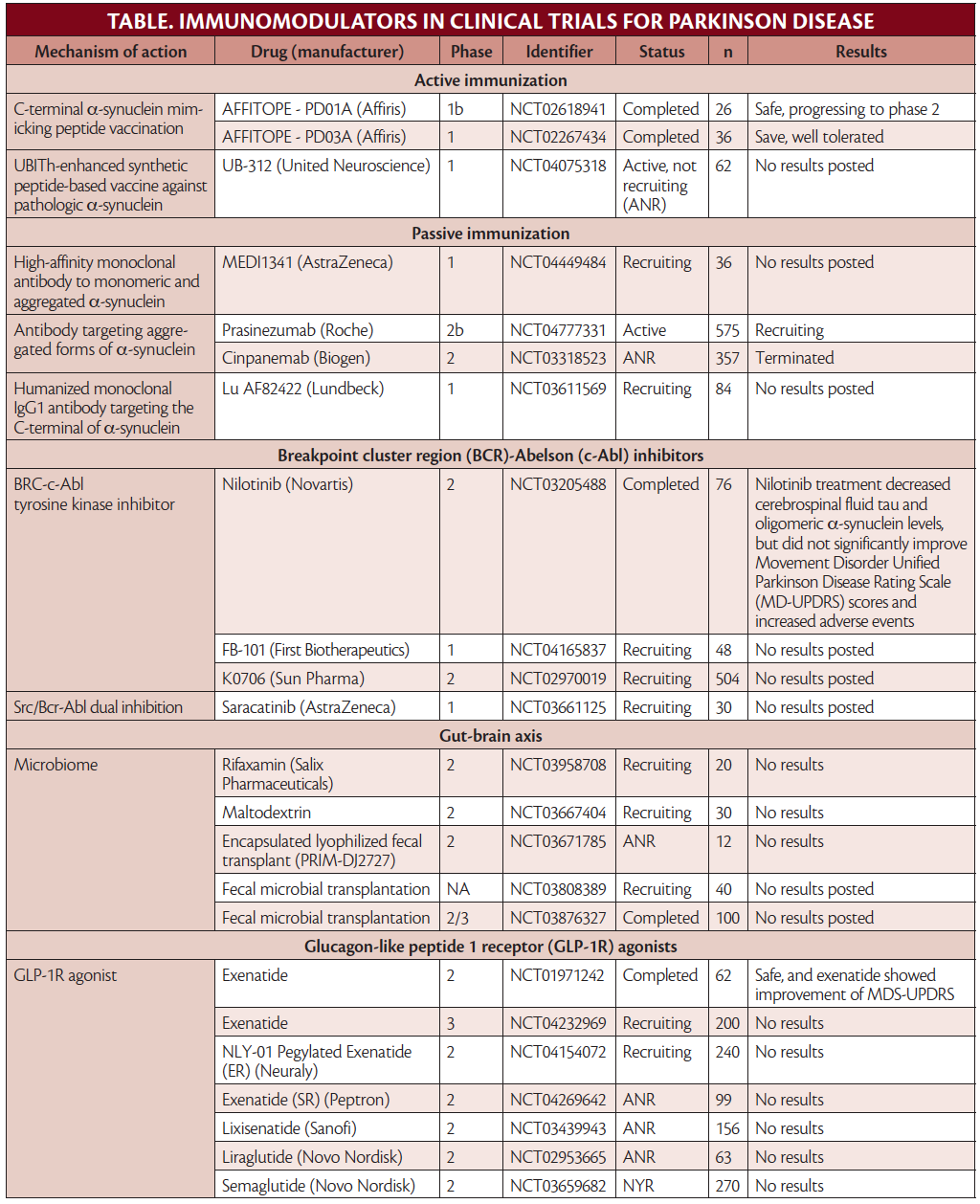
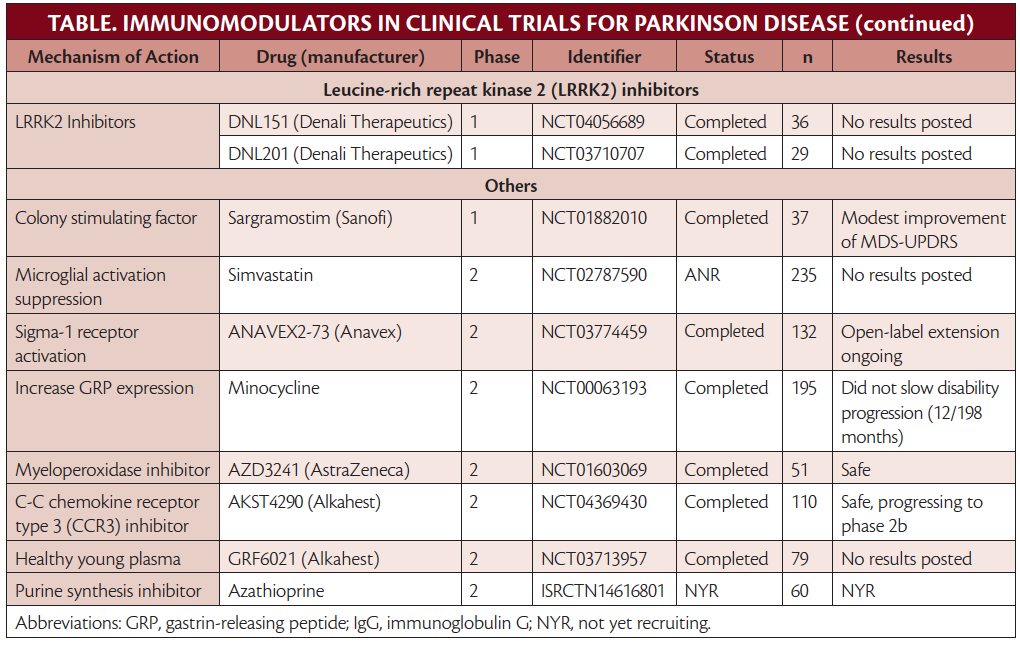
Imunomodulação para doença de Parkinson
Vários imunomoduladores estão sendo avaliados para o potencial tratamento da doença de Parkinson.
22 SEPTEMBER 2021 -
O termo neuroinflamação é usado com frequência, embora não haja
uma definição universalmente aceita. Conforme descrito em uma
revisão anexa, definimos neuroinflamação como uma resposta reativa
de células imunes e os mediadores que elas produzem (por exemplo,
citocinas, quimiocinas, espécies reativas de oxigênio e outros
mensageiros secundários), que causam inflamação do tecido neural.1
A neuroinflamação pode promover A agregação de α-sinucleína
(α-syn) para finalmente causar perda de células dopaminérgicas
(DA) na substância negra com agregados α-syn, denominados corpos de
Lewy, que são a marca registrada da doença de Parkinson (DP) .2 Foi
hipotetizado que α -syn patologia começa no intestino e viaja
através do nervo vago para entrar no sistema nervoso central (SNC)
no núcleo motor dorsal, embora isso tenha sido debatido desde
então.3 O tecido cerebral de pacientes com DP submetidos a
transplante nigral fetal mostrou aumento do citoplasma α-syn no
tecido transplantado, apoiando a teoria de que α-syn pode se
propagar entre as células, de forma semelhante aos príons.4 À
medida que a agregação de α-syn e os efeitos neuroinflamatórios
se acumulam, estes podem causar perda de células DA e sintomas e
sinais subsequentes de DP.5 Considerando esse possível mecanismo
patogênico, existem vários imunomoduladores - tratamentos que
aumentam ou suprimem várias etapas funcionais do sistema imunológico
- sob investigação para o tratamento de pacientes com DP, 6 que
revisamos aqui. Em um artigo anexo, revisamos as evidências para um
papel da neuroinflamação na patologia da DP.
Imunoterapia
visando α-sinucleína
Como os agregados de α-syn em corpos de
Lewy de DP são uma marca patológica da doença, a segmentação de
α-syn tem sido considerada uma terapia potencial. Anticorpos
monoclonais específicos direcionados a α-syn extracelular foram
estudados (Tabela). Estudos de fase 2 usando imunização passiva (ou
seja, infusão de anticorpos monoclonais) contra α-syn foram
conduzidos e 1 continua em um estudo aberto, mas outro foi encerrado
porque os alvos primários e secundários não foram atingidos.7,8
Estes anticorpos direcionados a diferentes regiões de α-syn.
Existem também estudos em andamento de imunização ativa novamente
α-syn.9
Outro medicamento que tem como alvo α-syn, o nilotinib, é um inibidor da região do breakpoint cluster (BCR) -Abelson tirosina quinase (c-Abl) que foi aprovado para uso como quimioterapia na leucemia mieloide crônica. O nilotinib ajuda a interromper a produção descontrolada de granulócitos em maturação (principalmente neutrófilos). Propriedades neuroprotetoras do nilotinib foram observadas com potencial para inibir a autofagia, agregação e propagação de α-syn. Em um estudo de fase 2, no entanto, houve preocupação com relação à penetração do nilotinib no cérebro, e não foi eficaz em retardar a progressão da doença.10,11 Os autores deste estudo alertaram que isso não refuta os potenciais efeitos neuroprotetores de outras moléculas que atuam no via c-Abl, e várias estão sob investigação (Tabela).
Mirando Microglia
A microglia contribui para a neuroinflamação por meio da liberação de espécies reativas de oxigênio (consulte também Neuroinflamação na doença de Parkinson nesta edição). A mieloperoxidase gera espécies reativas de oxigênio na microglia e tem sido alvo de ensaios clínicos com o inibidor de mieloperoxidase, AZD3241. Em um estudo de fase 2, o AZD3241 foi seguro e diminuiu plausivelmente a ativação da microglia, sugerindo que estudos adicionais são necessários. O ensaio de fase 3 em andamento, no entanto, não é para DP, mas sim para atrofia de múltiplos sistemas (MSA), um distúrbio de movimento neurodegenerativo diferente também caracterizado pela patologia α-syn.12
Linfócitos-alvo
A azatioprina (AZA) é um imunossupressor sistêmico sendo avaliado para tratamento de DP em um estudo duplo-cego de fase 2 controlado por placebo, incluindo 60 participantes com DP inicial. Como em muitos outros estudos, pessoas com outras condições imunológicas são excluídas da participação, o que pode excluir indivíduos com DP que podem estar em maior risco de autoimunidade e com maior probabilidade de se beneficiar de AZA ou outros imunomoduladores.13 Um pequeno ensaio clínico de fase 2 de 18 participantes avaliando o uso de plasma fresco congelado intravenoso de doadores jovens saudáveis, com idade entre 18 e 25 anos, foi concluído e relatou melhora da cognição em participantes com DP e comprometimento cognitivo. O plasma fresco congelado tem vários efeitos no sistema imunológico e consiste em imunoglobulinas de doadores saudáveis(IgGs) e outros componentes plasmáticos do plasma (por exemplo, fatores de coagulação). Os resultados não foram publicados em um jornal revisado por pares, embora um comunicado à imprensa afirme que o uso é seguro com resultados positivos.14 O inibidor de quimiocina, AKST4290, que inibe o receptor de quimiocina CC 3 para prevenir o recrutamento de células imunes, está sendo testado para o tratamento de PD em um estudo de fase 3 (Tabela).
Sargramostim é um fator estimulador de colônia de granulócitos-macrófagos recombinante humano que aumenta as células Treg e é aprovado para recuperação de medula óssea em indivíduos que realizaram transplante de medula óssea. Em um ensaio clínico de fase 1 em pessoas com DP, o sargramostim foi seguro e bem tolerado com melhorias modestas no perfil imunológico, por meio do aumento da função e frequência das células Treg, e também dos sintomas motores, embora fosse um tamanho de amostra pequeno.15 Não o ensaio de fase 2 foi registrado no banco de dados National Clinical Trials.
Citocinas de direcionamento
Vários estudos sugerem imunoterapias que bloqueiam citocinas pró-inflamatórias (por exemplo, fator de necrose tumoral [TNF] ou interleucina [IL] -1 podem ter benefícios protetores. Revisões retrospectivas mostraram que, embora a incidência de DP seja maior entre pacientes com colite ulcerativa ou doença de Crohn , esses pacientes diminuíram a prevalência de DP se expostos a esteroides ou terapia antiTNF.16,17 A metanálise mostrou que o uso de ibuprofeno foi associado a um menor risco de desenvolver DP.18
Acredita-se que o receptor do peptídeo 1 semelhante ao glucagon (GLP-1-R) reduza a apoptose celular (isto é, morte celular programada) que ocorre em resposta às citocinas inflamatórias. Com o objetivo de aumentar esse efeito neuroprotetor, vários agonistas de GLP-1-R estão sob investigação (Tabela) .19 Essa classe de medicamentos está aprovada para tratar diabetes. Em um ensaio clínico de fase 2, randomizado, duplo-cego, controlado por placebo e em local único, 60 participantes com DP foram tratados com o agonista GLP-1-R exenatida ou placebo por 48 semanas, seguido por um período de eliminação de 12 semanas. O tratamento com exenatida foi seguro e melhorou a função clínica, conforme medido com os escores motores da Escala de Avaliação da Doença de Parkinson Unificada da Sociedade de Distúrbios do Movimento (MDS-UPDRS) em comparação com o placebo.20 Um estudo de fase 3 de exenatida está em andamento e um estudo de fase 2 avaliando a segurança e eficácia de exenatida peguilada em pessoas com DP. Outros agonistas de GLP-1-R sendo estudados para potencial tratamento de DP incluem lixisenatida, liraglutida e semaglutida.21
Visando o Microbioma
Há uma série de pequenos estudos em andamento de agentes direcionados ao microbioma intestinal. O eixo intestino-cérebro é complexo e o microbioma afeta o sistema imunológico por meio da expressão de citocinas, iniciando o sistema imunológico adaptativo e ativando inflamassomas, entre outros mecanismos. Os estudos direcionados ao microbioma intestinal incluem, mas não estão limitados a, transplante microbiano fecal, rifaximina e maltodextrina. Um pequeno estudo de transplante fecal aberto, que altera o microbioma, em 15 participantes com DP mostrou melhora dos sintomas motores e não motores com eventos adversos limitados.21 Estudos de fase 2 nesta categoria estão em andamento, com muitos ainda recrutando.
Visando Genes Relacionados ao Imune e Parkinson
Mutações da proteína quinase 2 de repetição rica em leucina (LRRK2) estão entre as causas mais comuns de DP hereditária autossômica dominante. LRRK2 está implicado na inflamação neuronal e sistêmica via inibição lisossomal. As células imunes expressam altos níveis de LRRK2 e algumas variantes da mutação de LRRK2 estão associadas a um risco aumentado de doenças inflamatórias autoimunes do intestino.23,24 Existem 2 inibidores de pequenas moléculas potentes, seletivos e penetrantes no cérebro de LRRK2 sendo investigados. Os dados de segurança da Fase I foram relatados apenas em comunicados à imprensa que declararam que todas as metas de segurança e biomarcadores foram alcançadas, e que essas pequenas moléculas irão progredir para os testes de fase 2.25
Conclusão
Esses estudos mostram que há uma série de mecanismos complexos nos quais a neuroinflamação está implicada na patogênese da DP. Ainda existem muitos ensaios terapêuticos promissores de imunomoduladores. Os ensaios que foram concluídos com resultados negativos podem ser, em parte, devido ao momento subótimo da administração da terapia, considerando que há morte significativa de neurônios dopaminérgicos no momento em que os pacientes apresentam sintomas motores de DP e neuroinflamação foi implicada no estágios iniciais da patogênese da doença. Há uma série de outros medicamentos sob investigação que atuam no sistema imunológico com o objetivo de retardar a progressão da doença na DP, e esta não é uma lista completa (Tabela). Muitos outros imunomoduladores têm se mostrado promissores em contextos pré-clínicos e ainda não chegaram ao leito de pacientes com DP.26 Dados os vários mecanismos pelos quais a neuroinflamação leva à patogênese da doença em pacientes com DP, esses medicamentos fornecem uma fronteira promissora no tratamento da DP. Original em inglês, tradução Google, revisão Hugo. Fonte: Practicalneurology.
sexta-feira, 1 de janeiro de 2021
Estudo de segurança, tolerabilidade, farmacocinética e eficácia do radotinibe na doença de Parkinson
December 31, 2020 - Este estudo será conduzido para determinar se o Radotinibe é seguro e pode ser tolerado por pacientes com doença de Parkinson (DP) e para saber se o Radotinibe pode ser um agente terapêutico potencial para o tratamento da DP.
O radotinibe foi aprovado pelo Ministério de Alimentos e Segurança de Medicamentos da Coréia para tratar a Leucemia Mielóide Crônica (LMC), mas não foi aprovado para DP.
Em um estudo de eficácia não clínico, o efeito terapêutico de Radotinib HCl, inibidor de c-Abl, que exibe propriedades farmacocinéticas melhoradas e penetração BBB em comparação com nilotinib e outros inibidores de c-Abl, foi testado em um modelo de fibrilas pré-formadas de α-sinucleína (PFF) esporádicas PD. Como resultado, o tratamento de Radotinib HCl protege a toxicidade neuronal induzida por PFFs de α-sinucleína, reduz a patologia do tipo LB / LN induzida por PFFs e inibe a ativação de c-Abl induzida por PFFs em neurônios. Estudos in vivo demonstram que a administração de Radotinib HCl evita a perda de neurônios de dopamina e déficits comportamentais após toxicidade induzida por PFFs de α-sinucleína. Tomados em conjunto, esses achados indicam que o Radotinib HCl tem efeitos neuroprotetores benéficos na DP e fornece forte evidência de que inibidores seletivos e permeáveis ao cérebro c-Abl podem ser agentes terapêuticos potenciais para o tratamento da DP.
Esses dados são muito convincentes para avaliar os efeitos do Radotinibe em um ensaio clínico de fase II, randomizado, duplo-cego e controlado por placebo em pacientes com DP. Original em inglês, tradução Google, revisão Hugo. Fonte: Clinical Trials.
sábado, 30 de maio de 2020
O nilotinib é seguro na doença de Parkinson moderada e avançada
Leia mais sobre nilotinib AQUI.
/i.s3.glbimg.com/v1/AUTH_59edd422c0c84a879bd37670ae4f538a/internal_photos/bs/2021/u/a/4zqNBRTweBi4vs8KAL3g/idosocombola.jpg)