19 Fev 2025 - DBS
mediado por nanopartículas reverte os sintomas da doença de
Parkinson
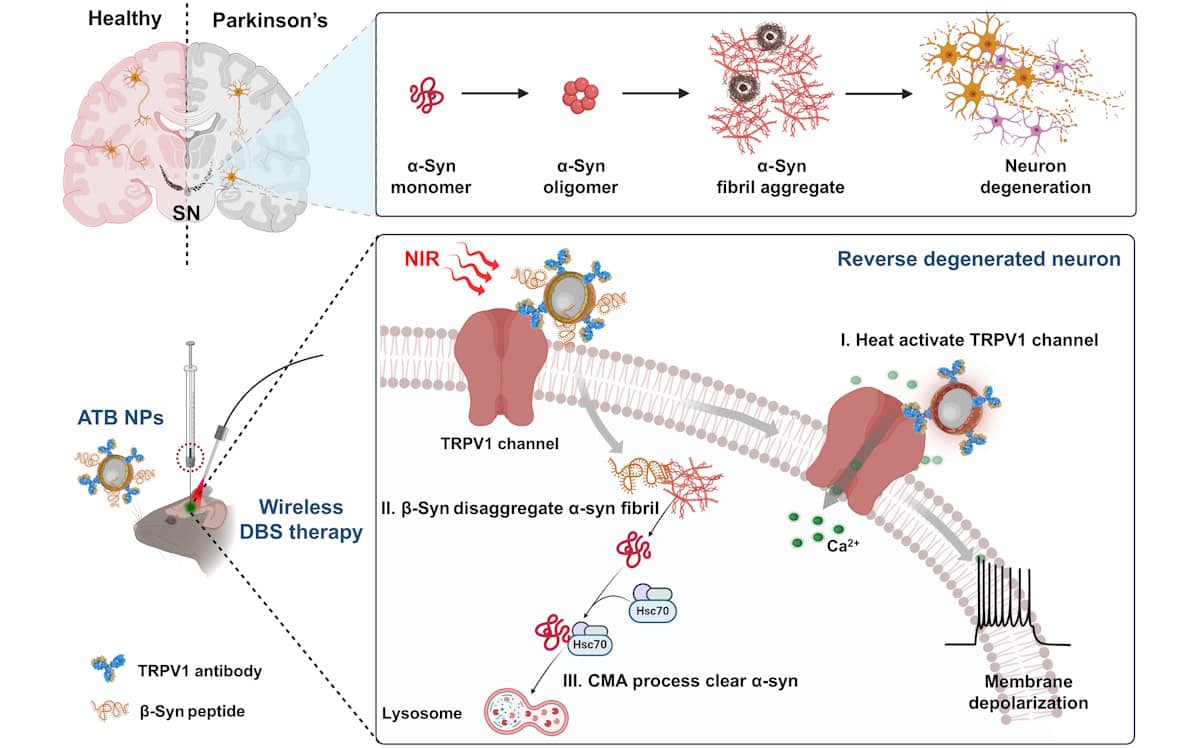
A irradiação NIR
pulsada DBS (I) mediada por nanopartículas desencadeia a ativação
térmica dos canais TRPV1. (II, III) A liberação do peptídeo β-syn
induzida por NIR nos neurônios desagrega as fibrilas α-syn e ativa
termicamente a autofagia para limpar as fibrilas. Esta terapia
reverte efetivamente os sintomas da doença de Parkinson. Criado
usando BioRender.com. (Cortesia: CC BY-NC / Science Advances 10.1126
/ sciadv.ado4927)
Um sistema de
estimulação cerebral profunda (DBS) fototérmico baseado em
nanopartículas reverteu com sucesso os sintomas da doença de
Parkinson em camundongos de laboratório. Em desenvolvimento por
pesquisadores em Pequim, China, o DBS injetável e sem fio não
apenas reverteu a degeneração dos neurônios, mas também aumentou
os níveis de dopamina, eliminando o acúmulo de fibrilas nocivas ao
redor dos neurônios da dopamina. Após o tratamento com DBS, os
camundongos doentes exibiram um comportamento locomotor quase
comparável ao dos camundongos controle saudáveis.
A doença de Parkinson
é um distúrbio cerebral crônico caracterizado pela degeneração
dos neurônios produtores de dopamina e a subsequente perda de
dopamina em regiões do cérebro. Os tratamentos atuais de DBS se
concentram na amplificação da sinalização e produção de
dopamina e podem exigir a implantação permanente de eletrodos no
cérebro. Outra abordagem sob investigação é a optogenética, que
envolve modificação genética. Ambas as técnicas aumentam os
níveis de dopamina e reduzem os sintomas motores parkinsonianos, mas
não restauram os neurônios degenerados para interromper a
progressão da doença.
A equipe de pesquisa,
do Centro Nacional de Nanociência e Tecnologia da Academia Chinesa
de Ciências, levantou a hipótese de que o receptor sensível ao
calor TRPV1, que é altamente expresso em neurônios dopaminérgicos,
poderia servir como um alvo modulador para ativar neurônios
dopaminérgicos na substância negra do mesencéfalo. Esta região
contém uma grande concentração de neurônios dopaminérgicos e
desempenha um papel crucial na forma como o cérebro controla o
movimento corporal.
Estudos anteriores
mostraram que a degeneração dos neurônios é impulsionada
principalmente por fibrilas de α-sinucleína (α-syn) que se agregam
na substância negra. O tratamento bem-sucedido, portanto, depende da
remoção desse acúmulo, o que requer o reinício do processo
autofágico intracelular (no qual uma célula se decompõe e remove
componentes desnecessários ou disfuncionais).
Como tal, o
investigador principal Chunying Chen e colegas pretendiam desenvolver
um sistema terapêutico que pudesse reduzir o acúmulo de α-syn
desagregando simultaneamente as fibrilas α-syn e iniciando o
processo autofágico. Seu nanossistema DBS de três componentes,
denominado ATB (Au@TRPV1@β-syn), combina nanopartículas de ouro
fototérmicas, anticorpos TRPV1 ativadores de neurônios
dopaminérgicos e peptídeos de β-sinucleína (β-syn) que quebram
as fibrilas α-syn.
As nanopartículas ATB
ancoram os neurônios da dopamina através do receptor TRPV1 e,
agindo como nanoantenas, convertem a irradiação pulsada do
infravermelho próximo (NIR) em calor. Isso ativa o receptor TRPV1
sensível ao calor e restaura os neurônios dopaminérgicos
degenerados. Ao mesmo tempo, as nanopartículas liberam peptídeos
β-syn que eliminam o acúmulo de fibrilas α-syn e estimulam a
autofagia intracelular.
Os pesquisadores
primeiro testaram o sistema in vitro em modelos celulares da doença
de Parkinson. Eles verificaram que, sob irradiação a laser NIR, as
nanopartículas de ATB ativam neurônios por meio de estimulação
fototérmica, agindo no receptor TRPV1, e que as nanopartículas
neutralizaram com sucesso a morte induzida por fibrila pré-formada
α-syn (PFF) de neurônios dopaminérgicos. Nos ensaios de
viabilidade celular, a morte dos neurônios foi reduzida de 68% para
zero após o tratamento com nanopartículas de ATB.
Em seguida, Chen e
colegas investigaram camundongos com doença de Parkinson induzida
por PFF. O tratamento DBS começa com a injeção estereotáxica das
nanopartículas de ATB diretamente na substância negra. Eles
selecionaram essa abordagem em vez da administração sistêmica
porque fornece direcionamento preciso, evita a barreira
hematoencefálica e atinge uma alta concentração local de
nanopartículas com uma dose baixa - potencialmente aumentando a
eficácia do tratamento.
Após a injeção de
nanopartículas ou solução salina, os camundongos foram submetidos
à irradiação NIR pulsada uma vez por semana durante cinco semanas.
A equipe então realizou uma série de testes para avaliar as
habilidades motoras dos animais (após uma semana de treinamento),
comparando o desempenho de camundongos PFF tratados e não tratados,
bem como de camundongos de controle saudáveis. Isso incluiu o teste
da vara rotativa, que mede o tempo até que o animal caia de uma
haste rotativa que acelera de 5 a 50 rpm em 5 minutos, e o teste da
vara, que registra o tempo para os ratos rastejarem por uma vara de
75 cm de comprimento.
Resultados de testes
motores em camundongos
Motor tests Results of
(left to right) rotarod, pole and open field tests, for control mice,
mice with PFF-induced Parkinson’s disease, and PFF mice treated
with ATB nanoparticles and NIR laser irradiation. (Courtesy: CC
BY-NC/Science Advances 10.1126/sciadv.ado4927)
A equipe também
realizou um teste de campo aberto para avaliar a atividade da
locomotiva e o comportamento exploratório. Aqui, os ratos são
livres para se mover em uma área de 50 x 50 cm, enquanto seus
caminhos de movimento e o número de vezes que cruzam um quadrado
central são registrados. Em todos os testes, os camundongos tratados
com nanopartículas e irradiação superaram significativamente os
controles não tratados, com desempenho quase comparável ao de
camundongos saudáveis.
A visualização dos
neurônios dopaminérgicos via imuno-histoquímica revelou uma
redução nos neurônios em camundongos tratados com PFF em
comparação com os controles. Essa perda foi revertida após o
tratamento com nanopartículas. As avaliações de segurança
determinaram que o tratamento não causou toxicidade bioquímica e
que o calor gerado pelas nanopartículas de ATB irradiadas com NIR
não causou nenhum dano considerável aos neurônios dopaminérgicos.
Oito semanas após o
tratamento, nenhum dos camundongos apresentou toxicidades. As
nanopartículas de ATB permaneceram estáveis na substância negra,
com apenas algumas partículas migrando para o líquido
cefalorraquidiano. Os pesquisadores também relatam que as partículas
não migraram para o coração, fígado, baço, pulmão ou rim e não
foram encontradas no sangue, urina ou fezes.
Chen diz ao Physics
World que, tendo descoberto as propriedades neuroprotetoras dos
aglomerados de ouro em modelos da doença de Parkinson, os
pesquisadores agora estão investigando estratégias terapêuticas
baseadas em aglomerados de ouro. Sua pesquisa atual se concentra na
engenharia de nanocompósitos multifuncionais de cluster de ouro
capazes de direcionar simultaneamente a agregação de α-syn,
mitigando o estresse oxidativo e promovendo a regeneração do
neurônio dopaminérgico. Fonte: physicsworld.