Objetivo: atualização nos dispositivos de “Deep Brain Stimulation” aplicáveis ao parkinson. Abordamos critérios de elegibilidade (devo ou não devo fazer? qual a época adequada?) e inovações como DBS adaptativo (aDBS). Atenção: a partir de maio/20 fui impedido arbitrariamente de compartilhar postagens com o facebook. Com isto este presente blog substituirá o doencadeparkinson PONTO blogspot.com, abrangendo a doença de forma geral.
quinta-feira, 30 de agosto de 2018
DBS ligado a distintas vias motoras e cognitivas no cérebro, achados que podem melhorar seu uso
Aug 30, 2018 - DBS Linked to Distinct Motor and Cognitive Pathways in Brain, Finding That May Improve Its Use.
quarta-feira, 29 de agosto de 2018
Nova rede cerebral ligada à dor crônica na doença de Parkinson
August 28, 2018 - Os cientistas revelaram uma nova rede cerebral que liga a dor na doença de Parkinson (DP) a uma região específica do cérebro, de acordo com um relatório publicado na revista eLife.
A pesquisa revela por que um subconjunto de neurônios em parte do cérebro chamado de núcleo subtalâmico é um alvo potencial para o alívio da dor na DP, bem como outras doenças, como demência, doença dos neurônios motores e Huntington, e certas formas de enxaqueca.
As pessoas com DP frequentemente relatam dor inexplicável, como sensação de queimação, dor aguda, coceira ou formigamento que não estão diretamente relacionadas aos seus outros sintomas de DP. O tratamento com estimulação cerebral profunda no núcleo subtalâmico pode ajudar com os sintomas relacionados ao movimento da DP, mas estudos recentes mostraram que também reduz a dor. A maneira como isso acontece, no entanto, ainda não está clara.
"Neste estudo, nos propusemos a determinar se o núcleo subtalâmico está envolvido na tradução de um estímulo nocivo, como lesão em dor, e se esta transmissão de informação é alterada na DP", explica Arnaud Pautrat, PhD Student at Grenoble Institut des Neurociências (Inserm, Instituto Nacional de Saúde e Pesquisa Médica / Universidade Grenoble Alpes), França.
A equipe começou usando a eletrofisiologia para medir o disparo de sinais elétricos em células nervosas no núcleo subtalâmico de ratos que receberam um choque na pata traseira. As células nervosas foram de fato ativadas temporalmente por essa estimulação. Eles também descobriram que os neurônios caíram em três grupos de resposta, mostrando um aumento, diminuição ou nenhuma mudança na sua taxa de disparo de linha de base.
Em seguida, eles analisaram se essas respostas causaram uma mudança na função cerebral. Ratos com um núcleo subtalâmico danificado levaram muito mais tempo para mostrar sinais de desconforto do que ratos saudáveis. Quando eles expandiram seu estudo para modelos de ratos com DP, a equipe descobriu que as células nervosas no núcleo subtalâmico tinham taxas de disparo mais altas e as respostas à dor eram maiores e mais longas do que nos animais saudáveis. Em conjunto, isso sugere que as vias disfuncionais de processamento da dor no núcleo subtalâmico são a causa da dor relacionada à DP.
Para entender de onde os sinais de dor para o núcleo subtalâmico estavam vindo, a equipe analisou duas estruturas cerebrais conhecidas por serem importantes na transmissão de sinais de dano da medula espinhal: o colículo superior e o núcleo parabraquial. O bloqueio de sua atividade revelou que ambas as estruturas desempenham um papel crucial na transmissão de informações sobre a dor para o núcleo subtalâmico, e que existe uma via de comunicação direta entre o núcleo parabraquial e o núcleo subtalâmico. Como resultado, a equipe acredita que esse caminho provavelmente está envolvido nos efeitos benéficos da estimulação cerebral profunda na dor na DP e que essas novas descobertas podem ajudar a direcionar a estimulação para partes específicas do cérebro para torná-la mais eficaz como uma dor apaziguada.
"Nós encontramos evidências de que o núcleo subtalâmico está funcionalmente ligado a uma rede de processamento de dor e que essas respostas são afetadas no Parkinsonismo", conclui a autora sênior e pesquisadora do Inserm, Veronique Coizet, PhD. "Mais experimentos são necessários para caracterizar completamente os efeitos da estimulação cerebral profunda nesta região do cérebro em nossos modelos experimentais, com o objetivo de encontrar maneiras de otimizá-la como um tratamento para a dor causada por Parkinson e outras doenças neurológicas." Original em inglês, tradução Google, revisão Hugo. Fonte: Science DailyOs cientistas revelaram uma nova rede cerebral que liga a dor na doença de Parkinson (DP) a uma região específica do cérebro, de acordo com um relatório publicado na revista eLife.
A pesquisa revela por que um subconjunto de neurônios em parte do cérebro chamado de núcleo subtalâmico é um alvo potencial para o alívio da dor na DP, bem como outras doenças, como demência, doença dos neurônios motores e Huntington, e certas formas de enxaqueca.
As pessoas com DP frequentemente relatam dor inexplicável, como sensação de queimação, dor aguda, coceira ou formigamento que não estão diretamente relacionadas aos seus outros sintomas de DP. O tratamento com estimulação cerebral profunda no núcleo subtalâmico pode ajudar com os sintomas relacionados ao movimento da DP, mas estudos recentes mostraram que também reduz a dor. A maneira como isso acontece, no entanto, ainda não está clara.
"Neste estudo, nos propusemos a determinar se o núcleo subtalâmico está envolvido na tradução de um estímulo nocivo, como lesão em dor, e se esta transmissão de informação é alterada na DP", explica Arnaud Pautrat, PhD Student at Grenoble Institut des Neurociências (Inserm, Instituto Nacional de Saúde e Pesquisa Médica / Universidade Grenoble Alpes), França.
A equipe começou usando a eletrofisiologia para medir o disparo de sinais elétricos em células nervosas no núcleo subtalâmico de ratos que receberam um choque na pata traseira. As células nervosas foram de fato ativadas temporalmente por essa estimulação. Eles também descobriram que os neurônios caíram em três grupos de resposta, mostrando um aumento, diminuição ou nenhuma mudança na sua taxa de disparo de linha de base.
Em seguida, eles analisaram se essas respostas causaram uma mudança na função cerebral. Ratos com um núcleo subtalâmico danificado levaram muito mais tempo para mostrar sinais de desconforto do que ratos saudáveis. Quando eles expandiram seu estudo para modelos de ratos com DP, a equipe descobriu que as células nervosas no núcleo subtalâmico tinham taxas de disparo mais altas e as respostas à dor eram maiores e mais longas do que nos animais saudáveis. Em conjunto, isso sugere que as vias disfuncionais de processamento da dor no núcleo subtalâmico são a causa da dor relacionada à DP.
Para entender de onde os sinais de dor para o núcleo subtalâmico estavam vindo, a equipe analisou duas estruturas cerebrais conhecidas por serem importantes na transmissão de sinais de dano da medula espinhal: o colículo superior e o núcleo parabraquial. O bloqueio de sua atividade revelou que ambas as estruturas desempenham um papel crucial na transmissão de informações sobre a dor para o núcleo subtalâmico, e que existe uma via de comunicação direta entre o núcleo parabraquial e o núcleo subtalâmico. Como resultado, a equipe acredita que esse caminho provavelmente está envolvido nos efeitos benéficos da estimulação cerebral profunda na dor na DP e que essas novas descobertas podem ajudar a direcionar a estimulação para partes específicas do cérebro para torná-la mais eficaz como uma dor apaziguada.
"Nós encontramos evidências de que o núcleo subtalâmico está funcionalmente ligado a uma rede de processamento de dor e que essas respostas são afetadas no Parkinsonismo", conclui a autora sênior e pesquisadora do Inserm, Veronique Coizet, PhD. "Mais experimentos são necessários para caracterizar completamente os efeitos da estimulação cerebral profunda nesta região do cérebro em nossos modelos experimentais, com o objetivo de encontrar maneiras de otimizá-la como um tratamento para a dor causada por Parkinson e outras doenças neurológicas." Original em inglês, tradução Google, revisão Hugo. Fonte: Science Daily.
A pesquisa revela por que um subconjunto de neurônios em parte do cérebro chamado de núcleo subtalâmico é um alvo potencial para o alívio da dor na DP, bem como outras doenças, como demência, doença dos neurônios motores e Huntington, e certas formas de enxaqueca.
As pessoas com DP frequentemente relatam dor inexplicável, como sensação de queimação, dor aguda, coceira ou formigamento que não estão diretamente relacionadas aos seus outros sintomas de DP. O tratamento com estimulação cerebral profunda no núcleo subtalâmico pode ajudar com os sintomas relacionados ao movimento da DP, mas estudos recentes mostraram que também reduz a dor. A maneira como isso acontece, no entanto, ainda não está clara.
"Neste estudo, nos propusemos a determinar se o núcleo subtalâmico está envolvido na tradução de um estímulo nocivo, como lesão em dor, e se esta transmissão de informação é alterada na DP", explica Arnaud Pautrat, PhD Student at Grenoble Institut des Neurociências (Inserm, Instituto Nacional de Saúde e Pesquisa Médica / Universidade Grenoble Alpes), França.
A equipe começou usando a eletrofisiologia para medir o disparo de sinais elétricos em células nervosas no núcleo subtalâmico de ratos que receberam um choque na pata traseira. As células nervosas foram de fato ativadas temporalmente por essa estimulação. Eles também descobriram que os neurônios caíram em três grupos de resposta, mostrando um aumento, diminuição ou nenhuma mudança na sua taxa de disparo de linha de base.
Em seguida, eles analisaram se essas respostas causaram uma mudança na função cerebral. Ratos com um núcleo subtalâmico danificado levaram muito mais tempo para mostrar sinais de desconforto do que ratos saudáveis. Quando eles expandiram seu estudo para modelos de ratos com DP, a equipe descobriu que as células nervosas no núcleo subtalâmico tinham taxas de disparo mais altas e as respostas à dor eram maiores e mais longas do que nos animais saudáveis. Em conjunto, isso sugere que as vias disfuncionais de processamento da dor no núcleo subtalâmico são a causa da dor relacionada à DP.
Para entender de onde os sinais de dor para o núcleo subtalâmico estavam vindo, a equipe analisou duas estruturas cerebrais conhecidas por serem importantes na transmissão de sinais de dano da medula espinhal: o colículo superior e o núcleo parabraquial. O bloqueio de sua atividade revelou que ambas as estruturas desempenham um papel crucial na transmissão de informações sobre a dor para o núcleo subtalâmico, e que existe uma via de comunicação direta entre o núcleo parabraquial e o núcleo subtalâmico. Como resultado, a equipe acredita que esse caminho provavelmente está envolvido nos efeitos benéficos da estimulação cerebral profunda na dor na DP e que essas novas descobertas podem ajudar a direcionar a estimulação para partes específicas do cérebro para torná-la mais eficaz como uma dor apaziguada.
"Nós encontramos evidências de que o núcleo subtalâmico está funcionalmente ligado a uma rede de processamento de dor e que essas respostas são afetadas no Parkinsonismo", conclui a autora sênior e pesquisadora do Inserm, Veronique Coizet, PhD. "Mais experimentos são necessários para caracterizar completamente os efeitos da estimulação cerebral profunda nesta região do cérebro em nossos modelos experimentais, com o objetivo de encontrar maneiras de otimizá-la como um tratamento para a dor causada por Parkinson e outras doenças neurológicas." Original em inglês, tradução Google, revisão Hugo. Fonte: Science DailyOs cientistas revelaram uma nova rede cerebral que liga a dor na doença de Parkinson (DP) a uma região específica do cérebro, de acordo com um relatório publicado na revista eLife.
A pesquisa revela por que um subconjunto de neurônios em parte do cérebro chamado de núcleo subtalâmico é um alvo potencial para o alívio da dor na DP, bem como outras doenças, como demência, doença dos neurônios motores e Huntington, e certas formas de enxaqueca.
As pessoas com DP frequentemente relatam dor inexplicável, como sensação de queimação, dor aguda, coceira ou formigamento que não estão diretamente relacionadas aos seus outros sintomas de DP. O tratamento com estimulação cerebral profunda no núcleo subtalâmico pode ajudar com os sintomas relacionados ao movimento da DP, mas estudos recentes mostraram que também reduz a dor. A maneira como isso acontece, no entanto, ainda não está clara.
"Neste estudo, nos propusemos a determinar se o núcleo subtalâmico está envolvido na tradução de um estímulo nocivo, como lesão em dor, e se esta transmissão de informação é alterada na DP", explica Arnaud Pautrat, PhD Student at Grenoble Institut des Neurociências (Inserm, Instituto Nacional de Saúde e Pesquisa Médica / Universidade Grenoble Alpes), França.
A equipe começou usando a eletrofisiologia para medir o disparo de sinais elétricos em células nervosas no núcleo subtalâmico de ratos que receberam um choque na pata traseira. As células nervosas foram de fato ativadas temporalmente por essa estimulação. Eles também descobriram que os neurônios caíram em três grupos de resposta, mostrando um aumento, diminuição ou nenhuma mudança na sua taxa de disparo de linha de base.
Em seguida, eles analisaram se essas respostas causaram uma mudança na função cerebral. Ratos com um núcleo subtalâmico danificado levaram muito mais tempo para mostrar sinais de desconforto do que ratos saudáveis. Quando eles expandiram seu estudo para modelos de ratos com DP, a equipe descobriu que as células nervosas no núcleo subtalâmico tinham taxas de disparo mais altas e as respostas à dor eram maiores e mais longas do que nos animais saudáveis. Em conjunto, isso sugere que as vias disfuncionais de processamento da dor no núcleo subtalâmico são a causa da dor relacionada à DP.
Para entender de onde os sinais de dor para o núcleo subtalâmico estavam vindo, a equipe analisou duas estruturas cerebrais conhecidas por serem importantes na transmissão de sinais de dano da medula espinhal: o colículo superior e o núcleo parabraquial. O bloqueio de sua atividade revelou que ambas as estruturas desempenham um papel crucial na transmissão de informações sobre a dor para o núcleo subtalâmico, e que existe uma via de comunicação direta entre o núcleo parabraquial e o núcleo subtalâmico. Como resultado, a equipe acredita que esse caminho provavelmente está envolvido nos efeitos benéficos da estimulação cerebral profunda na dor na DP e que essas novas descobertas podem ajudar a direcionar a estimulação para partes específicas do cérebro para torná-la mais eficaz como uma dor apaziguada.
"Nós encontramos evidências de que o núcleo subtalâmico está funcionalmente ligado a uma rede de processamento de dor e que essas respostas são afetadas no Parkinsonismo", conclui a autora sênior e pesquisadora do Inserm, Veronique Coizet, PhD. "Mais experimentos são necessários para caracterizar completamente os efeitos da estimulação cerebral profunda nesta região do cérebro em nossos modelos experimentais, com o objetivo de encontrar maneiras de otimizá-la como um tratamento para a dor causada por Parkinson e outras doenças neurológicas." Original em inglês, tradução Google, revisão Hugo. Fonte: Science Daily.
terça-feira, 28 de agosto de 2018
domingo, 19 de agosto de 2018
Estimulação do núcleo subtalâmico induz déficits na decodificação de expressões faciais emocionais na doença de Parkinson
Resumo
Antecedentes: A estimulação do núcleo subtalâmico bilateral (STN) é reconhecida como um tratamento para pacientes Parkinsonianos com complicações motoras graves relacionadas com a levodopa. Embora os efeitos adversos sejam infrequentes, alguns distúrbios comportamentais foram relatados.
Objetivo: Investigar as consequências da estimulação do STN no processamento de informações emocionais na doença de Parkinson, avaliando o desempenho de uma tarefa de decodificação da expressão facial emocional (EFE) em um grupo de pacientes antes e depois da cirurgia.
Métodos: 12 pacientes não-dementes com doença de Parkinson foram estudados. Eles foram avaliados um mês antes da cirurgia e três meses depois. Sua capacidade de decodificar EFEs foi avaliada usando uma tarefa quantitativa padronizada. Função cognitiva geral, função executiva, percepção visoespacial, depressão e ansiedade também foram medidas. Doze controles saudáveis foram pareados por idade, sexo e duração da educação.
Resultados: Antes da cirurgia, os pacientes não apresentaram comprometimento na decodificação EFE em comparação com os controles. Seu status cognitivo geral foi preservado, mas eles tinham uma síndrome moderada de disexecução. Três meses após a cirurgia, eles tiveram um comprometimento significativo da decodificação de EFE. Isso não estava relacionado ao seu estado cognitivo geral ou aos escores de depressão / ansiedade. Percepção visuoespacial não foi prejudicada. Não houve mudança na extensão da síndrome disexecutiva, exceto por uma redução na fluência de palavras fonêmicas.
Conclusões: A estimulação bilateral do STN perturba o processamento de informação emocional negativa na doença de Parkinson. A deficiência parece específica e não relacionada a certas variáveis secundárias. Esta complicação comportamental do STN pode ter implicações para a vida social do paciente. Original em inglês, tradução Google, revisão Hugo. Fonte: JNPP.
Antecedentes: A estimulação do núcleo subtalâmico bilateral (STN) é reconhecida como um tratamento para pacientes Parkinsonianos com complicações motoras graves relacionadas com a levodopa. Embora os efeitos adversos sejam infrequentes, alguns distúrbios comportamentais foram relatados.
Objetivo: Investigar as consequências da estimulação do STN no processamento de informações emocionais na doença de Parkinson, avaliando o desempenho de uma tarefa de decodificação da expressão facial emocional (EFE) em um grupo de pacientes antes e depois da cirurgia.
Métodos: 12 pacientes não-dementes com doença de Parkinson foram estudados. Eles foram avaliados um mês antes da cirurgia e três meses depois. Sua capacidade de decodificar EFEs foi avaliada usando uma tarefa quantitativa padronizada. Função cognitiva geral, função executiva, percepção visoespacial, depressão e ansiedade também foram medidas. Doze controles saudáveis foram pareados por idade, sexo e duração da educação.
Resultados: Antes da cirurgia, os pacientes não apresentaram comprometimento na decodificação EFE em comparação com os controles. Seu status cognitivo geral foi preservado, mas eles tinham uma síndrome moderada de disexecução. Três meses após a cirurgia, eles tiveram um comprometimento significativo da decodificação de EFE. Isso não estava relacionado ao seu estado cognitivo geral ou aos escores de depressão / ansiedade. Percepção visuoespacial não foi prejudicada. Não houve mudança na extensão da síndrome disexecutiva, exceto por uma redução na fluência de palavras fonêmicas.
Conclusões: A estimulação bilateral do STN perturba o processamento de informação emocional negativa na doença de Parkinson. A deficiência parece específica e não relacionada a certas variáveis secundárias. Esta complicação comportamental do STN pode ter implicações para a vida social do paciente. Original em inglês, tradução Google, revisão Hugo. Fonte: JNPP.
quinta-feira, 16 de agosto de 2018
Estimulação cerebral profunda de baixa frequência reduz o congelamento da marcha, mostra estudo
AUGUST 16, 2018 - A estimulação cerebral subtalâmica profunda de baixa frequência (STN-DBS), mas não a STN-DBS de alta frequência, reduz o congelamento da marcha em pacientes com Parkinson enquanto preserva sua capacidade de processar simultaneamente informações motoras e cognitivas, mostra um estudo recente.
O estudo, "Diminuir a frequência de estimulação cerebral subtalâmica profunda reverte a interferência cognitiva durante o início da marcha na doença de Parkinson", foi publicado na revista Clinical Neurosphysiology.
Muitos pacientes com Parkinson (50-70%) desenvolvem o congelamento da marcha, que ocorre quando um paciente sente temporariamente que seus pés estão colados ao chão e hesita antes de dar um passo à frente.
O congelamento da marcha ocorre principalmente quando um paciente quer começar a andar ou mudar de direção, mas também pode ocorrer em situações de dupla tarefa, como atravessar a rua ou conversar enquanto caminha. Isso muitas vezes leva a quedas e afeta a qualidade de vida dos pacientes, tornando o congelamento da marcha uma grande carga.
Evidências crescentes sugerem uma associação entre congelamento da marcha e atenção prejudicada, função executiva e controle cognitivo, apoiando o envolvimento adicional de regiões cerebrais não motoras nesse sintoma motor.
A estimulação cerebral profunda é frequentemente usada para tratar pacientes com Parkinson avançado, cujos problemas motores não melhoram com medicação.
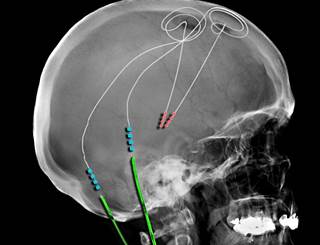
A técnica envolve a implantação cirúrgica de um eletrodo no cérebro que é conectado a um gerador de pulsos implantado através de fios subcutâneos. O gerador de pulsos é programado para fornecer impulsos elétricos controlados por carga e controlados por voltagem que estimulam o núcleo subtalâmico, uma área do cérebro envolvida na função motora e que se torna hiperativa em pacientes com Parkinson.
Vários estudos mostraram que o STN-DBS alivia os sintomas motores, reduz a dose diária necessária de medicação e melhora a qualidade de vida dos pacientes.
Enquanto alguns estudos mostraram que o STN-DBS de alta frequência alivia fortemente os sintomas motores em pacientes com Parkinson, outros sugerem que piora o congelamento da marcha e da função executiva, em comparação com STN-DBS de baixa frequência.
Pesquisadores franceses avaliaram agora os efeitos terapêuticos da frequência baixa (80 Hz) e alta (130 Hz) STN-DBS no desempenho de iniciação à marcha de pacientes com Parkinson, com ou sem a combinação de uma tarefa cognitiva.
Essa tarefa de interferência cognitiva consistiu em iniciar a caminhada de acordo com uma dica visual, que envolvia a integração de uma dica ambiental e a execução da tarefa motora.
O estudo incluiu 19 pessoas (15 homens e quatro mulheres) com doença de Parkinson avançada e uma idade média de 59 anos, e 20 pessoas saudáveis (15 homens e cinco mulheres) com uma idade média de 62 anos.
Enquanto o início da caminhada foi registrado em todos os participantes, apenas nove pacientes de Parkinson realizaram o teste de caminhada combinado com a tarefa de interferência cognitiva. Os testes foram realizados antes da cirurgia DBS, com ou sem medicações dopaminérgicas, e após a cirurgia sem medicações dopaminérgicas.
Na tarefa de iniciação simples, os pacientes com Parkinson apresentaram melhoras significativas na capacidade de andar após STN-DBS com frequência e com tratamento dopaminérgico prévio.
No entanto, quando associado à tarefa de interferência cognitiva, o tratamento com STN-DBS de alta frequência prejudicou significativamente o desempenho da caminhada dos pacientes. Essas alterações não foram observadas em pacientes tratados com STN-DBS de baixa frequência, com ou sem medicação dopaminérgica prévia, ou em pessoas saudáveis.
Esses achados sugerem que “o STN-DBS de alta frequência reduz a capacidade de processar simultaneamente informações motoras e cognitivas, enquanto isso parece preservado com STN-DBS de baixa frequência”, escreveram os pesquisadores.
Assim, os resultados suportam que o uso de STN-DBS de baixa frequência inibe o congelamento da marcha em pacientes com Parkinson.
A equipe observou que freqüências diferentes podem agir de maneira diferente nas redes cerebrais que regulam as funções motoras e cognitivas, e que estudos adicionais são necessários para esclarecer os mecanismos por trás desses diferentes efeitos. Original em inglês, tradução Google, revisão Hugo. Fonte: Parkinsons News Today.
O estudo, "Diminuir a frequência de estimulação cerebral subtalâmica profunda reverte a interferência cognitiva durante o início da marcha na doença de Parkinson", foi publicado na revista Clinical Neurosphysiology.
Muitos pacientes com Parkinson (50-70%) desenvolvem o congelamento da marcha, que ocorre quando um paciente sente temporariamente que seus pés estão colados ao chão e hesita antes de dar um passo à frente.
O congelamento da marcha ocorre principalmente quando um paciente quer começar a andar ou mudar de direção, mas também pode ocorrer em situações de dupla tarefa, como atravessar a rua ou conversar enquanto caminha. Isso muitas vezes leva a quedas e afeta a qualidade de vida dos pacientes, tornando o congelamento da marcha uma grande carga.
Evidências crescentes sugerem uma associação entre congelamento da marcha e atenção prejudicada, função executiva e controle cognitivo, apoiando o envolvimento adicional de regiões cerebrais não motoras nesse sintoma motor.
A estimulação cerebral profunda é frequentemente usada para tratar pacientes com Parkinson avançado, cujos problemas motores não melhoram com medicação.
A técnica envolve a implantação cirúrgica de um eletrodo no cérebro que é conectado a um gerador de pulsos implantado através de fios subcutâneos. O gerador de pulsos é programado para fornecer impulsos elétricos controlados por carga e controlados por voltagem que estimulam o núcleo subtalâmico, uma área do cérebro envolvida na função motora e que se torna hiperativa em pacientes com Parkinson.
Vários estudos mostraram que o STN-DBS alivia os sintomas motores, reduz a dose diária necessária de medicação e melhora a qualidade de vida dos pacientes.
Enquanto alguns estudos mostraram que o STN-DBS de alta frequência alivia fortemente os sintomas motores em pacientes com Parkinson, outros sugerem que piora o congelamento da marcha e da função executiva, em comparação com STN-DBS de baixa frequência.
Pesquisadores franceses avaliaram agora os efeitos terapêuticos da frequência baixa (80 Hz) e alta (130 Hz) STN-DBS no desempenho de iniciação à marcha de pacientes com Parkinson, com ou sem a combinação de uma tarefa cognitiva.
Essa tarefa de interferência cognitiva consistiu em iniciar a caminhada de acordo com uma dica visual, que envolvia a integração de uma dica ambiental e a execução da tarefa motora.
O estudo incluiu 19 pessoas (15 homens e quatro mulheres) com doença de Parkinson avançada e uma idade média de 59 anos, e 20 pessoas saudáveis (15 homens e cinco mulheres) com uma idade média de 62 anos.
Enquanto o início da caminhada foi registrado em todos os participantes, apenas nove pacientes de Parkinson realizaram o teste de caminhada combinado com a tarefa de interferência cognitiva. Os testes foram realizados antes da cirurgia DBS, com ou sem medicações dopaminérgicas, e após a cirurgia sem medicações dopaminérgicas.
Na tarefa de iniciação simples, os pacientes com Parkinson apresentaram melhoras significativas na capacidade de andar após STN-DBS com frequência e com tratamento dopaminérgico prévio.
No entanto, quando associado à tarefa de interferência cognitiva, o tratamento com STN-DBS de alta frequência prejudicou significativamente o desempenho da caminhada dos pacientes. Essas alterações não foram observadas em pacientes tratados com STN-DBS de baixa frequência, com ou sem medicação dopaminérgica prévia, ou em pessoas saudáveis.
Esses achados sugerem que “o STN-DBS de alta frequência reduz a capacidade de processar simultaneamente informações motoras e cognitivas, enquanto isso parece preservado com STN-DBS de baixa frequência”, escreveram os pesquisadores.
Assim, os resultados suportam que o uso de STN-DBS de baixa frequência inibe o congelamento da marcha em pacientes com Parkinson.
A equipe observou que freqüências diferentes podem agir de maneira diferente nas redes cerebrais que regulam as funções motoras e cognitivas, e que estudos adicionais são necessários para esclarecer os mecanismos por trás desses diferentes efeitos. Original em inglês, tradução Google, revisão Hugo. Fonte: Parkinsons News Today.
quarta-feira, 15 de agosto de 2018
Um Modelo para Prevenção de Melhorias na Qualidade de Vida Após Estimulação Cerebral Profunda
August 09, 2018 - Um aumento de 12,4% nas chances de melhora na qualidade de vida foi encontrado para cada 100 unidades adicionais de dose diária equivalente à levodopa prescrita no pré-operatório.
As 5 variáveis basais que podem ser usadas para prever melhorias significativas na qualidade de vida após a estimulação cerebral profunda (DBS) para pacientes com doença de Parkinson são pontuações de Parkinson Disease Questionnaire-39 (PDQ-39), bilateral vs unilateral DBS, levodopa equivalente diariamente dose, variação percentual na avaliação motora on / off e anos desde o início dos sintomas. Um modelo criado sobre essas associações previu melhorias na qualidade de vida com precisão de 81% do tempo, de acordo com um estudo publicado na Neurosurgery.
Houve 67 pacientes que foram submetidos à cirurgia de DBS para a doença de Parkinson no Cleveland Clinic Center for Neurological Restoration, Instituto de Neurologia entre 2007 e 2012 incluídos neste estudo retrospectivo, 36 dos quais experimentaram melhor qualidade de vida após a cirurgia.
Um aumento de 7,3% nas chances de melhora na qualidade de vida foi encontrado para cada aumento de 1 ponto no escore do PDQ-39 antes da cirurgia (OR, 1.073; 95% CI, 1.03–1.119; P = .001). Um aumento de 12,4% na chance de melhora na qualidade de vida foi encontrado para cada 100 unidades adicionais de dose diária equivalente à levodopa prescrita no pré-operatório (OR, 1,124; IC 95%, 1,008-1,254; P = 0,036). Um aumento de 4,5% nas chances de melhora na qualidade de vida foi encontrado para cada 1% adicional de mudança na medicação vs off nos escores Unified Parkinson Disease Rating Scale-II (OR, 1,045; 95% CI, 1,014-1,078; P = 0,005 ). Os pacientes que foram submetidos a implante DBS bilateral tiveram chances de melhorias na qualidade de vida 6 vezes maior em comparação com pacientes recebendo DBS apenas do lado direito (OR, 6,0; IC 95%, 1,331-27,047; P = 0,02). Um aumento de 11% nas chances de melhora na qualidade de vida foi encontrado para cada ano adicional desde o início dos sintomas da doença (OR, 1,11; IC 95%, 1.001-1.231; P =, 048).
"Nosso modelo pode prever com precisão se o pós-operatório [qualidade de vida] vai melhorar 81,4% do tempo", concluíram os autores do estudo. "[I] t ser possível construir um modelo de previsão mais abrangente que poderia servir como uma ferramenta prognóstica clinicamente relevante para os médicos que avaliam a candidatura do paciente para a cirurgia." Original em inglês, tradução Google, revisão Hugo. Fonte: Neurology Advisor.
As 5 variáveis basais que podem ser usadas para prever melhorias significativas na qualidade de vida após a estimulação cerebral profunda (DBS) para pacientes com doença de Parkinson são pontuações de Parkinson Disease Questionnaire-39 (PDQ-39), bilateral vs unilateral DBS, levodopa equivalente diariamente dose, variação percentual na avaliação motora on / off e anos desde o início dos sintomas. Um modelo criado sobre essas associações previu melhorias na qualidade de vida com precisão de 81% do tempo, de acordo com um estudo publicado na Neurosurgery.
Houve 67 pacientes que foram submetidos à cirurgia de DBS para a doença de Parkinson no Cleveland Clinic Center for Neurological Restoration, Instituto de Neurologia entre 2007 e 2012 incluídos neste estudo retrospectivo, 36 dos quais experimentaram melhor qualidade de vida após a cirurgia.
Um aumento de 7,3% nas chances de melhora na qualidade de vida foi encontrado para cada aumento de 1 ponto no escore do PDQ-39 antes da cirurgia (OR, 1.073; 95% CI, 1.03–1.119; P = .001). Um aumento de 12,4% na chance de melhora na qualidade de vida foi encontrado para cada 100 unidades adicionais de dose diária equivalente à levodopa prescrita no pré-operatório (OR, 1,124; IC 95%, 1,008-1,254; P = 0,036). Um aumento de 4,5% nas chances de melhora na qualidade de vida foi encontrado para cada 1% adicional de mudança na medicação vs off nos escores Unified Parkinson Disease Rating Scale-II (OR, 1,045; 95% CI, 1,014-1,078; P = 0,005 ). Os pacientes que foram submetidos a implante DBS bilateral tiveram chances de melhorias na qualidade de vida 6 vezes maior em comparação com pacientes recebendo DBS apenas do lado direito (OR, 6,0; IC 95%, 1,331-27,047; P = 0,02). Um aumento de 11% nas chances de melhora na qualidade de vida foi encontrado para cada ano adicional desde o início dos sintomas da doença (OR, 1,11; IC 95%, 1.001-1.231; P =, 048).
"Nosso modelo pode prever com precisão se o pós-operatório [qualidade de vida] vai melhorar 81,4% do tempo", concluíram os autores do estudo. "[I] t ser possível construir um modelo de previsão mais abrangente que poderia servir como uma ferramenta prognóstica clinicamente relevante para os médicos que avaliam a candidatura do paciente para a cirurgia." Original em inglês, tradução Google, revisão Hugo. Fonte: Neurology Advisor.
segunda-feira, 13 de agosto de 2018
Pânico
Terça feira passada
(31/07) estava carregando a bateria do meu marcapasso Activa RC e a
carga, que estava a 75%, foi bruscamente interrrompida. Faltou carga
na bateria do carregador. O display ficou apagado e o aparelho
(bateria intermediária) começou a emitir bips a cada 1 segundo. De
pronto conectei o carregador na tomada para tentar recarregá-lo e ele não
reagiu, mantendo os mesmos sintomas: display apagado e emitindo
bips.
Bateu um pânico,
pois apesar de estar com a bateria do marcapasso a 75% e tendo
autonomia para aproximadamente uma semana, fiquei preocupado ante a
pane do carregador, pois caso demorasse um tempo longo para reparo,
corria o risco de ficar sem bateria, pois teria que desligar antes de
esgotar a mesma, o protocolo recomendado, com os sintomas voltando.
Imediatamente,
seguindo orientações do manual do paciente, procurei meu médico,
que via “zap-zap” prontamente me orientou a procurar o representante da
Medtronic. Marcamos horário no consultório médico na quinta-feira
(02/08) e em 10 minutos, após uma observação do estado do
carrregador, foi procedido uma espécie de “reset” no mesmo e este voltou ao
funcionamento normal. Aprendi a lição: não negligenciar a carga da
bateria do carregador e manter o monitoramento da carga do marcapasso
em si.
E diga-se, viva por
morar em Porto Alegre, já que não precisei muito deslocamento e
demorado para manutenção do equipamento, com pronta resposta da
representante da Medtronic, Proger.
Acima a foto do
carregador (lado direito), que é dotado de um plug (setinha branca em cima à esquerda)
para inserção do conversor de energia que é ligado na tomada
elétrica residencial e da antena (esquerda) que, bem disposta sobre
o implante, localiza e identifica o marcapasso dentro do corpo e passa a fornecer a carga,
cuja eficiência é medida pela sucessão de segmentos quadradinhos (no caso mostrado com eficiência máxima).
sexta-feira, 3 de agosto de 2018
Abbott atualiza software de implante cerebral
A Food and Drug Administration dos EUA aprovou uma atualização de software pelo ar (wireless) para os implantes Infinity fabricados pela Abbott, fornecendo dispositivos usados em Parkinson e tremor essencial para a compatibilidade de RMI de corpo inteiro e um avanço na funcionalidade.
August 3, 2018 - A mudança de vida, a tecnologia de estimulação cerebral profunda (DBS) receberá a atualização do software sem fio usando conexão Bluetooth segura, sem necessidade de cirurgia.
A atualização será transmitida para todos os sistemas Infinity DBS implantados atualmente, adicionando rotulagem condicional MRI de corpo inteiro junto com um conjunto de atualizações de sistema.
Antes da aprovação mais recente da Abbott, as pessoas que são novas na terapia de estimulação cerebral profunda ou aquelas que vivem com sistemas mais antigos podem ter experimentado barreiras no acesso às opções de terapia DBS mais avançadas devido à necessidade potencial de uma ressonância magnética no futuro.
Com a sua rotulagem atualizada, a Abbott resolveu este desafio com a plataforma de terapia aprimorada do sistema Infinity DBS - a primeira e única tecnologia de estimulação cerebral profunda condicional MR aprovada pela FDA.
Binith Cheeran, diretor médico de distúrbios do movimento da Abbott, disse: “Com essa atualização de software, a Abbott promete desenvolver recursos poderosos que fortalecem a plataforma centrada no paciente da Infinity DBS, que usa a tecnologia familiar da Apple e libera o paciente recarregando seu dispositivo.”
"Estamos comprometidos com a inovação contínua em neuromodulação, desenvolvendo avanços contínuos e eficiências para os médicos e, mais importante, ajudando milhares de pessoas que estão lutando contra distúrbios do movimento a viver uma vida mais plena".
Agora, os médicos poderão simplificar o processo de programação de dispositivos com um dispositivo tablet usando o novo software de programação Informy da Abbott, permitindo que eles se tornem mais eficientes em sua prática e obtenham resultados ideais com eletrodos direcionais. Além disso, os pacientes podem gerenciar discretamente seus sintomas com o controlador de estilo tablet Infinity DBS System.
O sistema Infinity da Abbott é o primeiro e único sistema de estimulação cerebral profunda do mundo operando em uma plataforma de software separada com tecnologia sem fio Bluetooth e é usado atualmente por milhares de pacientes em 30 países ao redor do mundo. Original em inglês, tradução Google, revisão Hugo. Fonte: Pharma Phorum.
sexta-feira, 27 de julho de 2018
Indicação para a cirurgia de Estimulação Cerebral Profunda (DBS)
Não conheço tampouco tenho referências deste médico, no entanto considero bem coerentes suas orientações.
Dr. Rubens Cury explica, de forma geral, quais as características do paciente com Parkinson mais indicado para o implante de um Estimulador Cerebral Profundo (DBS) e apresenta quando a cirurgia pode ser uma opção de terapia. Cada caso é um caso, por isso Dr. Rubens reforça que é fundamental consultar um especialista para fazer uma avaliação adequada.
Assinar:
Postagens (Atom)