May 24, 2016 - Qual opção você escolherá quando for a hora de selecionar uma bateria recarregável ou não recarregável?
Nota para o leitor: Tenha em mente que este artigo foi escrito em 2016. As baterias DBS estão mudando e duram mais do que quando o artigo foi escrito há apenas alguns anos!
A tomada de decisões não é fácil, especialmente quando sua saúde está em jogo. Depois que você decide ter uma estimulação cerebral profunda, você escolhe se deseja fazer uma cirurgia unilateral ou bilateral, seguida por uma opção de tipo de bateria. Suas opções são uma bateria recarregável ou não recarregável.
Com uma bateria não recarregável, você vive livre de tremores até que a bateria acabe. Você fará uma cirurgia para substituir a bateria aproximadamente a cada 3-5 anos, mas algumas pessoas precisarão substituí-la em muito menos tempo. Como Cinderela em seu vestido e sapatos de vidro, você deve estar ciente de que sua bateria não-recarregável tem um prazo para a substituição. Com a mesma autoridade que a Fada Madrinha, as configurações do neuroestimulador determinam a rapidez com que descarregam a bateria.
Uma bateria recarregável durará 9 anos, mas você deve carregá-la praticamente diariamente. (N.T.: Provavelmente isto ocorra mais para o fim da vida útil da bateria) (*)
Não há resposta certa. Um caso pode ser feito para qualquer decisão. Em última análise, você deve fazer a escolha sozinho.
Diferença de Custos entre Baterias Recarregáveis e Não Recarregáveis
Por uma questão de interesse, uma bateria recarregável é uma bateria mais cara, enquanto uma bateria não recarregável é menos dispendiosa. A diferença de preço varia muito dependendo do hospital. Isto é baseado em contratos hospitalares nacionais ou regionais, volume hospitalar, pedidos em massa, etc. Além disso, isso não é necessariamente o preço que os pacientes verão em sua fatura, já que os hospitais e as seguradoras tendem a ter sua marca também. Um canal duplo recarregável custa cerca de três vezes mais do que um canal único não recarregável, e um canal duplo não recarregável de célula primária está em algum lugar no meio dessas duas figuras.
Opções da área da baía (Califórnia)
Na área da baía, a Kaiser Permanente (N.T.: Plano de Saúde) oferece uma opção entre baterias recarregáveis e não recarregáveis. Minha especialista em distúrbios do movimento, Dra. Rima Ash, disse: “As pessoas geralmente não escolhem recarregáveis devido à provação de carga, mas, para a maioria, é uma atividade simples que leva de 20 a 30 minutos, se feita diariamente. A Medtronic saiu agora com melhores maneiras de carregar sem ter que usar o cinto de recarga”.
Dra. Helen Bronte-Stewart. MD, MSE, FANN, FANA, diretor do Stanford Comprehensive Movement Disorders Center, disse: “Meus pacientes com o recarregável estão indo bem com ele e carregam todas as noites / dias(*). A maioria deles tem distonia, que é onde nós a usamos com mais frequência, pois eles exigem substituições de IPG com mais frequência”.
Se você pesquisar on-line, você verá que a UCSF não recomenda recarregável, a menos que você esteja usando seu sistema existente em menos de dois anos após a implantação. "Esta não é uma regra difícil e rápida na UCSF", disse Monica Volz, enfermeira do Centro de Distúrbios do Movimento e Neuromodulação da UCSF. “Nós temos alguns pacientes que têm alguns sinais de demência ou outras condições mentais, onde mesmo se eles estivessem passando pela bateria em menos de dois anos, a UCSF recomendaria substituições não-recarregáveis. Isso realmente só depende. Os prós e contras são discutidos com todos os pacientes antes da substituição”.
Profundidade do Implante
Às vezes, os implantadores colocam um não-recarregável um pouco mais profundo por causa da anatomia do paciente, mas, se um paciente muda para um recarregável, ele pode ser muito profundo para obter um excelente acoplamento. Isso seria uma complicação que exigiria uma revisão da bolsa e profundidade. Isso geralmente seria feito no momento da substituição, mas algo a considerar para alguns pacientes.
Diferença na facilidade de usar
O Dr. Eric Sabelman, Bioengenheiro Sênior em Neurocirurgia Funcional da Kaiser Permanente-Redwood City, aponta: com baterias recarregáveis, os pacientes com DBS podem ter dificuldade em posicionar a bobina de recarga, o que pode ser difícil para uma pessoa com função de braço e mão prejudicada.
Há um "ponto ideal" que alguns usuários têm dificuldade em localizar para que a carga seja bem-sucedida.
Alguns pacientes escolhem não recarregáveis porque não querem lidar com a carga.
Você pode se sentir atraído por uma bateria não recarregável, porque sua vida familiar e seu estilo de vida colocam tanta tensão em você que você não pode tolerar outra tarefa diária(*).
Se você estiver viajando no exterior, deve levar consigo um adaptador para recarregar. "Certifique-se de recarregar de forma conservadora no início, quando viajar", sugere o médico assistente Ivan Bernstein na Kaiser-Permanente Redwood City.
Diferença no Número de Visitas Hospitalares
Alguns médicos preferem recarregável porque reduz o número de cirurgias que você terá com a vida mais curta bateria não-recarregável.
Desenvolvimentos tecnológicos
Um benefício colateral da bateria não recarregável é que ela garante que, a cada 3 a 5 anos, você receberá uma reavaliação abrangente e uma reavaliação da correspondência de tecnologia. Quem sabe que tipo de equipamento eles vão usar amanhã? Original em inglês, tradução Google, revisão Hugo. Fonte: Parkinsons Women.
(*) Eu uso bateria recarregável Medtronic (Activa RC). Normalmente faço a recarga quando a monitoro e a mesma está marcando Low Battery ou quando acima disso, necessitar ficar um tempo longe de ter condições de recarga (viagens, etc...). A prática de carregá-la quando estiver abaixo de 25% de carga ou Low Bat, provavelmente prolongue a vida útil, diminuindo o efeito memória, já que quando a carga é dada até full, demanda cerca de 4 horas e tenho feito a recarga atualmente a cada 12 dias em média.
Já fiz uso de baterias descartáveis Kinetra bi-lateral da Medtronic. Quando a mesma termina é um sofrimento, pois meu plano de saúde impõe que ela esteja esgotada para a partir daí começar o processo de troca, que envolve pedidos, idas e vindas, e muita burocracia, e tu ficas nas mãos deles, e sofrendo. É muito desgaste, inclusive emocional.
No meu entendimento são muitas as vantagens da bateria recarregável, inclusive na margem de manobra dos parâmetros de estimulação, que certamente propicia maiores limiares, sem esgotar a bateria, já que com a descartável essa margem de manobra seria necessariamente mais comedida.
Objetivo: atualização nos dispositivos de “Deep Brain Stimulation” aplicáveis ao parkinson. Abordamos critérios de elegibilidade (devo ou não devo fazer? qual a época adequada?) e inovações como DBS adaptativo (aDBS). Atenção: a partir de maio/20 fui impedido arbitrariamente de compartilhar postagens com o facebook. Com isto este presente blog substituirá o doencadeparkinson PONTO blogspot.com, abrangendo a doença de forma geral.
quinta-feira, 2 de maio de 2019
Critérios de elegibilidade para o DBS
A Estimulação Cerebral Profunda (DBS) tem o potencial de aumentar sua qualidade de vida de maneira significativa; no entanto, esse não é o tratamento certo para todos.
A Fundação Davis Phinney realizou um webinar sobre DBS e publicou uma página com informações úteis para aqueles que consideram o procedimento:
O QUE, QUANDO, PORQUÊ E FORMA DE ESTIMULAÇÃO PROFUNDA DO CÉREBRO COM A DRA. KARA BEASLEY.
Recentemente, realizamos um webinar sobre DBS quando falamos sobre o que é, quando fazer, como funciona e como pode ajudá-lo a conviver bem com o Parkinson.
Para ter acesso à gravação do webinar, clique AQUI.
Fonte: Davis Phinney Foundation. Atenção: Trata-se de evento patrocinado pela Boston Scientific, que produz neuroestimuladores, portanto interesses comerciais.
domingo, 21 de abril de 2019
Estimulação Cerebral Profunda (DBS)
Apr 15, 2019 - Estimulação Cerebral Profunda (DBS) é uma melhoria incrível na qualidade de vida das pessoas com tremor de Parkinson dominante. Este videoclipe da televisão irlandesa, onde alguém que fez uma cirurgia DBS desliga o estimulador e depois liga de novo, é um ótimo exemplo de como esse tratamento pode ser significativo:
https://www.joe.ie/fitness-health/watch-irish-parkinsons-patient-demonstrates-dramatic-effects-deep-brain-stimulation-665649 Fonte: ParkinsonFit.
E isto abaixo, comigo, quando ainda usava um Kinetra descartável e que era ligado/desligado por um magneto.
E isto abaixo, comigo, quando ainda usava um Kinetra descartável e que era ligado/desligado por um magneto.
quarta-feira, 17 de abril de 2019
Globus Pallidus Pars Interna pode ser alvo preferencial do DBS na Doença de Parkinson
 |
| Ao considerar os resultados cognitivos, o globus pallidus pars interna pode ser um alvo preferido para a estimulação cerebral profunda em pacientes com doença de Parkinson. |
O estudo incluiu dois grupos de pacientes com doença de Parkinson - 12 que foram submetidos à DBS GPi bilateral e 17 que foram submetidos ao núcleo subtalâmico bilateral (STN) DBS - no Centro DBS da Mayo Clinic em Scottsdale, Arizona, entre 2002 e 2015.
No início do estudo e 6 meses após o DBS, os pesquisadores avaliaram as diferenças nos escores dos testes neuropsicológicos nos testes Boston Naming Test e Wechsler Adult Intelligence Scale Verbal Comprehension, Working Memory e Processing Speed Indexes.
Não houve diferenças significativas entre os escores de referência e de acompanhamento em qualquer um dos testes neuropsicológicos entre os pacientes do grupo GPi GPi. Pacientes no grupo STN DBS tiveram significativamente piores índices de velocidade de processamento no acompanhamento em comparação com o valor basal (média [desvio padrão (SD)], 91,47 [10,42] vs 81,65 [12,03], P = 0,03).
Quando os pesquisadores compararam os dois grupos, eles encontraram uma diferença significativa entre os escores de referência e de acompanhamento no Wechsler Adult Intelligence Scale Verbal Comprehension Index. Os pacientes do grupo STN DBS tiveram menor pontuação (delta médio, -3,41 [DP = 5,91]), enquanto os pacientes do GPi GPi tiveram maior pontuação (média delta, 4,83 [DP = 10,15]; p = 0,008) no início do estudo vs. acima.
Apesar do pequeno tamanho da amostra deste estudo, os pesquisadores afirmaram: “Nossas descobertas se somam ao crescente corpo de evidências mostrando que o alvo preferido para DBS em pacientes com doença de Parkinson pode ser GPi ao invés de STN, pois esta abordagem pode ser mais provável de minimizar potenciais negativos. efeitos sobre a cognição”. Original em inglês, tradução Google, revisão Hugo. Fonte: Psychiatry Advisor.
quinta-feira, 11 de abril de 2019
Quando é hora de pensar em cirurgia para tratar o Parkinson
Por Chloé Pinheiro
11 abr 2019 - O 11 de abril marca o Dia Mundial de Conscientização do Parkinson, doença neurodegenerativa que afeta 1% dos idosos do mundo, cerca de 200 mil deles no Brasil. Apesar de mais conhecida pelos tremores e enrijecimento muscular, ela também prejudica o sistema urinário, intestino, olfato e pode provocar depressão e dores articulares.
Não há cura para a condição, caracterizada pela queda brusca e intensa na concentração de dopamina, um neurotransmissor envolvido no controle dos movimentos. Os remédios mais utilizados no tratamento repõem essa substância, mas podem deixar de funcionar depois de um tempo.
“A partir do quinto ano de diagnóstico, um quarto dos indivíduos terá flutuação motora relacionada ao medicamento”, explica Murilo Martinez Marinho, coordenador de neurocirurgia funcional no Hospital São Paulo, da Universidade Federal de São Paulo (Unifesp). Nessa situação, os movimentos involuntários pioram quando o efeito do comprimido passa, algumas horas após a aplicação.
Mesmo com o ajuste de doses, os sintomas às vezes continuam atrapalhando a vida. O efeito benéfico dos fármacos, por sua vez, fica cada vez mais curto – em certos episódios, ele não passa de uns poucos minutos livres de tremores.
Para esses casos mais severos, há alternativas como a estimulação cerebral profunda (ECP). Trata-se de uma cirurgia que insere uma espécie de marca-passo em uma região do cérebro. Isso para reduzir as alterações motoras e até o consumo de fármacos.
Quem pode fazer a estimulação cerebral profunda
Além das pessoas com flutuação motora, aquelas com mais de quatro anos de doença, cujos sintomas deixaram de responder aos remédios mesmo após o aumento da dose. “Até quem foi diagnosticado recentemente, mas tem tremores incapacitantes e refratários ao tratamento convencional, beneficia-se da neuroestimulação”, comenta Marinho.
Há ainda um último grupo, mais raro, que teria indicação para essa técnica. São os sujeitos que têm intolerância gastrointestinal ao uso da medicação ou que sofrem demais com seus efeitos colaterais (náuseas e sonolência, entre outros).
A neuroestimulação está incluída no rol de procedimentos a serem cobertos pelos planos de saúde e é realizada em alguns centros de referência do Sistema Único de Saúde (SUS).
Como funciona o marca-passo e a cirurgia
O dispositivo envia sinais elétricos constantes e pode ser colocado em três núcleos diferentes do cérebro que estão envolvidos com o Parkinson. A escolha pelo local da instalação na massa cinzenta é baseada nos sintomas de cada pessoa. Geralmente, a área estimulada é o núcleo subtalâmico, o mais associado às alterações motoras.
A cirurgia se divide em duas partes. Na primeira, um gerador é inserido na área da clavícula. Na segunda etapa, esse equipamento é conectado a dois eletrodos, que são colocados pela parte frontal da cabeça. “As incisões ali são pequenas, menores que uma moeda de dez centavos”, aponta Martinho.
O indivíduo fica acordado durante esse processo para que, uma vez que os eletrodos estejam no lugar, os médicos avaliem ao vivo e a cores a fala, a coordenação motora e os tremores.
Se for necessário, há ajuste no posicionamento dos dispositivos. Com tudo certo, uma anestesia geral é aplicada para finalizar a instalação. Alguns dispositivos recarregáveis chegam a durar 15 anos antes que uma troca seja mandatória.
Vantagens da abordagem cirúrgica
Essa terapia tem evoluído desde os anos 1980, quando começou a ser utilizada para tratar a doença de Parkinson. Um estudo publicado em 2012 no Journal of American Medicine (JAMA), feito com veteranos do exército americano, mostrou que o método proporciona, em média, até quatro horas a mais sem tremores por dia.
“Outros trabalhos demonstram melhora em sintomas não motores, como sono, dores e fadiga”, destaca Marinho. Um trabalho alemão, de 2013, comparou 251 pacientes e observou uma melhora de 26% na qualidade de vida de quem passou pela ECP. O grupo que ficou apenas no tratamento medicamentoso viu esse índice piorar em 1%, segundo os dados do estudo, conduzido pela Universidade de Kiel e extraído de um compêndio da empresa Medtronic, que produz um desses marca-passos.
Agora, não estamos falando de uma cura definitiva. “Problemas no equilíbrio e dificuldades na fala podem aparecer, mas não se trata de um efeito colateral da cirurgia, e sim uma progressão natural da doença”, aponta Marinho.
Outros tratamentos para Parkinson
Além da estimulação elétrica, novas opções de terapias chegaram nos últimos anos, como as bombas de infusão que liberam remédios direto no aparelho digestivo do paciente ou as infusões subcutâneas com o mesmo papel. E o futuro com certeza reserva mais progressos.
Entre as linhas de pesquisa, há neuroestimuladores modernos, capazes de monitorar a atividade cerebral e fornecer dados que ajudem a escolher o melhor tratamento. Remédios à base de canabidiol, um dos princípios ativos da maconha, também demonstraram aliviar os sintomas diários em estudos.
Há até outras abordagens mais ousadas. Em novembro de 2018, experts japoneses anunciaram um transplante de células-tronco em um portador de Parkinson para estimular a produção natural de dopamina – aquele neurotransmissor que fica em falta na doença, se lembra?
O homem será acompanhado por dois anos para verificar se houve alguma melhora. Enquanto isso, a ciência trabalha. “O Parkinson é prevalente e os números tendem a aumentar com o envelhecimento da população. Até por isso há inúmeros estudos para combatê-la”, encerra Marinho. Fonte: Saude Abril.
Casos que progridem rapidamente ou não respondem aos remédios podem ser amenizados com um marca-passo cerebral. Saiba mais no Dia Mundial do Parkinson
Não há cura para a condição, caracterizada pela queda brusca e intensa na concentração de dopamina, um neurotransmissor envolvido no controle dos movimentos. Os remédios mais utilizados no tratamento repõem essa substância, mas podem deixar de funcionar depois de um tempo.
“A partir do quinto ano de diagnóstico, um quarto dos indivíduos terá flutuação motora relacionada ao medicamento”, explica Murilo Martinez Marinho, coordenador de neurocirurgia funcional no Hospital São Paulo, da Universidade Federal de São Paulo (Unifesp). Nessa situação, os movimentos involuntários pioram quando o efeito do comprimido passa, algumas horas após a aplicação.
Mesmo com o ajuste de doses, os sintomas às vezes continuam atrapalhando a vida. O efeito benéfico dos fármacos, por sua vez, fica cada vez mais curto – em certos episódios, ele não passa de uns poucos minutos livres de tremores.
Para esses casos mais severos, há alternativas como a estimulação cerebral profunda (ECP). Trata-se de uma cirurgia que insere uma espécie de marca-passo em uma região do cérebro. Isso para reduzir as alterações motoras e até o consumo de fármacos.
Quem pode fazer a estimulação cerebral profunda
Além das pessoas com flutuação motora, aquelas com mais de quatro anos de doença, cujos sintomas deixaram de responder aos remédios mesmo após o aumento da dose. “Até quem foi diagnosticado recentemente, mas tem tremores incapacitantes e refratários ao tratamento convencional, beneficia-se da neuroestimulação”, comenta Marinho.
Há ainda um último grupo, mais raro, que teria indicação para essa técnica. São os sujeitos que têm intolerância gastrointestinal ao uso da medicação ou que sofrem demais com seus efeitos colaterais (náuseas e sonolência, entre outros).
A neuroestimulação está incluída no rol de procedimentos a serem cobertos pelos planos de saúde e é realizada em alguns centros de referência do Sistema Único de Saúde (SUS).
Como funciona o marca-passo e a cirurgia
O dispositivo envia sinais elétricos constantes e pode ser colocado em três núcleos diferentes do cérebro que estão envolvidos com o Parkinson. A escolha pelo local da instalação na massa cinzenta é baseada nos sintomas de cada pessoa. Geralmente, a área estimulada é o núcleo subtalâmico, o mais associado às alterações motoras.
A cirurgia se divide em duas partes. Na primeira, um gerador é inserido na área da clavícula. Na segunda etapa, esse equipamento é conectado a dois eletrodos, que são colocados pela parte frontal da cabeça. “As incisões ali são pequenas, menores que uma moeda de dez centavos”, aponta Martinho.
O indivíduo fica acordado durante esse processo para que, uma vez que os eletrodos estejam no lugar, os médicos avaliem ao vivo e a cores a fala, a coordenação motora e os tremores.
Se for necessário, há ajuste no posicionamento dos dispositivos. Com tudo certo, uma anestesia geral é aplicada para finalizar a instalação. Alguns dispositivos recarregáveis chegam a durar 15 anos antes que uma troca seja mandatória.
Vantagens da abordagem cirúrgica
Essa terapia tem evoluído desde os anos 1980, quando começou a ser utilizada para tratar a doença de Parkinson. Um estudo publicado em 2012 no Journal of American Medicine (JAMA), feito com veteranos do exército americano, mostrou que o método proporciona, em média, até quatro horas a mais sem tremores por dia.
“Outros trabalhos demonstram melhora em sintomas não motores, como sono, dores e fadiga”, destaca Marinho. Um trabalho alemão, de 2013, comparou 251 pacientes e observou uma melhora de 26% na qualidade de vida de quem passou pela ECP. O grupo que ficou apenas no tratamento medicamentoso viu esse índice piorar em 1%, segundo os dados do estudo, conduzido pela Universidade de Kiel e extraído de um compêndio da empresa Medtronic, que produz um desses marca-passos.
Agora, não estamos falando de uma cura definitiva. “Problemas no equilíbrio e dificuldades na fala podem aparecer, mas não se trata de um efeito colateral da cirurgia, e sim uma progressão natural da doença”, aponta Marinho.
Outros tratamentos para Parkinson
Além da estimulação elétrica, novas opções de terapias chegaram nos últimos anos, como as bombas de infusão que liberam remédios direto no aparelho digestivo do paciente ou as infusões subcutâneas com o mesmo papel. E o futuro com certeza reserva mais progressos.
Entre as linhas de pesquisa, há neuroestimuladores modernos, capazes de monitorar a atividade cerebral e fornecer dados que ajudem a escolher o melhor tratamento. Remédios à base de canabidiol, um dos princípios ativos da maconha, também demonstraram aliviar os sintomas diários em estudos.
Há até outras abordagens mais ousadas. Em novembro de 2018, experts japoneses anunciaram um transplante de células-tronco em um portador de Parkinson para estimular a produção natural de dopamina – aquele neurotransmissor que fica em falta na doença, se lembra?
O homem será acompanhado por dois anos para verificar se houve alguma melhora. Enquanto isso, a ciência trabalha. “O Parkinson é prevalente e os números tendem a aumentar com o envelhecimento da população. Até por isso há inúmeros estudos para combatê-la”, encerra Marinho. Fonte: Saude Abril.
Atenção: o dbs não é tão eficiente para casos de parkinson hereditário.
sexta-feira, 5 de abril de 2019
Estimulação Cerebral Profunda: É eletrizante
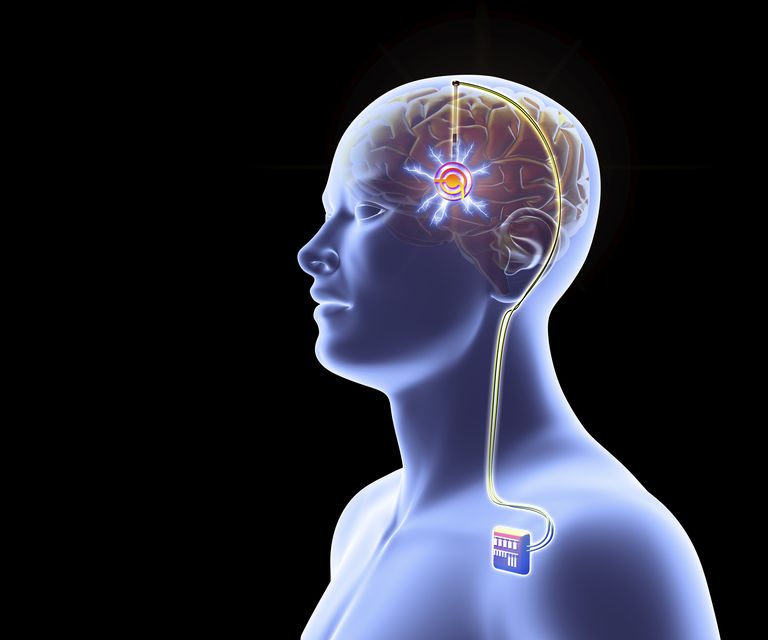 |
| ALFRED PASIEKA/SCIENCE PHOTO LIBRARY / Getty Images |
April 5, 2019 - E se você pudesse entrar em um consultório médico e dissesse: "Quero ser menos introvertido" ou "Quero ser mais corajoso" e planejar uma cirurgia para realizar esse desejo? Você faria isso? E mais importante, você deve fazer isso? Embora a tecnologia ainda não esteja nesse ponto, a estimulação cerebral profunda poderia um dia ser usada para adaptar de maneira seletiva as mudanças na personalidade de uma pessoa.
A estimulação cerebral profunda (DBS) é mais comumente usada como tratamento para pacientes com distúrbios graves do movimento, como a doença de Parkinson, para os quais a medicação não é uma opção viável. O sistema envolve colocar cirurgicamente um neuroestimulador no peito para fornecer sinais elétricos de rotina a eletrodos implantados no cérebro. O objetivo dessa corrente elétrica de criação de ritmo é anular as vias de sinalização defeituosas, especificamente aquelas que causam tremores, rigidez e outras anormalidades de movimento em pacientes com Parkinson.
O sucesso do DBS em pacientes com Parkinson levou a pesquisas mais recentes sobre o uso desta terapia para doenças psiquiátricas, como depressão e síndrome de Tourette, e foi sancionada em casos de transtorno obsessivo-compulsivo (TOC) resistente ao tratamento. No entanto, médicos e cientistas permanecem inconscientes dos mecanismos exatos pelos quais esses sinais elétricos remitem os sintomas observados. No caso da doença de Parkinson, para a qual o DBS foi aprovado, os médicos sabem onde implantar o dispositivo e ver um alívio claro dos sintomas. Este não é o caso da depressão, cuja base neurológica ainda é um mistério. Entendimento insuficiente dos estados de DBS e doença mental é, portanto, uma barreira considerável à autorização do procedimento para tais doenças mentais. Portanto, os cientistas ainda não podem confirmar a DBS como um tratamento concreto para a depressão, apesar das melhorias na depressão de alguns pacientes do estudo após o implante cirúrgico desses dispositivos.
Um fator adicional a ser cauteloso é a possibilidade de efeitos colaterais não intencionais deste procedimento. Há muito sobre o funcionamento do cérebro que permanece desconhecido, como exemplificado pela falta de conhecimento completo sobre o DBS. Consequentemente, a aplicação de um sinal elétrico ao cérebro com a intenção de produzir um objetivo poderia facilmente induzir outro resultado não intencional. A DBS poderia causar o resultado desejado de curar a depressão, mas ao mesmo tempo acidentalmente trocar a tendência de introversão com a extroversão ou até mesmo mudar algo aparentemente não relacionado à preferência musical. A interconectividade e a complexidade das vias elétricas no cérebro também abrem a possibilidade de sintomas mais prejudiciais ou indesejados, incluindo agressividade, mania e mudanças totais de personalidade. Portanto, é importante que a pesquisa científica continue no campo da DBS, para que seus trabalhos exatos possam ser compreendidos e controlados.
Uma vez que estimular eletricamente o cérebro pode criar efeitos tão profundos sobre o caráter e a personalidade, determinar quais regiões produzem esse efeito que poderia levar à viabilidade da auto-modificação deliberada, como mencionado anteriormente. Os pacientes poderiam pagar do próprio bolso pelo DBS “cosmético” para solicitar alterações, como melhor memória ou remoção de timidez. No entanto, dar às pessoas essa opção não seria sensato.
Nossas personalidades, falhas e tudo mais, são o que nos tornam humanos. Nós não somos robôs controlados pelos computadores em nossas cabeças, mas sim seres cognoscentes e pensantes com o poder de escolher nossas próprias ações. Em pessoas com depressão ou Parkinson, seus cérebros estão ativamente trabalhando contra eles, tirando suas habilidades de escolher a felicidade ou controlar seus movimentos. Para essas pessoas, a DBS poderia muito bem ser um tratamento plausível para recuperar o controle de suas vidas. No entanto, remediar doenças deve ser o alcance dessa tecnologia. O conhecimento sobre o cérebro e a capacidade de mudar sua fiação deve ser usado para retornar a autonomia humana, não para eliminar artificialmente falhas ou traços indesejáveis de personalidade. Original em inglês, tradução Google, revisão Hugo. Fonte: Dailycampus.
sábado, 30 de março de 2019
Novos dados mostram os benefícios terapêuticos dos eletrodos direcionais para uso com o sistema Infinity DBS da Abbott para tratamento da doença de Parkinson
29th March 2019 - New data show the therapeutic benefits of directional leads for use with Abbott’s Infinity DBS system for treatment of Parkinson’s disease.
Matéria "veladamente" publicitária.
terça-feira, 19 de março de 2019
Pacientes de Parkinson com má qualidade de vida podem se beneficiar ao máximo da estimulação cerebral profunda, segundo estudo
MARCH 19, 2019 - Indivíduos com a doença de Parkinson que têm má qualidade de vida devido a suas deficiências relacionadas à doença podem se beneficiar mais do tratamento com estimulação cerebral profunda.
O estudo com essa descoberta, "Qualidade de vida prediz resultado de estimulação cerebral profunda na doença de Parkinson precoce", foi publicado pela revista Neurology.
A estimulação cerebral profunda (DBS) é uma técnica cirúrgica invasiva na qual fios finos são implantados no cérebro para fornecer pulsos elétricos a áreas específicas, como o núcleo subtalâmico (STN), para aliviar os sintomas motores em pacientes para os quais os medicamentos padrão não são eficazes.
Estudos demonstraram que o DBS pode efetivamente ajudar a controlar os sintomas motores e reduzir a dose diária necessária de medicação, melhorando a qualidade de vida daqueles com Parkinson avançado ou em estágio inicial.
Em um estudo clínico anterior da Fase 4 (NCT00354133) chamado EARLYSTIM, os pesquisadores avaliaram o impacto de longo prazo do STN-DBS como um complemento ao melhor tratamento médico em relação à qualidade de vida em pacientes com doença de Parkinson por um período de mais de dois anos.
O estudo incluiu pacientes com menos de 61 anos que tiveram uma boa resposta à terapia com levodopa, mas que ainda desenvolveram complicações motoras. Entre os participantes, 124 foram tratados com DBS-STN e melhor tratamento médico, enquanto 127 pacientes receberam apenas o melhor tratamento médico.
No estudo mais recente, os pesquisadores revisaram os dados do estudo para entender quais fatores contribuíram para as mudanças detectáveis na qualidade de vida específica da doença, medida pelo índice de 39 itens do questionário Parkinson’s Disease Questionnaire (PDQ-39-SI). O questionário auto-relatado avalia a saúde específica de Parkinson em oito dimensões de qualidade de vida.
A análise revelou que a qualidade de vida ao longo dos dois anos de acompanhamento se correlacionou com o valor inicial do PDQ-39-SI em ambos os grupos de tratamento. Ainda assim, essa associação foi mais pronunciada entre os pacientes que foram tratados com STN-DBS.
Pacientes com comprometimento muito leve devido a Parkinson, correspondendo a valores de PDQ-39-SI menores que 15, não foram beneficiados com STN-DBS em comparação com pacientes tratados apenas com tratamento padrão. Em contraste, os pacientes tratados com STN-DBS que apresentavam feridas PDQ-39-SI superiores a 15 (pior qualidade de vida) no início do estudo apresentaram melhores mudanças na qualidade de vida.
“Em pacientes com avaliações de linha de base muito baixas no PDQ-39-SI, a progressão natural do comprometimento da [qualidade de vida] pode superar a melhora alcançada pelo STN-DBS”, escreveram os pesquisadores. “Por outro lado, alguns pacientes com comprometimento muito modesto da sua [qualidade de vida] parecem ter menos a ganhar com o STN-DBS”, acrescentaram.
O estado cognitivo dos pacientes antes do tratamento, conforme determinado pela Mattis Dementia Rating Scale (MDRS), não foi preditivo de mudança na qualidade de vida em nenhum dos grupos de tratamento. No entanto, escores mais altos de depressão e pior humor correlacionaram-se com maiores melhorias na qualidade de vida entre os pacientes do grupo STN-DBS.
Essas descobertas "podem indicar que esses pacientes têm um potencial de melhora não-motora para obter com a cirurgia", sugeriram os pesquisadores.
Mudanças na qualidade de vida durante os dois anos de acompanhamento foram independentes da idade do paciente, duração da doença, duração das complicações motoras, gravidade da manifestação motora Parkinsoniana sob terapia com levopoda ou complicações do tratamento.
Com base nesses resultados, a equipe acredita que “o comprometimento basal da qualidade de vida é (...) um aspecto razoável a ser considerado para a decisão de tratar com STN-DBS”.
“O sofrimento individual subjetivo medido com o PDQ-39-SI deve ser levado em conta como um fator preditivo para o resultado ao selecionar pacientes com complicações motoras precoces para STN-DBS”, concluíram os pesquisadores. Original em inglês, tradução Google, revisão Hugo. Fonte: Parkinsons News Today.
O estudo com essa descoberta, "Qualidade de vida prediz resultado de estimulação cerebral profunda na doença de Parkinson precoce", foi publicado pela revista Neurology.
A estimulação cerebral profunda (DBS) é uma técnica cirúrgica invasiva na qual fios finos são implantados no cérebro para fornecer pulsos elétricos a áreas específicas, como o núcleo subtalâmico (STN), para aliviar os sintomas motores em pacientes para os quais os medicamentos padrão não são eficazes.
Estudos demonstraram que o DBS pode efetivamente ajudar a controlar os sintomas motores e reduzir a dose diária necessária de medicação, melhorando a qualidade de vida daqueles com Parkinson avançado ou em estágio inicial.
Em um estudo clínico anterior da Fase 4 (NCT00354133) chamado EARLYSTIM, os pesquisadores avaliaram o impacto de longo prazo do STN-DBS como um complemento ao melhor tratamento médico em relação à qualidade de vida em pacientes com doença de Parkinson por um período de mais de dois anos.
O estudo incluiu pacientes com menos de 61 anos que tiveram uma boa resposta à terapia com levodopa, mas que ainda desenvolveram complicações motoras. Entre os participantes, 124 foram tratados com DBS-STN e melhor tratamento médico, enquanto 127 pacientes receberam apenas o melhor tratamento médico.
No estudo mais recente, os pesquisadores revisaram os dados do estudo para entender quais fatores contribuíram para as mudanças detectáveis na qualidade de vida específica da doença, medida pelo índice de 39 itens do questionário Parkinson’s Disease Questionnaire (PDQ-39-SI). O questionário auto-relatado avalia a saúde específica de Parkinson em oito dimensões de qualidade de vida.
A análise revelou que a qualidade de vida ao longo dos dois anos de acompanhamento se correlacionou com o valor inicial do PDQ-39-SI em ambos os grupos de tratamento. Ainda assim, essa associação foi mais pronunciada entre os pacientes que foram tratados com STN-DBS.
Pacientes com comprometimento muito leve devido a Parkinson, correspondendo a valores de PDQ-39-SI menores que 15, não foram beneficiados com STN-DBS em comparação com pacientes tratados apenas com tratamento padrão. Em contraste, os pacientes tratados com STN-DBS que apresentavam feridas PDQ-39-SI superiores a 15 (pior qualidade de vida) no início do estudo apresentaram melhores mudanças na qualidade de vida.
“Em pacientes com avaliações de linha de base muito baixas no PDQ-39-SI, a progressão natural do comprometimento da [qualidade de vida] pode superar a melhora alcançada pelo STN-DBS”, escreveram os pesquisadores. “Por outro lado, alguns pacientes com comprometimento muito modesto da sua [qualidade de vida] parecem ter menos a ganhar com o STN-DBS”, acrescentaram.
O estado cognitivo dos pacientes antes do tratamento, conforme determinado pela Mattis Dementia Rating Scale (MDRS), não foi preditivo de mudança na qualidade de vida em nenhum dos grupos de tratamento. No entanto, escores mais altos de depressão e pior humor correlacionaram-se com maiores melhorias na qualidade de vida entre os pacientes do grupo STN-DBS.
Essas descobertas "podem indicar que esses pacientes têm um potencial de melhora não-motora para obter com a cirurgia", sugeriram os pesquisadores.
Mudanças na qualidade de vida durante os dois anos de acompanhamento foram independentes da idade do paciente, duração da doença, duração das complicações motoras, gravidade da manifestação motora Parkinsoniana sob terapia com levopoda ou complicações do tratamento.
Com base nesses resultados, a equipe acredita que “o comprometimento basal da qualidade de vida é (...) um aspecto razoável a ser considerado para a decisão de tratar com STN-DBS”.
“O sofrimento individual subjetivo medido com o PDQ-39-SI deve ser levado em conta como um fator preditivo para o resultado ao selecionar pacientes com complicações motoras precoces para STN-DBS”, concluíram os pesquisadores. Original em inglês, tradução Google, revisão Hugo. Fonte: Parkinsons News Today.
China realiza a primeira cirurgia remota do mundo usando 5G
O Dr. Ling realizou a operação a partir de Sanya, na ilha de Hainan, enquanto seu paciente estava em Pequim a mais de 1.800 milhas (3.000 km) de distância.
quinta-feira, 14 de março de 2019
O tratamento de Parkinson fornece um aumento de poder nas "baterias" de células cerebrais
Mar 14, 2019 - Os cientistas ganharam pistas sobre como o tratamento da doença de Parkinson, chamado de estimulação cerebral profunda, ajuda a combater os sintomas.
O estudo em estágio inicial, realizado por pesquisadores do Imperial College London, sugere que o tratamento aumenta o número e a força das "baterias" de células cerebrais chamadas mitocôndrias. Essas baterias, por sua vez, fornecem energia às células cerebrais, o que pode ajudar a reduzir problemas com movimentos e tremores.
A estimulação cerebral profunda é um tratamento usado para o estágio avançado da doença de Parkinson, que envolve a implantação cirúrgica de fios finos, chamados eletrodos, no cérebro. Esses fios fornecem pequenos impulsos elétricos na cabeça, o que ajuda a reduzir o movimento lento, o tremor e a rigidez.
No entanto, os cientistas têm dúvidas sobre como o tratamento, que é dado a cerca de 300 pacientes por ano, aborda os sintomas de Parkinson.
O Dr. Kambiz Alavian, autor sênior do estudo do Departamento de Medicina do Imperial College London, disse: “A estimulação cerebral profunda tem sido usada com sucesso para tratar Parkinson há mais de 20 anos e é oferecida aos pacientes quando a medicação não controla mais seus sintomas.
“Mas, apesar do sucesso do tratamento, ainda não sabemos exatamente como a entrega de pulsos elétricos às células cerebrais cria esses efeitos benéficos. Nossos resultados, apesar de estarem em um estágio inicial, sugerem que os pulsos elétricos aumentam as baterias nas células cerebrais. Isso potencialmente abre caminhos para explorar como replicar esse aumento de células com tratamentos não cirúrgicos, sem a necessidade de implantar eletrodos no cérebro”.
Tremores e problemas de movimento
A doença de Parkinson afeta cerca de 127.000 pessoas no Reino Unido e causa a perda progressiva de células cerebrais em uma área chamada substantia nigra. Isso leva a uma redução de uma substância química do cérebro chamada dopamina, que é crucial para controlar o movimento. Como resultado, a condição desencadeia sintomas como tremores e movimentos lentos.
As causas iniciais da doença ainda são desconhecidas, mas estudos recentes sugerem que as células cerebrais da substância negra dos pacientes têm menos mitocôndrias - pequenas estruturas produtoras de energia que mantêm as células vivas.
No mais recente estudo, publicado no The FASEB Journal, cientistas investigaram células cerebrais de três pacientes falecidos com doença de Parkinson que receberam estimulação cerebral profunda (DBS), quatro pacientes falecidos que tiveram a doença de Parkinson mas não receberam DBS e três indivíduos falecidos que não tinham Parkinson.
Todos os cérebros vieram do Parkinson UK Brain Bank, no Imperial College London.
A equipe descobriu que as células cerebrais de pessoas que receberam estimulação cerebral profunda tinham um número maior de mitocôndrias, em comparação com pacientes que não receberam o tratamento. As mitocôndrias nos pacientes DBS também foram maiores do que aqueles em pacientes que não receberam tratamento, sugerindo que podem produzir mais energia.
Banco do cérebro
Os cientistas destacam o fato de que apenas um pequeno número de amostras cerebrais foram usadas para este estudo, mas agora esperamos iniciar investigações maiores.
"Esses tipos de estudos são difíceis de realizar, pois só podem ser realizados depois que um paciente faleceu. Sem o Parkinson UK Brain Bank - e, finalmente, as pessoas afetadas pela doença de Parkinson que escolheram doar seu cérebro após a morte, nós não poderíamos realizar estudos importantes como esses.
“Agora esperamos realizar estudos maiores para explorar novos tratamentos que possam preservar as mitocôndrias das células cerebrais. O objetivo final seria manter as células energizadas por mais tempo e os sintomas de Parkinson na baía.”
Este artigo foi republicado a partir de materiais fornecidos pelo Imperial College London. Nota: o material pode ter sido editado para comprimento e conteúdo. Para mais informações, entre em contato com a fonte citada. Original em inglês, tradução Google, revisão Hugo. Fonte: Technologynetworks. Leia também aqui: Mar 18, 2019 - Deep-brain Stimulation Can Reverse Mitochondria Defects Linked to PD, Study Finds.
O estudo em estágio inicial, realizado por pesquisadores do Imperial College London, sugere que o tratamento aumenta o número e a força das "baterias" de células cerebrais chamadas mitocôndrias. Essas baterias, por sua vez, fornecem energia às células cerebrais, o que pode ajudar a reduzir problemas com movimentos e tremores.
A estimulação cerebral profunda é um tratamento usado para o estágio avançado da doença de Parkinson, que envolve a implantação cirúrgica de fios finos, chamados eletrodos, no cérebro. Esses fios fornecem pequenos impulsos elétricos na cabeça, o que ajuda a reduzir o movimento lento, o tremor e a rigidez.
No entanto, os cientistas têm dúvidas sobre como o tratamento, que é dado a cerca de 300 pacientes por ano, aborda os sintomas de Parkinson.
O Dr. Kambiz Alavian, autor sênior do estudo do Departamento de Medicina do Imperial College London, disse: “A estimulação cerebral profunda tem sido usada com sucesso para tratar Parkinson há mais de 20 anos e é oferecida aos pacientes quando a medicação não controla mais seus sintomas.
“Mas, apesar do sucesso do tratamento, ainda não sabemos exatamente como a entrega de pulsos elétricos às células cerebrais cria esses efeitos benéficos. Nossos resultados, apesar de estarem em um estágio inicial, sugerem que os pulsos elétricos aumentam as baterias nas células cerebrais. Isso potencialmente abre caminhos para explorar como replicar esse aumento de células com tratamentos não cirúrgicos, sem a necessidade de implantar eletrodos no cérebro”.
Tremores e problemas de movimento
A doença de Parkinson afeta cerca de 127.000 pessoas no Reino Unido e causa a perda progressiva de células cerebrais em uma área chamada substantia nigra. Isso leva a uma redução de uma substância química do cérebro chamada dopamina, que é crucial para controlar o movimento. Como resultado, a condição desencadeia sintomas como tremores e movimentos lentos.
As causas iniciais da doença ainda são desconhecidas, mas estudos recentes sugerem que as células cerebrais da substância negra dos pacientes têm menos mitocôndrias - pequenas estruturas produtoras de energia que mantêm as células vivas.
No mais recente estudo, publicado no The FASEB Journal, cientistas investigaram células cerebrais de três pacientes falecidos com doença de Parkinson que receberam estimulação cerebral profunda (DBS), quatro pacientes falecidos que tiveram a doença de Parkinson mas não receberam DBS e três indivíduos falecidos que não tinham Parkinson.
Todos os cérebros vieram do Parkinson UK Brain Bank, no Imperial College London.
A equipe descobriu que as células cerebrais de pessoas que receberam estimulação cerebral profunda tinham um número maior de mitocôndrias, em comparação com pacientes que não receberam o tratamento. As mitocôndrias nos pacientes DBS também foram maiores do que aqueles em pacientes que não receberam tratamento, sugerindo que podem produzir mais energia.
Banco do cérebro
Os cientistas destacam o fato de que apenas um pequeno número de amostras cerebrais foram usadas para este estudo, mas agora esperamos iniciar investigações maiores.
"Esses tipos de estudos são difíceis de realizar, pois só podem ser realizados depois que um paciente faleceu. Sem o Parkinson UK Brain Bank - e, finalmente, as pessoas afetadas pela doença de Parkinson que escolheram doar seu cérebro após a morte, nós não poderíamos realizar estudos importantes como esses.
“Agora esperamos realizar estudos maiores para explorar novos tratamentos que possam preservar as mitocôndrias das células cerebrais. O objetivo final seria manter as células energizadas por mais tempo e os sintomas de Parkinson na baía.”
Este artigo foi republicado a partir de materiais fornecidos pelo Imperial College London. Nota: o material pode ter sido editado para comprimento e conteúdo. Para mais informações, entre em contato com a fonte citada. Original em inglês, tradução Google, revisão Hugo. Fonte: Technologynetworks. Leia também aqui: Mar 18, 2019 - Deep-brain Stimulation Can Reverse Mitochondria Defects Linked to PD, Study Finds.
Assinar:
Postagens (Atom)


