29/03/2022 - Painting with Parkinsons – Southside
Objetivo: atualização nos dispositivos de “Deep Brain Stimulation” aplicáveis ao parkinson. Abordamos critérios de elegibilidade (devo ou não devo fazer? qual a época adequada?) e inovações como DBS adaptativo (aDBS). Atenção: a partir de maio/20 fui impedido arbitrariamente de compartilhar postagens com o facebook. Com isto este presente blog substituirá o doencadeparkinson PONTO blogspot.com, abrangendo a doença de forma geral.
segunda-feira, 28 de março de 2022
domingo, 27 de março de 2022
Ser tratado como se você fosse estúpido.
por John Citron
MARCH 26, 2022 - Não conheço outra maneira de dizer isso além do que o título do tópico diz.
As pessoas normais não têm ideia do que passamos! Minha família, por exemplo, não entende, não importa quantas vezes eu explique a eles que demoro um pouco mais para processar informações e realizar tarefas. Percebi que isso é mais perceptível pela manhã, antes de tomar minha primeira dose.
Eles me acusam de não ouvir quando eu não pulo para fazer as coisas imediatamente, ou de não fazer as coisas rápido o suficiente e eles acabam literalmente me empurrando de lado e assumindo a tarefa. Isso aconteceu há uma semana, enquanto meu irmão e eu estávamos pintando as paredes da sala. Fui encarregado de lavar a madeira e as paredes com um pouco de sapólio e uma esponja áspera. Como eu não estava limpando rápido o suficiente, gritaram comigo e me mandaram sair.
O problema é que não é apenas minha família que faz isso. Um suposto amigo meu, ou agora ex-amigo, fez isso comigo em uma viagem que fizemos juntos. A viagem foi um pesadelo para começar com um carro que estragou me obrigando a alugar um veículo para podermos viajar.
Paramos em um restaurante de fast-food durante nossas viagens. Tive problemas para sair do carro alugado e acompanhar meu “amigo”. Não ajudou o fato de ser verão com temperaturas em torno de 98 F (37 C) com 85% de umidade, o que me fez sentir fraco.
Saí do veículo e me levantei lentamente, pois estava me sentindo tonto e cambaleante. Eu também estava arrastando os pés, e meu andar estava como desligado. Eu ouvi o que ele disse, mas levei tempo para alinhar as tarefas em minha mente o que tinha que ser feito. São esses segundos ou minutos extras que levam as pessoas ao limite, eu acho.
Entramos no restaurante e pegamos nossas bebidas e mesa. Foi então que eu disse minha parte porque eu estava segurando-a por alguns dias, já que este não foi o único incidente em que isso ocorreu porque me pediram para tirar algo do carro e não pulei imediatamente.
Eu disse ao meu “amigo” que não sou estúpido. Estou apenas pensando e fazendo mais devagar e isso me leva tempo para processar o que está sendo dito para que eu possa realizar as tarefas que me levarão um pouco mais de tempo para realizar. Eu disse isso alto o suficiente para os outros ouvirem e olharem para ele enquanto esse grande bruto de um homem se reduzia a nada em seu assento.
Ele ficou um pouco melhor depois, mas não muito. Nós não falamos mais, embora ele tenha me procurado de vez em quando. Original em inglês, tradução Google, revisão Hugo. Fonte: Parkinsons News Today.
quinta-feira, 24 de março de 2022
Desafios da identificação de episódios OFF na doença de Parkinson
March 24, 2022 – Os Drs Laxman Bahroo e Sanjay Iyer discutem desafios comuns na identificação de episódios OFF na doença de Parkinson, a importância da educação do paciente e utilização de diários de rastreamento de sintomas.
Laxman Bahroo, DO: Há uma
pequena porção de pacientes que podem nunca experimentar episódios
OFF antecipadamente. Eles vão te dizer, na primeira vez que eles
tiverem um OFF, eles vão te explicar, e você pode não entender,
porque a explicação deles pode ser mais complicada. Acredito que os
OFFs sem motor são provavelmente os mais desafiadores, porque não
temos certeza se eles estão genuinamente com um OFF não motor ou se
há algo mais acontecendo ao mesmo tempo. A recorrência ou a
natureza repetitiva disso fará mais sentido, se isso acontecer no
final de uma dose ou depois de tomar uma dose. Existem desafios para
identificar OFFs e, como disse o Dr. Iyer, a educação é certamente
um deles e ser capaz de dizer aos pacientes que estejam atentos a
seus OFFs e descubram o que está causando alguns de seus episódios.
Quais você acha que são os desafios de identificar esses episódios
OFF?
Sanjay Iyer, MD: Como você disse no início, as
pessoas não sabem o que esperar. “Eu tenho doença de Parkinson e
minha mão está tremendo, o que vai acontecer amanhã? Será uma
progressão rápida ou lenta? É um dia bom ou um dia ruim?” Muitas
vezes, eles não sabem o que esperar quando tomam a medicação, o
que deve melhorar. Alguns dos desafios são que a vida atrapalha, as
pessoas estão vivendo suas vidas, estão tentando fazer seu
trabalho, estão tentando cuidar de sua família. Eles podem não ser
muito autoconscientes sobre o que está acontecendo de momento a
momento. Precisamos explicar aos pacientes que precisamos observar o
horário de sua medicação e rastrear qualquer coisa que você
esteja sentindo em relação à última dose de levodopa ou à
próxima dose. É um fenômeno de muito ou pouco, ou o que está
acontecendo? Geralmente, é difícil rastrear os sintomas porque as
pessoas também estão tentando viver suas vidas.
Laxman
Bahroo, DO: Concordo completamente, e é difícil rastrear algumas
dessas coisas porque as pessoas podem experimentá-las em quantidades
diferentes. Existem alguns indivíduos que podem experimentar OFFs
menores em partes do dia, outras vezes podem experimentar OFFs mais
graves. Muitas vezes isso depende de quando seus medicamentos são
tomados, quando é a hora mais ativa do dia. As pessoas podem
experimentar OFFs de manhã, no meio do dia e no final de uma dose,
no início de uma dose, no meio de uma dose, e isso dificulta muito o
rastreamento. Há várias coisas diferentes sobre as quais podemos
falar, coisas para rastreá-lo.
Eu gosto de avaliar OFFs
de várias maneiras diferentes. Uma coisa é que eu faço perguntas,
e isso deve ser feito de forma aberta: “Você já tomou uma dose
que atrasou? Você perdeu uma dose, o que acontece?” E muitas
vezes, as pessoas relutam em admitir que tomam doses atrasadas ou
perdem uma dose, não querem admitir. E sejamos honestos, se
tivéssemos que tomar algo 3 vezes ao dia, perderíamos as doses. Eu
sei, porque eu tive que tomar algo 3 vezes ao dia, e sinto falta de
doses, todos nós tomamos. Três vezes ao dia, 4 vezes ao dia, muitas
vezes eu pergunto aos pacientes: “O que acontece quando você perde
uma dose, ou se você toma uma hora ou duas atrasada”? Às vezes
eles vão dizer: “nada”. Eu acho, bom, eles não têm OFFs. Ou
eles me dizem: “Não, 30 minutos depois comecei a notar mais
tremores e estava me perguntando por que, e percebi que não havia
tomado minha pílula das 12 horas e eram 12h45”. E eu direi: “OK,
então é assim que seus OFFs se parecem”. De muitas maneiras, as
pessoas vão descobrir isso sozinhas.
Meu objetivo é
extrair essa informação para mantê-la no meu banco de dados e nas
notas para o que acontece porque quando eles têm mais OFFs, e eles
estão descrevendo, eu quero poder contar com essas informações.
Mas, muitas vezes, a conversa é simples, e falar sobre quando perdem
uma dose, quão ruim é, quais sintomas aparecem? Muitas vezes, eles
podem me dizer: “Eu não apenas tive tremor, mas comecei a ficar
mais suado, fiquei mais vermelho. Eu senti que as luzes estavam se
apagando, as coisas estavam ficando mais escuras.” Há um
componente de efeito para isso também muitas vezes. OFFS motor e não
motor combinados não são desafiadores, são os puramente não
motores que são mais desafiadores.
Para as pessoas em quem há mais desafio, muitas vezes digo a elas: “Olha, talvez um diário de sintomas possa ser seu amigo. Não tenho certeza de quais são esses sintomas, não tenho certeza se estão relacionados à sua doença de Parkinson. Estou tentando sondar e fazer perguntas para ver, está relacionado com a medicação, é o fim de uma dose, é o início de uma dose? E você está me dando respostas como, às vezes está aqui, às vezes está lá, e talvez não haja padrão para isso. Talvez essa seja a variabilidade disso, ou talvez haja, aqui está um diário de sintomas.” Muitas vezes você pode baixar diários de sintomas da internet. Nós mantemos um que praticamente cobre um dia de 20 horas. Os pacientes marcam as doses que tomam nos momentos e, em seguida, registram os sintomas que você deseja, se você deseja que eles rastreiem a discinesia, se você deseja rastrear os OFFs. Normalmente, está OFF e quero que eles rastreiem sua comida. O que você acha dos diários?
Sanjay
Iyer, MD: Os diários podem ser muito úteis se as pessoas forem
organizadas e puderem segui-los e completá-los. As 2 situações com
as quais luto são quando o OFF está relacionado à ansiedade e
outra é a fadiga. Essas são 2 situações em que, é parte de sua
manifestação OFF, ou é um sintoma separado relacionado à doença
de Parkinson? Novamente, voltando ao rastreamento, a que horas isso
acontece? É sempre quando o seu remédio é devido? É sempre nesta
situação? Mas é fácil ignorar esses sintomas não motores e
apenas culpar, bem, a doença de Parkinson causa muitas coisas; pode
estar relacionado com o momento da sua medicação.
Laxman
Bahroo, DO: Com certeza. Vou dizer mais uma coisa, o que você disse
foi muito correto, preciso. Uma coisa que precisamos perceber é que
os diários têm um efeito benéfico que podemos não perceber. Você
dá o diário para um paciente, nós damos talvez 2 folhas de papel,
digamos, preencha 3 ou 4 dias. Uma ressalva, se você planeja usar
diários, entenda que a população com doença de Parkinson pode ser
um pouco obsessiva. Você pode dizer a eles: “Quero que você
acompanhe talvez cerca de 4 ou 5 dias”, porque um paciente pode
retornar com 14 dias de dados. Se eles tiverem 14 dias de dados, você
não poderá vê-los. Eu quero ser capaz de ver um padrão, mas quero
que a relação sinal-ruído seja a meu favor para ver se há um
padrão. Se você me trouxer 14, 15, 16 dias, talvez eu não consiga
ver tanto, ou tão facilmente; são muito mais dados para
percorrer.
Agora, o interessante é que, às vezes, vejo
pacientes, eles marcam uma dose às 2 horas e fazem uma anotação
dizendo: “Olha, a dose foi tomada atrasada”. Eu direi: “Vejo
que sua dose deveria ser às 12, você tomou às 2, e vejo que a
partir das 11:30, você marcou O para OFFs o tempo todo. E adivinhe,
você pegou às 2, e os OFFs continuaram até as 3 horas, você teve
quase 3 horas de OFF.” Parte disso foi o que eu chamo de
auto-infligido, no sentido de que se você tomar sua dose aos 12,
você pode ter tomado uma quantidade menor. Os diários têm um
efeito corretivo nas pessoas, elas percebem exatamente quando estão
comendo, quando estão tomando os remédios, qual é a relação. Às
vezes eles falam: “Olha, eu peguei minha comida às 12h, tomei
minha medicação à 1h, só funcionou às 14h30”. E eu direi:
“Veja, exatamente. Agora que você marcou, você acredita nisso, no
que estamos lhe dizendo, que você pode ou não estar disposto a
aceitar.”
Então tem um efeito corretivo dos diários,
mas eu levo isso com o fato de que os pacientes têm que estar
dispostos a preenchê-los. Acho que o Dr. Iyer está completamente
correto, se você não obtiver bons dados, poderá não obter bons
resultados com isso. É por isso que eu digo às pessoas para
mantê-lo por 3 ou 4 dias, alguns dias nesta semana, alguns dias na
próxima semana e depois voltar para nós, e podemos revisá-los.
Aliás, não conheço o Dr Iyer, mas com certeza reviso esses
diários, às vezes pelo nosso sistema de portal, e faço uma visita
virtual com eles. Eles não precisam trazer diários de volta ao meu
escritório. Eu digo a eles: “Você pode me enviar o diário, as
páginas dele, virtualmente, no dia anterior. Vou revisar na nossa
visita, falaremos sobre isso e podemos conversar, porque as próximas
mudanças que vamos fazer são baseadas nos dados do diário. E eu já
examinei você algumas semanas antes de qualquer maneira.
Sanjay
Iyer, MD: Também é bom poder alavancar um parceiro de cuidados, um
cônjuge, um amigo, um ente querido. E muitas vezes dou a eles um
diário e digo: “Por que você não preenche isso juntos, porque a
percepção do paciente sobre se eles estão LIGADOS ou DESLIGADOS
pode ser diferente”. Uma esposa pode notar, ele está arrastando os
pés agora e não está andando bem, enquanto um paciente pode não
perceber isso. Gosto de envolver o maior número de olhos possível
no processo.
Laxman Bahroo, DO: Com certeza. E muitas vezes, se os pacientes não estão cientes, os diários são um desafio. Direi a eles: “Grave o que você sente que é um OFF e mostre isso para mim”, com o entendimento de que vou pegar 1 ou 2 vídeos disso, talvez cerca de um minuto ou mais, que mostra algo como eles se levantando de uma cadeira e indo. Então eu normalmente tendo a vê-los ON. Quase invariavelmente, quando os indivíduos vêm aos nossos escritórios, eles estão quase sempre ligados. Nesse sentido, chamo de brincadeira uma visita virtual de soro da verdade para muitos pacientes. Eu costumo ver os pacientes OFF porque eles não tomaram a medicação esta manhã porque não precisavam ir a lugar nenhum. Esqueceram de tomar a dose, ou tomaram a dose e era a hora ruim do dia, quando normalmente teriam cancelado a consulta. Mas hoje, eles não o fizeram porque é virtual e eles ficariam sentados em casa. Mas eles me dizem: “Olha, estou tendo um dia de OFF”, e, de certa forma, o virtual é um soro da verdade nesse sentido.
Sanjay Iyer, MD: É sempre importante discutir a situação dos OFFs matinais. Porque todos nós, à medida que envelhecemos, minhas costas doem quando acordo de manhã, estou dolorido, estou duro. Mas entender isso pode ser um momento difícil para muitas pessoas, onde elas são extremamente lentas. De manhã, pode demorar um pouco para a primeira dose de levodopa fazer efeito. Essa é uma situação que tento educar os pacientes sobre esse horário e dizer: “Você realmente percebe muito mais seus sintomas de Parkinson ou é apenas suas costas estão um pouco doloridas e rígidas, como as minhas estão? Original em inglês, tradução Google, revisão Hugo. Fonte: Neurologylive.
Estimulação cerebral profunda na doença de Parkinson: uma meta-análise dos resultados neuropsicológicos a longo prazo
2022 Mar 23 - Resumo
A estimulação cerebral profunda (DBS) do núcleo subtalâmico (STN) ou globo pálido interno (GPi) melhora as funções motoras em pacientes com doença de Parkinson (DP), mas pode causar um declínio em domínios cognitivos específicos. O objetivo desta revisão sistemática e meta-análise foi avaliar os efeitos a longo prazo (1-3 anos) de STN ou GPi DBS em quatro funções cognitivas: (i) memória (recordação tardia, memória de trabalho, recordação imediata), ( ii) funções executivas incluindo controle de inibição (teste Color-Word Stroop) e flexibilidade (fluência verbal fonêmica), (iii) linguagem (fluência verbal semântica) e (iv) humor (ansiedade e depressão). Medline e Web of Science foram pesquisados, e estudos publicados antes de julho de 2021 investigando mudanças de longo prazo em pacientes com DP após DBS foram incluídos. As meta-análises do modelo de efeitos aleatórios foram realizadas usando o software R para estimar a diferença média padronizada (SMD) calculada como g de Hedges com IC de 95%. Foram identificadas 2.522 publicações, das quais 48 atenderam aos critérios de inclusão. Quatorze meta-análises foram realizadas, incluindo 2.039 adultos com diagnóstico clínico de DP submetidos à cirurgia de DBS e 271 controles de DP. Nossos achados acrescentam novas informações à literatura existente ao demonstrar que, em um longo intervalo de seguimento (1-3 anos), tanto os efeitos positivos, como uma leve melhora na ansiedade e na depressão (STN, Hedges' g = 0,34 , p = 0,02), e efeitos negativos, como diminuição da memória de longo prazo (g de Hedges = -0,40, p = 0,02), fluência verbal como fluência fonêmica (g de Hedges = - 0,56, p < 0,0001), e foram observados subdomínios específicos das funções executivas, como o teste Color-Word Stroop (g de Hedges = -0,45, p = 0,003). O nível de evidência qualificado com o GRADE variou de baixo para as pré-análises pós-análise a médio quando comparado a um grupo controle. Original em inglês, tradução Google, revisão Hugo. Fonte: PubMed.
Notícias de última hora: avanço crítico anunciado na imagem do cérebro de Parkinson vivo
March 16, 2022 - Hoje em Barcelona, Espanha, na Conferência
Internacional sobre Doenças de Alzheimer e Parkinson (AD/PD), uma
equipe de pesquisa financiada pela Fundação Michael J. Fox está
anunciando um progresso importante na busca do traçador de imagens
de alfa-sinucleína - uma pesquisa importante prioridade para a
Fundação devido ao seu potencial para transformar o desenvolvimento
de medicamentos.
O dobramento incorreto e a aglomeração
da proteína alfa-sinucleína nas células do cérebro e do corpo são
a marca patológica da doença de Parkinson. Os cientistas acreditam
que essa disfunção tóxica dá origem ao início e à progressão
do Parkinson. A capacidade de visualizar a atividade da
alfa-sinucleína no cérebro vivo seria um divisor de águas para
testar e desenvolver potenciais novos medicamentos para Parkinson.
(Estratégias semelhantes na doença de Alzheimer tiveram um efeito
importante na aceleração do desenvolvimento de medicamentos para
essa doença.)
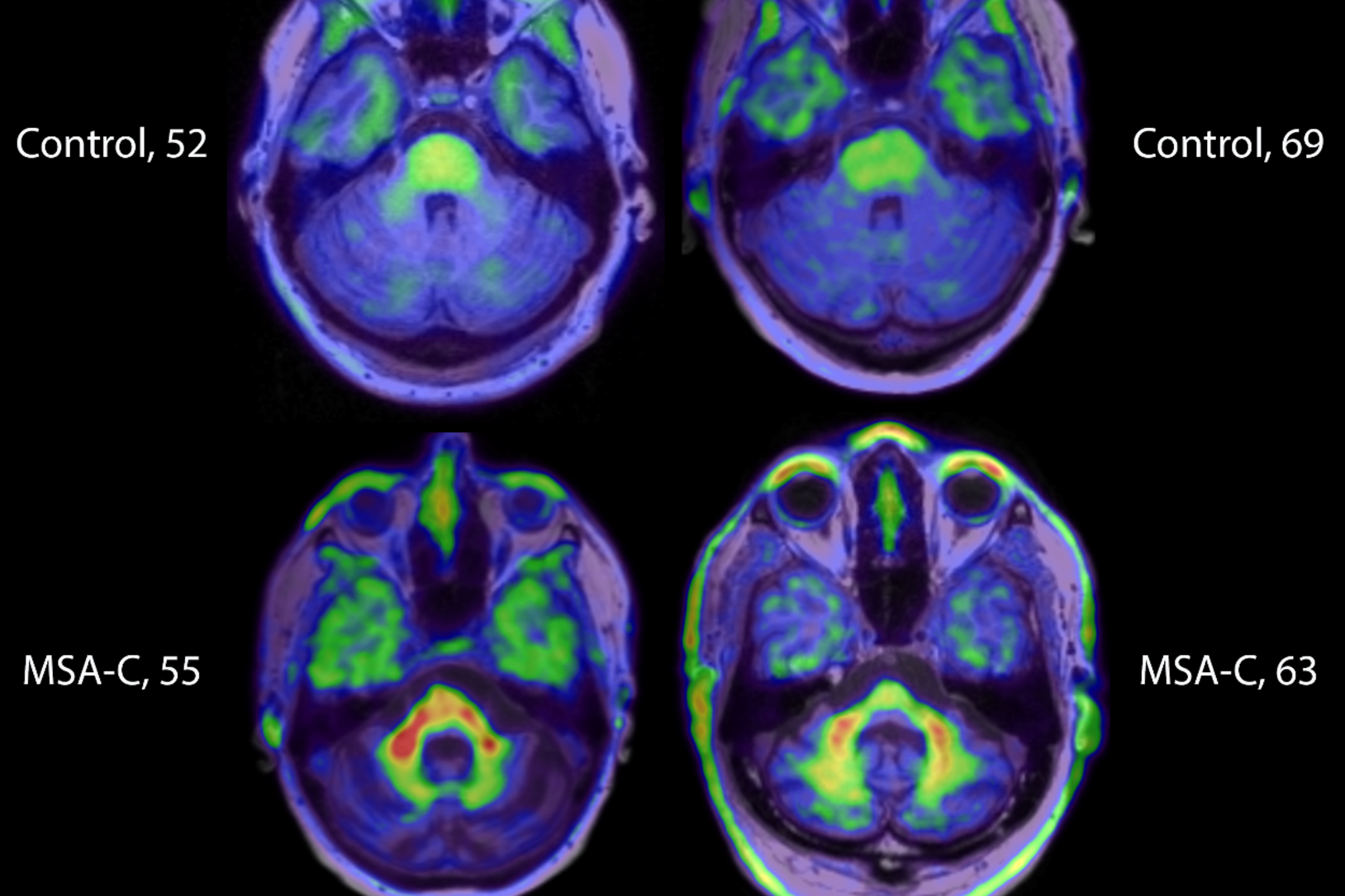
Agora AC Immune, uma empresa de
biotecnologia suíça, compartilhou as primeiras imagens de
alfa-sinucleína no cérebro humano vivo. Eles alcançaram esse
grande passo em frente trabalhando em indivíduos que vivem com
atrofia de múltiplos sistemas (MSA) – um parkinsonismo relacionado
que, como o Parkinson, é caracterizado por dobras incorretas e
aglomeração de alfa-sinucleína no cérebro. Em seu comunicado à
imprensa, a empresa disse que seu rastreador PET (tomografia por
emissão de pósitrons) pode diferenciar pessoas com MSA de
voluntários de controle, pessoas com doença de Parkinson e pessoas
com demência por corpos de Lewy. (Saiba mais sobre essas condições
relacionadas ao Parkinson.)
Se validado, o traçador do AC
Immune deve ser um poderoso trampolim para a ferramenta de traçador
crítica para alfa-sinucleína em pacientes com doença de
Parkinson.
Jamie Eberling, PhD, vice-presidente sênior de
recursos de pesquisa da MJFF, lidera os programas de neuroimagem da
Fundação. “Nossa Fundação há muito apoia o desenvolvimento
dessas ferramentas de imagem críticas, mas indescritíveis, e
estamos animados com esse progresso em sua aplicação generalizada”,
disse ela. “Assim como para a doença de Alzheimer, os marcadores
PET seriam fundamentais para transformar o futuro da pesquisa e do
tratamento de Parkinson”.
A Fundação Michael J. Fox
tem trabalhado para impulsionar o progresso na geração de imagens
de alfa-sinucleína por mais de uma década. O Ken Griffin
Alpha-synuclein Imaging Competition, anunciado em 2020, concedeu à
AC Immune e duas outras equipes (em Mass General Brigham e Merck) um
financiamento significativo para acelerar o trabalho nessa área.
Além disso, em 2016, anunciamos um prêmio de imagem de
alfa-sinucleína a ser concedido à primeira equipe governada por um
júri de especialistas a obter imagens bem-sucedidas de
alfa-sinucleína no cérebro humano vivo.
Atualização
(21/03/22): AC Immune apresentou mais dados sobre seus resultados do
traçador ACI-12589 na conferência AD/PD na sexta-feira, 18 de
março.
“É o assunto da reunião”, disse o Dr.
Eberling. “Há trabalho a ser feito, mas estamos cautelosamente
otimistas.”
Acrescentou Ken Marek, MD, consultor
científico especial do MJFF, que também esteve em Barcelona para a
apresentação: “Este é um primeiro passo importante. Mais dados
são necessários, mas essas descobertas - possibilitadas pelo apoio
da Michael J. Fox Foundation - ajudarão a energizar o campo para
fornecer rastreadores adicionais."
A empresa está
planejando um webinar sobre seu portfólio de diagnóstico e
terapêutico de alfa-sinucleína em 29 de março às 10h ET. Saiba
mais e cadastre-se no site da empresa. Original em inglês, tradução
Google, revisão Hugo. Fonte: MichaelJFox.
segunda-feira, 21 de março de 2022
Novas terapias podem impedir as células T de atacar as células cerebrais na doença de Parkinson
Neurônios Doença de Parkinson. A doença de Parkinson geralmente não é vista como uma doença autoimune. Crédito: Cortesia de Leterrier, NeuroCyto Lab, INP, Marselha, França
MARCH 21, 2022 - Cientistas da LJI descobrem novos alvos para o tratamento da doença de Parkinson.Cientistas do
La Jolla Institute for Immunology (LJI) descobriram que pessoas com
doença de Parkinson têm uma “assinatura genética” clara da
doença em suas células T de memória. Os cientistas esperam que o
direcionamento desses genes possa abrir as portas para novos
tratamentos e diagnósticos de Parkinson.
“A doença de
Parkinson geralmente não é vista como uma doença autoimune”, diz
a professora assistente de pesquisa do LJI Cecilia Lindestam
Arlehamn, Ph.D. “Mas todo o nosso trabalho aponta para que as
células T tenham um papel na doença”.
“Agora que
podemos ver o que essas células T estão fazendo, achamos que a
intervenção com terapias de anticorpos pode ter um impacto na
progressão da doença, especialmente no início”, acrescenta o
professor da LJI Alessandro Sette, Dr. Biol.Sci., que liderou o
trabalho. com Lindestam Arlehamn.
Este estudo foi
publicado recentemente na revista npj Parkinson's Disease.
Uma
visão inconstante do Parkinson
O Parkinson progride à medida
que os neurônios produtores de dopamina no cérebro morrem.
Infelizmente, os cientistas não conseguiram identificar o que causa
essa morte celular – embora tenham uma pista: os neurônios
condenados contêm aglomerados de uma proteína danificada chamada
alfa-sinucleína.
A pesquisa do LJI sugere que esses
aglomerados podem ser o beijo da morte para os neurônios produtores
de dopamina. Sette e Lindestam Arlehamn mostraram recentemente que as
pessoas com Parkinson têm células T que têm como alvo a
alfa-sinucleína no início da doença de Parkinson.
As
células T autorreativas podem danificar as próprias células do
corpo, incluindo os neurônios. Na verdade, as células T
auto-reativas são as culpadas por muitas doenças
autoimunes.
Pesquisadores encontram alvos de drogas
inesperados
O novo estudo oferece uma maneira de parar essas
células T em suas trilhas. A equipe do LJI descobriu que as pessoas
com doença de Parkinson têm células T de memória com uma
assinatura genética muito específica. Esses genes parecem
responsáveis por direcionar a alfa-sinucleína e
potencialmente causar inflamação contínua nos casos de
Parkinson.
“Identificar esses genes permitirá ver quais
pacientes têm células T que respondem à alfa-sinucleína e quais
não”, diz Lindestam Arlehamn.
Um gene importante
expresso nessas células T é o LRRK2. Este gene está associado ao
tipo genético ou familiar da doença de Parkinson. Neurônios em
muitas pessoas com Parkinson expressam LRRK2, mas o novo estudo é o
primeiro a mostrar esse gene expresso em células T.
Mas
muitos dos genes expressos nessas células T foram completamente
inesperados e não estavam previamente ligados à doença de
Parkinson. “Esta descoberta sugere que encontramos novos alvos para
potenciais terapêuticas”, diz Sette.
Os cientistas
encontraram esses genes expressos em amostras de sangue coletadas no
John and Susan Major Center for Clinical Investigation da LJI e por
colaboradores do estudo na UC San Diego, Columbia University Irving
Medical Center e University of Alabama em Birmingham.
“Não
poderíamos ter feito nada desse trabalho sem os doadores de sangue
locais e o trabalho instrumental do nosso Centro de Investigação
Clínica”, diz Lindestam Arlehamn. “Todo mundo envia suas
amostras de sangue para nós, e o LJI Center for Clinical
Investigation as processa.”
O caminho para novas
terapias de Parkinson
No futuro, Lindestam Arlehamn e seus
colaboradores planejam estudar amostras de cérebro post-mortem. Este
trabalho confirmará se as mesmas células T autorreativas
encontradas no sangue também têm como alvo os neurônios em pessoas
com Parkinson. A equipe também quer procurar outros alvos, chamados
antígenos, que possam ser reconhecidos pelas células T em
indivíduos com doença de Parkinson.
Para traduzir esse
trabalho em novas terapias, será importante que os cientistas
estudem como eles podem ativar ou inibir diferentes genes em
diferentes estágios da progressão do Parkinson.
“Temos
muitos caminhos agora para pesquisas futuras”, diz Sette. Original
em inglês, tradução Google, revisão Hugo. Fonte: Scitechdaily.
Fenomenologia dos Transtornos de Ansiedade Atípica na Doença de Parkinson: Uma Revisão Sistemática
2022 Feb 15 - Resumo
Objetivo: A ansiedade é uma preocupação proeminente na doença de Parkinson (DP) que afeta negativamente a qualidade de vida, aumenta a incapacidade funcional e complica o manejo clínico. As apresentações atípicas de ansiedade são pouco reconhecidas e tratadas inadequadamente em pacientes com DP, comprometendo o cuidado global da DP. (...)
Conclusão: A ansiedade atípica é comum, clinicamente relevante e de natureza heterogênea. Uma melhor compreensão da fenomenologia, curso clínico e fisiopatologia das várias formas de ansiedade atípica na DP é necessária para melhorar o reconhecimento, avançar no desenvolvimento terapêutico e, finalmente, otimizar a qualidade de vida na DP. Original em inglês, tradução Google, revisão Hugo. Fonte: PubMed.
domingo, 20 de março de 2022
Clima frio e sintomas de Parkinson
Programado para postar no início do outono no hemisfério sul do nosso planeta, pois hoje, 10/12/21, aqui na praia de Imbé – RS, o clima é primaveril, agradável, entre 17.oC e 25.oC.
November 12, 2019 - Se você acha que os sintomas da doença de Parkinson são piores no clima frio, você não está sozinho. Muitos membros do MyParkinsonsTeam notam maior rigidez, dor e outros sintomas durante os meses de inverno. A doença de Parkinson (DP) afeta a capacidade de uma pessoa de regular a temperatura corporal, o que torna algumas pessoas com DP mais sensíveis a temperaturas quentes ou frias.
O
clima de inverno é extremamente desagradável para alguns membros do
MyParkinsonsTeam. “Neste inverno, quando a temperatura caiu para
[abaixo de zero], senti mais dor, rigidez, congelamento e lentidão”,
postou um membro. “Foi tão opressor que não consegui encontrar
nenhum remédio, exceto cinco cobertores. A dor foi
surpreendente.”
Vários outros membros mencionaram que
as baixas temperaturas podem causar ou piorar a dor relacionada à
doença de Parkinson. “Eu fico resfriado com muita facilidade e
tremo”, escreveu um membro. "Porque estou rígido, realmente
dói estar com frio." Outros concordaram: “Minhas costas e
pescoço estão terrivelmente doloridos, mais do que o normal”.
O
tempo frio também pode agravar os tremores de Parkinson. Um membro
comentou: “Descobri que meus tremores para me manter aquecido
pioram meus tremores”. Outro membro do MyParkinsonsTeam
acrescentou: “Também estou lutando contra o frio agora. Isso
provoca meu tremor, então sempre tenho que ficar aquecido.”
Alguns
membros do MyParkinsonsTeam não sabiam sobre o impacto do resfriado
no DP até que outros membros levantaram a questão. “Achei que
estava sozinho com meus sintomas”, escreveu um membro em resposta a
uma pergunta sobre o tempo frio.
Os membros do
MyParkinsonsTeam compartilham dicas para lidar com o clima frio. Suas
sugestões incluem:
Vestindo camadas: “Tenho que me
lembrar de me vestir adequadamente para o clima e vestir camadas”,
disse um membro que luta contra o frio. Outro membro sugere roupa
íntima térmica para os meses mais frios.
Bolsos: “Eu geralmente visto um moletom com bolsos na frente para manter as duas mãos aquecidas”, escreveu um membro cujas mãos estão sempre geladas.
Cobertores elétricos: “Eu me cubro com cobertores elétricos para aquecer”, recomendou um membro. Um cuidador sugere ligar um cobertor elétrico antes que seja necessário: "Tento me lembrar de pré-aquecer a cama com o cobertor elétrico cerca de 30 minutos antes de ele ir para a cama."
Bolsas de calor reutilizáveis: “Eu aquecia uma dessas bolsas de terapia (com arroz) e colocava sob meus pés”, um membro sugeriu a outro que lutava com os pés gelados.
Banho quente ou piscina: Um membro recomenda banhos quentes para combater o frio, “Eu entro em uma banheira de água quente quando realmente começo a doer [de frio].” Outro recomenda nadar em uma piscina aquecida, "Eu posso ir para uma piscina de 90 graus (Fahrenheit) o ano todo e nadar ou fazer exercícios".
No MyParkinsonsTeam, a rede social e grupo de apoio online para aqueles que vivem e cuidam de alguém com doença de Parkinson, os membros falam sobre uma série de experiências pessoais e lutas. O tempo frio é um tópico frequentemente discutido.
Aqui estão algumas conversas
sobre o tempo frio e os sintomas de Parkinson:
“Este
tempo frio em Michigan é muito difícil para ele. Seu Parkinson
parece não machucá-lo tanto no tempo quente.”
“Alguém mais acha que as mudanças no clima afetam seus sintomas?” Original em inglês, tradução Google, revisão Hugo. Fonte: My ParkinsonsTeam.
sábado, 19 de março de 2022
A equoterapia ajuda pessoas com doença de Parkinson, mostra estudo
March 19, 2022 - Equine therapy helps people with Parkinson’s disease, study shows.
sexta-feira, 18 de março de 2022
Como Michael J. Fox bateu os prognósticos e trabalhou até aos 60 — mesmo com Parkinson
O ator, aposentado desde 2021, continua a assumir-se como um otimista, apesar dos vários problemas de saúde que tem enfrentado.
Aos 60 anos, Fox finalmente reformou-se
18/03/2022 - Michael J. Fox estava no melhor momento da sua carreira. Depois de ser Alex Keaton, o jovem conservador de “Quem Sai aos Seus”, criou um clássico instantâneo em “Regresso ao Futuro”. Continuou a brilhar em episódios da série familiar até 1989 e a trabalhar nas sequelas do filme. Pelo caminho, foi sentindo pequenas mudanças no corpo.
Nada de muito assustador ou grave. Ainda um jovem de 20 e muitos anos, começou a sentir um pequeno tremor no dedo mindinho. Fox não desvalorizou o sintoma e submeteu-se a vários exames, que deram um resultado improvável. O ator fazia parte dos diminutos quatro por cento de pacientes com Parkinson cuja doença é detetada ainda antes dos 30.
“Não sabia o que esperar, mas uma das coisas que recordo e pela qual sempre irei amar a Tracy [a sua mulher] é que nem sequer pestanejou”, recorda sobre o momento em que revelou o diagnóstico à mulher com quem casou em 1988. Hoje, com 60 anos, continua a resistir à doença e descreve-se como o “Senhor Otimismo”. Curiosamente, nunca deixou de trabalhar nas últimas três décadas.
Durante muito tempo, poucos conheciam o diagnóstico que recebeu em 1991. Mais precisamente, durante os sete anos em que Fox conseguiu ocultar as debilidades físicas. Foi, contudo, incapaz de esconder o efeito psicológico provocado pela doença e promessas dos médicos, de que seria incapaz de manter a sua profissão dentro de poucos anos.
Fox recolheu-se e entregou-se ao álcool e à depressão. Durante dois anos a carreira ficou em pausa e a ausência despertou a curiosidade da imprensa e, sobretudo, dos paparazzi. “Ficavam à frente da minha casa a chatear-me. ‘O que é que se passa contigo?’, gritavam. Percebi que não podia obrigar os meus vizinhos a passarem por isto, por isso decidi assumir tudo. Foi uma coisa fantástica.”
Esse período entre 91 e 93 foi um dos mais negros da vida do ator. “A minha primeira reação [ao diagnóstico] foi começar a beber muito. Costumava beber nas festas, para me divertir, mas nessa altura bebia sozinho, todos os dias.” A depressão é também comum em pacientes com Parkinson, sobretudo devido “à degeneração nos circuitos cerebrais, na dopamina, serotonina e epinefrina”, explica um especialista à “People”.
Como Alex Keaton em “Quem Sai aos Seus”.
Fox aproveitou para se tornar num embaixador da doença, uma cara famosa para ajudar a promover o conhecimento e os tratamentos para uma condição da qual, ainda hoje, se sabe muito pouco. Sabe-se que existe um fator genético que a pode causar, mas as origens são ainda muito difusas. Um dos dados que saltou para o debate com a confissão do ator foi o facto de fazer parte de um grupo de pessoas que sofrem de Parkinson desde muito cedo.
Em 1978, Fox participou numa série canadiana chamada “Leo and Me”, tinha apenas 17 anos. Outros três elementos — o realizador, um câmara e um argumentista — também foram diagnosticados com Parkinson, o que gerou muitas discussões sobre potenciais causas da doença.
O ator canadiano-americano haveria de abordar o tema em várias ocasiões, mas nunca gastou muita energia a tentar perceber o que poderia explicar o surgimento da doença. Até porque ela não iria a lado nenhum. “Consigo imaginar milhares de cenários: costumava ir nadar num rio junto a fábricas de processamento de papel e comia o salmão que apanhava; visitei imensas quintas; fumei imensa erva no liceu quando o governo envenenava as culturas. Mas podemos ficar loucos se tentarmos descodificar tudo isso”, explicou em 2020.
A contrariar todas as opiniões médicas, Fox continuou a trabalhar e a fazer filmes, embora sem o fulgor da carreira pré-diagnóstico. Na vida privada, pouco mudou. Ou melhor, tudo mudou: o casal teve o primeiro filho, Sam, em 1989; seguiu-se o par de gémeas em 1995 e a filha mais nova, já em 2001.
“As pessoas sentiam-se estranhamente confortáveis em perguntar-nos se estávamos preocupados com o facto de termos mais filhos, enquanto lidávamos com uma imprevisível escalada de uma grave doença neurológica. Se não tínhamos medo de que os bebés pudessem herdar a doença”, revelou o ator nas suas memórias lançadas em 2021. “A questão era totalmente desapropriada, mas a resposta era só uma: se nós não estávamos preocupados, eles também não deveriam estar.”
Para combater a doença tanto quanto possível, criou a Fundação Michael J. Fox, que desde 2010 financia investigação e terapias focadas não só na cura mas na melhoria da vida dos pacientes. Estima-se que, desde a sua criação, tenha angariado mais de mil milhões de euros.
Infelizmente para Fox, a doença começou a ser cada vez mais notória e a afetar aquela que acreditava ser a sua melhor ferramenta como ator, as expressões faciais. “A minha cara começou a regredir, a tornar-se passiva, quase congelada”, recorda do momento em que decidiu abandonar a série “Spin City” e interromper a carreira. Não faria mais papéis a tempo inteiro, mas isso não o impedia de, ocasionalmente, fazer aparições aleatórias em projetos. Os convites não faltavam.
Colaborou em vários episódios de “Scrubs”, emprestou a sua voz em “Stuart Little 2” e até colaborou em videojogos sobre a saga “Regresso ao Futuro”. “Descobri que conseguia evitar focar-me nos sinais externos e parar de tentar esconder os sintomas”, recorda. Na série de comédia, assumiu o papel de um médico com transtorno obsessivo-compulsivo, o que ajudou a disfarçar a condição.
(Vídeo na fonte)
“Ao invés de tentar ser perfeito, assumi trazer a Parkinson comigo para o estúdio. Ajudou-me a sentir-me mais livre para me concentrar na tarefa principal de um ator, tenha ele ou não condições físicas, que é a de descobrir a vida interna de outro ser humano. Coloquei todo o ênfase nas vulnerabilidades da minha personagem e não da minha própria pessoa. Isso fez com que pudesse fazer desaparecer a doença.”
Nunca mais fez parte do elenco fixo de uma série ou filme, mas em 2009, aceitou um papel recorrente em “The Good Wife”, ao assumir uma personagem com um problema neurológico semelhante a Parkinson. O papel valeu-lhe enormes elogios e três nomeações para os Emmys. E para quem estava mais desligado da arte por causa da doença, a verdade é que Fox queria muito continuar a trabalhar. Em 2012, estreou “The Michael J. Fox Show”, uma série inspirada na sua vida, mas que foi cancelada ao fim de 15 episódios.
O ator foi sempre um exemplo de resiliência, pelo menos até 2017, quando várias quedas o levaram ao hospital e a um novo diagnóstico: um tumor na coluna vertebral estava a crescer e a causar-lhe problemas nos movimentos. Submeteu-se a uma cirurgia para a remoção, mas os riscos eram altos: um passo em falso e Fox poderia ficar paralisado.
De repente, o Senhor Otimista estava assustado. “Tinha este medo de acordar e perceber que a minha vida ia ser completamente diferente”, recordou no seu livro de memórias, lançado em 2021. “Muitos cirurgiões não me queriam tocar, porque achavam que era uma situação que não podia acabar bem. Era muito arriscado.”
(Vídeo na fonte)
Quando conheceu Nicholas Theodore percebeu que queria mesmo avançar com o procedimento e que seria ele o seu cirurgião. “Quando falei com ele, disse-me que percebia porque é que ninguém me queria operar. Aproximou-se de mim e sussurrou: ‘Quem é que quer ser o tipo que paralisa o Michael J. Fox?’. E eu disse-lhe: ‘Se tem tomates para me dizer isto, então tem que ser o meu cirurgião.”
A operação foi bem-sucedida, mas a recuperação foi outro obstáculo difícil. Teve que reaprender a caminhar e a saúde ficou mais debilitada, já sobrecarregada com o peso da doença de Parkinson. Poucos meses depois, uma queda em casa resultou numa fratura no braço que obrigou a colocar 19 parafusos para estabilizar o uso do membro.
“Por estranho que possa parecer, o tumor e o Parkinson eram mais fáceis de aceitar do que a fratura. Essa crise surgiu num instante, como uma explosão. Um cataclismo. Estava completamente impreparado para o que se seguiria e o meu ânimo desvaneceu-se.”
Apesar do regresso do fantasma da depressão e com a saúde a deteriorar-se, Fox continuou a aceitar convites para trabalhar, mesmo com as contínuas falhas de memória e dificuldades na fala, atenuadas por uma intensa medicação. Acabaria por anunciar a reforma no final de 2020, com 59 anos.
“Cheguei a um ponto em que não podia confiar na minha capacidade de falar, o que significava que já não me sentia confortável a interpretar. Foi por isso que decidi reformar-me”, explicou um ano depois da decisão de deixar de vez a profissão. A viver uma vida mais privada, é várias vezes confrontado com a mesma questão: está à espera da descoberta da cura para a doença? “Tenho 60 anos e a ciência é uma coisa difícil”, explica, antes de ir direto ao assunto. “Não.” Fonte: Nit, com fotos e vídeos.
Procuração Médica e Doença de Parkinson
December
20, 2021 - Um diagnóstico de doença de Parkinson é um evento de
mudança de vida que pode alterar a maneira como você pensa sobre
seu futuro. Ter Parkinson pode colocar a vida em perspectiva e trazer
à tona questões sobre as quais você pode não ter pensado,
incluindo como deseja ser cuidado se não puder se defender.
Vários
membros da MyParkinsonsTeam disseram que gostariam de obter
diretrizes antecipadas, mas não conseguiram. Como um membro
compartilhou: “Eu ainda preciso obter uma procuração para minha
filha sobre mim apenas por precaução, já que moro com ela e dois
dos meus netos”. Outro disse: “Precisava fazer a procuração da
minha filha… não posso mais assinar meu nome… ugh!”
Se
você tem medo do processo de criação de um testamento vital ou
preenchimento de diretivas antecipadas, pode ficar mais tranquilo
depois de marcar essa tarefa crítica da sua lista de tarefas. Como
outro membro escreveu: “Vou ser breve. Você precisa de uma
procuração médica. Você pode obter um formulário e instruções
completas no Google.”
Aqui estão alguns detalhes sobre
procuração médica e como selecionar seu agente de saúde.
O
que é uma procuração médica?
Uma procuração médica, às
vezes chamada de procuração durável para assistência médica, é
um documento legal que dá a outra pessoa a capacidade de tomar
decisões médicas em seu nome, se você não puder tomar as
decisões. Nos Estados Unidos, existem algumas leis estaduais
específicas para a criação de uma procuração médica. A pessoa
que você escolher pode ser chamada de seu:
Agente de
saúde
Procuração de cuidados de saúde
Substituto de
saúde
Representante de saúde
Procurador de saúde
Advogado
do paciente
Um
procurador médico deve seguir todas as diretrizes predeterminadas
que você especificar. No entanto, essa pessoa pode tomar decisões
importantes, incluindo continuar com qualquer tratamento de suporte à
vida que você possa precisar. Seu agente também pode decidir se
você será um doador de órgãos após a morte, mas a autoridade
dessa pessoa termina quando você não está mais vivo.
Como
você conclui o processo?
Para a maior parte dos Estados Unidos,
há um formulário simplificado que você pode usar para designar seu
agente de saúde. Este formulário multiestado básico é válido em
todos os estados, exceto Ohio, New Hampshire, Texas e Wisconsin. Cada
um desses outros estados tem sua declaração de divulgação
obrigatória para o mesmo propósito.
Você deve encontrar
formulários de procuração médica no site do governo do seu
estado. A maioria dos estados não exige um notário, mas normalmente
duas testemunhas devem estar presentes para certificar que você
assinou os formulários. Diferentes estados têm regras específicas
sobre quem pode servir como testemunha, portanto, certifique-se de
ler os termos com atenção ou se reunir com um advogado para obter
assistência.
Ao selecionar um agente médico de
procuração, você também pode querer colocar outros documentos
legais para planejamento imobiliário, decisões de cuidados de fim
de vida, beneficiários, planejamento financeiro e outras
necessidades. Peça ao seu médico um encaminhamento para um
assistente social ou advogado que possa ajudá-lo com o processo
enquanto você ainda estiver em um estado de espírito são. Tomar
essas medidas não é importante apenas para pessoas com Parkinson,
mas também para qualquer adulto que queira opinar sobre seus
cuidados futuros.
Benefícios e riscos potenciais
Às
vezes, saber o que fazer não é o mesmo que realmente fazer,
especialmente quando se trata de papelada. Um membro do
MyParkinsonsTeam compartilhou: “Sou assistente social aposentado e
não tenho testamento vital ou DPOA (procuração durável), e
costumava fazer isso por outras pessoas. O que é aquele velho
ditado? Os filhos do sapateiro não têm sapatos? Bem, será uma
prioridade aqui neste inverno.”
Embora possa ser difícil
pensar em um futuro incerto, a escolha de um procurador médico pode
reduzir a carga sobre seus entes queridos se sua saúde piorar.
Delinear suas preferências em diretivas antecipadas dá a você um
melhor controle sobre seus cuidados médicos. No entanto, as
situações de assistência médica podem ser complicadas, e ter uma
pessoa de confiança que possa atuar como seu advogado ajudará sua
equipe de atendimento a lidar com circunstâncias imprevistas.
Ao
tomar decisões com antecedência – ou escolher alguém que entenda
o que você quer – você pode evitar que outras pessoas enfrentem
escolhas difíceis sobre seus cuidados ou se arrependam.
Certifique-se de informar a pessoa que você escolher como seu agente
para que essa pessoa possa estar preparada e disponível se for
chamada. Deixe seus entes queridos conhecerem seu raciocínio para
escolher essa pessoa e incentive-os a apoiar seu agente no
cumprimento de suas responsabilidades de tomada de decisão.
Se
você não escolher um procurador médico, um agente pode ser
escolhido para você. As seguintes pessoas estão legalmente
autorizadas (na ordem listada) para tomar decisões sobre seus
cuidados de saúde se você estiver incapacitado:
Quaisquer
tutores ou conservadores previamente nomeados por um tribunal
Um
cônjuge legal ou parceiro doméstico
Uma criança adulta
Um
irmão adulto
Um cuidador (que não é o seu prestador de
cuidados de saúde)
Um amigo próximo ou parente próximo
Se
você não quiser que nenhuma das pessoas acima tenha poder sobre
seus cuidados, certifique-se de colocar isenções de
responsabilidade para especificar essa escolha. A designação de um
procurador médico garante que sua pessoa ou pessoas preferidas serão
responsáveis.
Sempre há risco envolvido quando você dá
autoridade legal a outra pessoa sobre seus direitos. A procuração
médica não entrará em jogo a menos que você não tenha clareza
mental ou capacidade de se comunicar, no entanto. Um médico deve
verificar sua incapacidade de tomar decisões de saúde antes que seu
agente possa intervir.
Você também pode definir limites
para os tipos de decisões médicas que seu agente pode tomar para
você e eles devem seguir todas as instruções fornecidas. Como um
membro compartilhou: “As procurações são bastante comuns e muito
seguras se montadas corretamente. Você pode ter um POA específico
ou parcial, onde sua pessoa só pode tomar decisões por você sobre
coisas específicas, ou um POA universal, onde seriam todas as
coisas.”
Se um tribunal acreditar que seu agente de
saúde não está agindo em seu melhor interesse ou de acordo com
seus desejos previamente planejados, o direito de procuração médica
pode ser revogado.
Escolhendo a pessoa certa
As leis
estaduais variam, mas, em geral, uma pessoa deve atender a alguns
critérios antes de receber uma procuração médica. Por exemplo,
seu agente deve ser maior de 18 anos ou legalmente emancipado. A
pessoa não pode ser o seu prestador de cuidados de saúde ou o seu
prestador de cuidados de longa duração (se residir numa
instalação), e o seu agente não deve estar relacionado com o seu
prestador de cuidados de saúde ou de cuidados de longa
duração.
Evite escolher alguém em quem você não
confia totalmente ou não acredita que possa lidar com a
responsabilidade. Há muito a considerar antes de assinar um
documento de procuração médica, incluindo se você acha que a
outra pessoa está à altura da tarefa. Só porque alguém se importa
com você não significa que eles sejam a melhor escolha para atuar
como seu representante.
As pessoas que normalmente são
nomeadas para serem agentes de saúde incluem:
Um amigo
próximo
Um membro da família
Um membro de sua comunidade
religiosa
Um vizinho de confiança
Um membro do
MyParkinsonsTeam compartilhou sua experiência, dizendo: “Acabei de
nomear meu filho mais velho como meu POA (power
of attorney – procuração médica) universal
ou completo. Obviamente, seria alguém em quem você confia
implicitamente e que você tem certeza que sobreviverá a
você.”
Idealmente, você deve escolher um procurador
médico antes que sua saúde seja questionada. Como as circunstâncias
podem mudar com o tempo, você tem o direito de alterar seu agente ou
revogar os direitos de seu agente, desde que ainda seja capaz de
tomar suas próprias decisões de saúde. Se um cônjuge recebeu a
procuração, ele pode ter esse direito removido se você se
divorciar.
Converse com outras pessoas que
entendem
MyParkinsonsTeam é a rede social para se conectar com
outras pessoas que vivem com Parkinson. No MyParkinsonsTeam, mais de
80.000 membros se reúnem para fazer perguntas, dar conselhos e
compartilhar suas histórias com outras pessoas que entendem a vida
com a doença de Parkinson.
Você designou uma procuração
médica? Você se encontrou com um advogado ou concluiu o processo
sozinho? Compartilhe sua visão nos comentários abaixo ou inicie uma
conversa postando no MyParkinsonsTeam. Original em inglês, tradução
Google, revisão Hugo. Fonte: MyParkinsons Team.
quinta-feira, 17 de março de 2022
Rugas, pés de galinha? Envelhecimento da pele pode ter origem no cérebro, aponta estudo
16/03/2022 - Rugas, pés de galinha? Envelhecimento da pele pode ter origem no cérebro, aponta estudo.
Parkinson: como o desequilíbrio na flora intestinal pode favorecer o surgimento da doença
Pesquisas brasileiras explicam mecanismo e o impacto das bactérias boas e ruins no desenvolvimento do distúrbio
17/03/22 - O conflito entre as bactérias patogênicas e benéficas no intestino, pode favorecer o surgimento da doença de Parkinson.
As bactérias que vivem em nosso intestino podem influenciar no desenvolvimento e na progressão de distúrbios neurodegenerativos, mostram evidências científicas. Dois estudos brasileiros recentes comprovam essa relação e descrevem como o desequilíbrio da flora intestinal, o conflito entre as bactérias patogênicas e benéficas no intestino (processo chamado de disbiose), pode favorecer o surgimento da doença de Parkinson.
Um dos trabalhos foi conduzido por pesquisadores ligados ao Laboratório Nacional de Biociências (LNBio), que integra o complexo do Centro Nacional de Pesquisa em Energia e Materiais (CNPEM), em Campinas, e apoiado pela Fapesp. Parte dos resultados foi publicado em fevereiro, no periódico iScience. O segundo artigo foi divulgado este mês na revista Scientific Reports.
Vários trabalhos recentes relataram consistentemente a existência de disbiose intestinal em portadores de Parkinson esporádico (casos em que não há um fator genético envolvido), reportando uma maior abundância da espécie bacteriana Akkermansia muciniphila em amostras fecais desses pacientes, quando comparados ao grupo-controle. Segundo o coordenador da pesquisa brasileira, Matheus de Castro Fonseca, o diagnóstico de Parkinson costuma ocorrer tardiamente, mas é possível observar sinais do distúrbio precocemente no sistema nervoso entérico, que controla a motilidade gastrointestinal.
"Foi recentemente descrito que células específicas do epitélio intestinal, chamadas de células enteroendócrinas, possuem muitas propriedades semelhantes às dos neurônios, incluindo a expressão da proteína α-sinucleína [αSyn], cuja agregação está sabidamente relacionada com a doença de Parkinson e com outras doenças neurodegenerativas. Por estarem em contato direto com o lúmen intestinal – isto é, o espaço interior dos intestinos – e se conectarem por sinapse com os neurônios entéricos, as células enteroendócrinas formam um circuito neural entre o trato gastrointestinal e o sistema nervoso entérico, sendo assim um possível ator-chave no surgimento da doença de Parkinson no intestino", disse Fonseca à Agência Fapesp.
Com esses conhecimentos, o grupo de pesquisadores brasileiros buscou entender se os produtos secretados pela bactéria Akkermansia muciniphila poderiam iniciar a agregação da α-sinucleína nas células enteroendócrinas. E se a αSyn agregada nessas células poderia, então, migrar para terminações nervosas periféricas do sistema nervoso entérico.
Eles descobriram que a disbiose intestinal pode levar ao aumento de espécies de bactérias que, eventualmente, contribuem para a agregação da αSyn nos intestinos. E que essa proteína pode então migrar para o sistema nervoso central, configurando um possível mecanismo de surgimento da doença de Parkinson esporádica. Fonte: Folha de Pernambuco. Veja mais aqui: Study reveals how gut imbalance can lead to Parkinson’s disease.
quarta-feira, 16 de março de 2022
Eixo cérebro-intestino-microbiota na doença de Parkinson: uma revisão histórica e perspectiva futura
1 June 2022 - Resumo
A doença de Parkinson (DP) é a segunda doença degenerativa mais comum do sistema nervoso central (SNC) depois da doença de Alzheimer. Além dos sintomas motores típicos, as manifestações clínicas dos pacientes com DP incluem sintomas gastrointestinais, que precedem inclusive os sintomas motores. Pesquisas recentes descobriram que a microbiota intestinal regula a interação axial cérebro-intestino através de mecanismos imunológicos, endócrinos e neurais diretos, apoiando a hipótese de que o processo patológico da DP se espalha do intestino para o cérebro. Neste artigo de revisão, destacamos os achados marcantes no campo da DP, com atenção especial ao eixo cérebro-intestino-microbiota. Resumimos as alterações e seus efeitos clínicos na microbiota intestinal e nos metabólitos observados na DP. A microbiota intestinal pode conter alvos apropriados para a prevenção e tratamento da DP. Estudos clínicos de coorte sugerem que certos micróbios intestinais têm efeitos protetores ou patogênicos na progressão da DP. Uma melhor compreensão da interação entre o eixo intestino-cérebro, a microbiota intestinal e a DP tem o potencial de levar a novas abordagens diagnósticas e terapêuticas. Experimentos em animais sugerem que o transplante de microbiota fecal (FMT - fecal microbiota transplantation) é útil para o tratamento da DP, e espera-se que a FMT seja um tratamento eficaz para a DP no futuro. Original em inglês, tradução Google, revisão Hugo. Fonte: Sciencedirect.
segunda-feira, 14 de março de 2022
Efeitos da terapia comportamental da deglutição em pacientes com doença de Parkinson: uma revisão sistemática
13 Mar 2022 - Resumo
Objetivo:
Uma revisão sistemática anterior de 2014 descrevendo os efeitos do
tratamento das terapias de deglutição na doença de Parkinson (DP)
demonstrou a falta de estudos controlados randomizados bem
desenhados. Esta revisão atual apresenta e avalia as evidências
mais recentes para terapias comportamentais de deglutição para
disfagia relacionada à DP para melhorar a tomada de decisão baseada
em evidências dos fonoaudiólogos sobre as escolhas de
tratamento.
Método: Uma revisão sistemática de artigos
publicados em inglês e coreano foi realizada de janeiro de 2014 a
junho de 2020 usando as bases de dados eletrônicas PubMed, Embase e
Cochrane Library. Dois autores pesquisaram independentemente a
literatura e as diferenças após a pesquisa foram resolvidas após
discussão e consenso. Os estudos identificados foram avaliados
quanto à qualidade com a escala de classificação ABC e critérios
de avaliação crítica.
Resultado: Oito estudos após a
busca inicial e três estudos adicionais que atendiam aos nossos
critérios originais, mas não estavam disponíveis gratuitamente ou
publicados após o período de busca inicial também foram incluídos.
Onze estudos incluíram os seguintes tratamentos: terapia de
biofeedback (N = 1), treinamento de coordenação
respiração-deglutição (N = 2), estimulação elétrica
neuromuscular (EENM) (N = 1), treinamento de força muscular
expiratória (EMST) (N = 2) , programa intensivo de deglutição
baseado em exercícios (ISP) (N = 1), estratégia de queixo para
baixo (N = 2), Lee Silverman Voice Treatment (N = 1) e canto
terapêutico (N = 1).
Conclusão: A maioria das
terapias comportamentais melhorou a função de deglutição na DP.
Os tratamentos que melhoraram a função das vias aéreas em todo o
mundo demonstraram efeitos positivos na função da deglutição,
assim como o tratamento intensivo e direcionado da deglutição. No
entanto, a estratégia chin-down não mostrou um efeito significativo
na deglutição medida por avaliações endoscópicas flexíveis da
deglutição. Os efeitos do destreinamento do EMST implicaram a
necessidade de projetar o treinamento de manutenção em DP. No
futuro, são necessários ensaios controlados randomizados bem
desenhados para consolidar os efeitos dessas terapias. Original em
inglês, tradução Google, revisão Hugo. Fonte: Tandfonline.
Alterações neuropatológicas na doença de Parkinson avançada
14 March 2022 - Resumo
Pacientes com doença de Parkinson (DP) avançada apresentam disfunção motora grave, wearing-off, discinesia, demência e insuficiência autonômica. Esses sintomas se correlacionam com o desenvolvimento de achados neuropatológicos, como perda severa de neurônios nigroestriatais e não dopaminérgicos e gliose, e acúmulo de alfa-sinucleína fosforilada (pSyn) no sistema nervoso central e periférico. Além disso, muitas vezes há alterações co-patológicas, incluindo acúmulos de tau e amilóide relacionados ao Alzheimer. De acordo com a hipótese de progressão da DP de Braak, no momento do diagnóstico clínico da DP, o acúmulo de estruturas pSyn-positivas já está disseminado no tronco encefálico e sistema nervoso periférico, e na DP avançada, essas estruturas pSyn-positivas já se espalharam para o sistema límbico e neocórtex. Nesta revisão, descrevemos a neuropatologia básica da DP, com particular atenção à hipótese de Braak e à distribuição de estruturas pSyn-positivas na DP avançada. Original em inglês, tradução Google, revisão Hugo. Fonte: Onlinelibrary Wiley.
sexta-feira, 11 de março de 2022
Você conhece a receita para prevenir a prisão de ventre?
Cerca de 20% do mundo sofre com isso, de acordo com o Guia de Constipação Mundial de Gastroenterologia (GMO)
11 · 03 · 22 - Muitas pessoas no
mundo sabem que a constipação é comum em suas vidas, com o
inconveniente que isso acarreta. De fato, esta patologia tem uma
prevalência estimada em cerca de 20% da população mundial, segundo
o guia de constipação World Gastroenterology (GMO). Além disso, é
mais comum no sexo feminino, em pessoas com estilo de vida sedentário
e nas quais digerem uma dieta pobre em líquidos e fibras (frutas e
legumes). E durante as férias fica ainda pior, pois a mudança de
hábitos e até o “banheiro desconhecido” podem levar a uma
verdadeira tortura intestinal.
Quando podemos falar sobre
constipação?
Os especialistas da Fundação do Sistema
Digestivo Espanhol (FEAD) reconhecem que uma coisa é a definição
clínica deste problema e outra muito diferente que cada paciente
percebe subjetivamente. Os especialistas estabelecem uma escala:
menos de três evacuações por semana, e que as fezes estejam duras,
em pequenas quantidades ou secas, é sinal de que o paciente está
sofrendo de constipação. Mas é claro que cada um tem seu próprio
ritmo intestinal e essa escala não se aplica a todos os casos
igualmente. Portanto, a constipação também é considerada se o
paciente observar uma diminuição no número de vezes que defeca,
exige mais esforço para fazê-lo e as fezes são duras.
Por
outro lado, uma questão importante deve ficar clara: o FEAD não
considera a constipação uma doença, mas pode ser devido a uma
patologia específica (doença de Crohn, colite isquêmica, fissuras
anais ou hemorroidas complicadas). Também pode ser causada pelo
consumo de algumas drogas como:
Benzodiazepínicos
Medicamentos
para Parkinson
Antidepressivos, anti-inflamatórios não
esteroides
Diuréticos
Dieta rica em fibras, a melhor
prevenção
A Fundação
do Sistema Digestivo Espanhol (FEAD) recomenda uma dieta rica em
fibras para prevenir ou tratar a constipação. Embora a fibra
dietética faça parte do que é considerado uma dieta saudável,
também é recomendada para prevenir ou tratar a constipação. O
fato é que a fibra aumenta muito a massa fecal. Portanto, seu
consumo aumenta a frequência de defecação e reduz o tempo de
trânsito intestinal. Mas se não tivermos certeza de quanta fibra
nossa dieta deve conter, os especialistas da FEAD nos oferecem alguns
requisitos mínimos:
Duas porções de vegetais por dia,
pelo menos uma crua, como em saladas, e outra como parte de um prato
elaborado ou como guarnição.
Três pedaços de fruta
diariamente, de preferência inteiros e com casca, desde que
comestíveis, é claro, pois a fibra é encontrada principalmente na
polpa e na casca.
Todos os dias entre quatro e seis porções de produtos que contêm farinha integral ou são enriquecidos com farelo de trigo para maior ingestão de fibras. Como fazer isso? Assim, por exemplo, tome alguns cereais matinais, pão integral nas refeições ou também, como refeição em si, alimentos como massas ou arroz integral.
Semanalmente duas a cinco porções de leguminosas, pois são uma das principais fontes de fibra. Eles podem ser usados como substitutos de cereais e vegetais cozidos pela adição de cereais, aumentando assim o valor biológico do teor de proteínas.
Os especialistas em digestão dão-nos algumas ideias: lentilhas com arroz, guisado com batatas ou homus com pão, etc. Claro, essas quantidades levando em conta que uma porção equivale a um prato individual de cerca de 60 gramas cru. Original em catalão, tradução Google, revisão Hugo. Fonte: Diari de Girona.
Parkinson: quando as rugas da pele são um sintoma precoce da doença
Estudo inédito liderado por cientistas brasileiros identificou a relação
Doença de Parkinson - Foto: Pixabay
11/03/22 - Rugas e perda de viço da pele podem revelar bem mais do que sinais de envelhecimento. Um novo estudo sugere que seriam um indicador visível da presença de depósitos anômalos de proteínas já associados a doenças neurodegenerativas, em especial, o Parkinson.
Realizado por cientistas brasileiros e publicado na revista científica Neurobiology of Aging, o estudo abre mais do que janelas, mas um portal de possibilidades para a compreensão do envelhecimento e de formas para diagnosticar e tratar doenças neurodegenerativas, hoje sem cura.
Ainda no campo da hipótese, o trabalho lança bases para se imaginar, por exemplo, o desenvolvimento de um creme para a pele que possa não apenas retardar e amenizar os sinais de envelhecimento, mas também prevenir ou tratar doenças que atacam o cérebro. Pois, os sinais na pele antecederiam o avanço de distúrbios para o sistema nervoso central.
"A nova pesquisa se soma a trabalhos internacionais recentes, que propõe uma nova compreensão sobre o envelhecimento e as doenças neurodegenerativas ligadas a ele, como o Parkinson e Alzheimer", afirma o neurocientista Stevens Rehen, um dos autores do estudo e pesquisador do Departamento de Genética do Instituto de Biologia da Universidade Federal do Rio de Janeiro (UFRJ) e do Instituto D’Or de Pesquisa e Ensino (IDOR).
A pele de qualquer pessoa definha à medida que se envelhece, mas nem todo mundo terá doenças neurodegenerativas na velhice. Porém, a ciência começa a reunir pistas sobre os fatores que fazem a diferença entre doença e envelhecimento saudável. Os agregados de determinadas proteínas estão logo à frente na lista de culpados.
O estudo investigou o que acontece com a pele quando exposta a agregados, ou seja, depósitos, de uma proteína chamada alfa-sinucleína. Esses agregados de alfa-sinucleína formam as fibras que matam os neurônios produtores de dopamina de pacientes com Parkinson, levando a tremores e problemas motores característicos da doença.
Já se sabia que eles existem na pele de pessoas com Parkinson. Mas não como eles afetam a pele de forma geral. Em condições normais, a alfa-sinucleína é uma proteína importante para as sinapses, a conversa entre os neurônios. Por motivos desconhecidos, ela pode começar a se agregar. Nesse momento, ela se torna tóxica.
"O que fizemos foi ‘desafiar’ um modelo de pele humana com agregados de alfa-sinucleína e o que vimos nos impressionou", explica a neurocientista Júlia Oliveira, pesquisadora do IDOR e primeira autora do estudo, realizado em parceria com a UFRJ e a L’Oreal.
Eles viram a pele envelhecer sob a lente do microscópio. Os cientistas usaram um organoide, uma espécie de “minipele” desenvolvida em laboratório, mas que tem a estrutura da epiderme (a camada superficial) da pele humana. A minipele foi exposta aos agregados de alfa-sinucleína e os pesquisadores observaram que os queratinócitos, as principais células da epiderme humana, passaram a proliferar menos.
Os queratinócitos normalmente têm intensa proliferação, pois são eles que renovam e mantém saudável a pele. Porém, uma vez expostos aos agregados, eles começaram a degenerar. Isso porque os agregados deflagram uma violenta resposta inflamatória do sistema de defesa do organismo.
O sistema imunológico tenta, mas não consegue atacar os agregados. Eles são muito grandes para serem engolidos por células de defesa especializadas e resistentes a todas as enzimas que dissolvem estruturas nocivas, explica Debora Foguel, também autora do estudo e professora titular do Instituto de Bioquímica Médica da UFRJ. O ataque imune fracassado acaba por levar à uma reação inflamatória descontrolada. Com isso, a pele se torna mais fina e imperfeita.
"É a mesma coisa que acontece no envelhecimento", observa Oliveira.
As mudanças na pele podem ser um sinal de alerta antes que os agregados cheguem e se estabeleçam no cérebro. Normalmente, os sinais clínicos das doenças neurodegenerativas só se tornam perceptíveis quando o estrago já está feito no cérebro, observa Foguel.
Como essas proteínas anômalas se acumulam lentamente, à medida que envelhecemos, detectá-las precocemente ainda na pele pode se tornar um instrumento de diagnóstico poderoso para a medicina.
"Será que intervenções na pele podem vir a aliviar a progressão de doenças neurodegenerativas? É o que queremos investigar", salienta Rehen.
O cérebro, que se considerava a origem e o alvo dessas doenças, pode ser apenas o derradeiro destino de um processo iniciado em outras partes do corpo, como a pele e o intestino, onde esses agregados também já foram encontrados em pacientes com Parkinson. Em vez de neurodegenerativas, seriam doenças sistêmicas, isto é, que afetam numerosas partes do corpo.
"Talvez não existam propriamente doenças neurodegenerativas, mas sim doenças sistêmicas provocadas pelo acúmulo de proteínas", diz Foguel.
Parkinson, Alzheimer e uma série de outras doenças neurodegenerativas são causadas pelo acúmulo de depósitos de proteínas. Elas se agregam e formam fibras chamadas de amiloides. Pelo menos 30 proteínas podem formar fibras amiloides associadas a doenças. Os exemplos mais conhecidos são alfa-sinucleína (Parkinson), beta-amiloide (Alzheimer) e príon (mal da vaca louca).
"Uma hipótese interessante que nosso artigo levanta é se esses agregados de alfa-sinucleína seriam capazes de serem transferidos da pele para neurônios periféricos e de lá até o cérebro, contribuindo para o avanço da doença. Um processo semelhante poderia ocorrer com os agregados do Alzheimer", acrescenta Rehen.
A ciência ainda não compreende a complexa linguagem de sinais bioquímicos entre a pele e o cérebro. Mas já descobriu que, no ambiente controlado de laboratório, é possível amenizar o avanço da degeneração provocada pelos agregados ao controlar a inflamação.
Os pesquisadores também querem identificar que motivos fazem proteínas se tornarem nocivas. No caso da pele, a radiação ultravioleta é a candidata mais óbvia por alterar o DNA e a expressão das proteínas, mas não está sozinha.
"Os agregados vão se juntando ao longo da vida. Obesidade, que é inflamatória; infecções virais; dermatites, há numerosas condições que podem influenciar", afirma a neurocientista Marília Zaluar Guimarães, do IDOR e do Instituto de Ciências Biomédicas da UFRJ, que também participou do estudo.
"Os agregados aceleram a degeneração da pele, não apenas de quem tem Parkinson. Não se sabe o quão frequentes são. Porém, podemos vislumbrar formas de cuidar melhor da pele ao tratá-los", enfatiza Júlia Oliveira. Fonte: Folha de Pernambuco.
Demência do corpo de Lewy: causas e sintomas
November 01, 2021 - Demência por corpos de Lewy (LBD - Lewy body dementia) é um termo abrangente para dois tipos relacionados de demência – demência com corpos de Lewy e demência da doença de Parkinson (PDD - Parkinson’s disease dementia). A demência é uma doença que prejudica progressivamente a capacidade de uma pessoa pensar, raciocinar, lembrar e funcionar. Embora essas duas condições tenham características sobrepostas, também existem distinções importantes. Compreender as causas e sintomas de LBD, bem como como seus dois subtipos, demência com corpos de Lewy e PDD, diferem um do outro é fundamental para diagnósticos adequados e encurtar o tempo para iniciar o tratamento.
Leia sobre o diagnóstico e tratamento da demência por corpos de Lewy.
Prevalência de Demência de
Corpos de Lewy
Depois da doença de Alzheimer, os LBDs são a
segunda causa mais comum de demência em pessoas com mais de 65 anos.
Os cientistas não têm certeza de quão comuns são essas demências.
Em uma revisão de estudos sobre demência com corpos de Lewy, sua
prevalência no total de casos de demência variou de 0,3% a 24,4%,
dependendo do estudo. Essa inconsistência é provavelmente porque os
cientistas estão apenas começando a entender a demência com corpos
de Lewy e a diferenciá-la da doença de Alzheimer. Outro estudo
estima que pelo menos 75% dos indivíduos que vivem com doença de
Parkinson (DP) por pelo menos 10 anos desenvolverão
demência.
Causas da Demência de Corpos de Lewy
Os
LBDs são pouco compreendidos, mas acredita-se que sejam
caracterizados pelo acúmulo de corpos de Lewy no cérebro. Os corpos
de Lewy são agrupamentos ou aglomerados de proteínas mal formadas
(desdobradas) chamadas proteínas alfa-sinucleína. As proteínas
alfa-sinucleína saudáveis são normalmente encontradas
amplamente em todo o cérebro e acredita-se que desempenhem muitos
papéis, incluindo a participação na plasticidade. Isso significa
que eles afetam como as células cerebrais se comunicam umas com as
outras e mudam em resposta à experiência de uma pessoa. No entanto,
quando essas proteínas se dobram e se acumulam, o resultado são os
corpos de Lewy, que levam à morte celular no cérebro.
O
tipo de LBD que uma pessoa tem é determinado por onde no cérebro os
corpos de Lewy começam a se formar. Quando os corpos de Lewy começam
a se formar no córtex, a demência com corpos de Lewy é o resultado
mais provável. Esses depósitos iniciais de proteínas no córtex
levam a mudanças cognitivas precoces, como desatenção. Quando os
corpos de Lewy primeiro se depositam em áreas do cérebro mais
relacionadas ao controle motor e movimento, como a substância negra,
o PDD é o resultado mais provável.
Mas o que faz com que
esses corpos de Lewy se formem em primeiro lugar?
A
genética ou elementos hereditários provavelmente desempenham um
papel. Acredita-se que os seguintes genes estejam envolvidos no
espectro de distúrbios relacionados à DP, incluindo demência com
corpos de Lewy e PDD.
APOE
SNCA
LRRK2PD
O gene APOE,
que produz a apolipoproteína E. tem sido associado à demência por
corpos de Lewy. Especificamente, a demência com corpos de Lewy tem
sido associada à presença da variante ε4, assim como a doença de
Alzheimer. PDD não está associado a esta variante do gene.
Essas
doenças também foram associadas a mutações no SNCA (um gene que
controla a produção de alfa-sinucleína) e LRRK2 (um gene que
controla a produção de uma proteína quinase). O LRRK2 é um gene
particularmente interessante, pois as mutações no LRRK2 estão
ligadas ao acúmulo de alfa-sinucleína e proteína tau (outra
proteína anormalmente dobrada que se acumula na doença de
Alzheimer). No entanto, mais pesquisas são necessárias para
entender o complicado papel desses genes e como eles podem estar
interagindo. Alterações nessas proteínas podem levar a
consequências devastadoras para indivíduos com doença de
Parkinson.
Sinais e sintomas de demência do corpo de
Lewy
Existem muitos sinais e sintomas de LBD. Uma característica
importante é o comprometimento cognitivo. É definida na versão
mais recente do Manual Diagnóstico e Estatístico de Transtornos
Mentais (DSM-5) como declínio cognitivo em uma ou mais áreas
(atenção complexa, função executiva, aprendizagem e memória,
linguagem, percepção-motora ou cognição social). Pessoas com
problemas nessas áreas podem ser esquecidas, ter problemas para
prestar atenção, ter problemas para resolver problemas, ser
incapazes de aprender novos fatos ou habilidades, ter dificuldade em
falar ou formar frases ou ter mudanças comportamentais. Esses
sintomas podem variar de leves a graves e, para fazer o diagnóstico,
devem prejudicar significativamente o funcionamento diário de uma
pessoa.
O comprometimento cognitivo não é a única marca
registrada do LBD. Pessoas com demência com corpos de Lewy e PDD
podem se apresentar de maneira muito diferente por causa de como (e
onde) os corpos de Lewy se depositam no cérebro.
A
demência com corpos de Lewy é caracterizada por três
características principais, de acordo com o DSM-5:
Problemas
com a cognição (incluindo variações acentuadas na atenção e no
estado de alerta)
Alucinações visuais
Características espontâneas do parkinsonismo (sintomas motores ou de movimento), que começam após o aparecimento dos sintomas cognitivos
Outras
características que podem sugerir demência com corpos de Lewy
são:
Distúrbio comportamental do sono de movimento
rápido dos olhos
Sensibilidade a medicamentos antipsicóticos
Os
sintomas do PDD são semelhantes, mas o momento é diferente. A
diferença importante é que no PDD, os sintomas do movimento
parkinsoniano (movimento lento, andar arrastado, tremores, tremores,
músculos rígidos, cãibras musculares, problemas de equilíbrio)
começam antes que os sintomas cognitivos e a demência apareçam.
Os
sintomas característicos de ambas as doenças incluem:
Alucinações
visuais – Ver ou ouvir coisas ou pessoas que não estão
lá
Distúrbios do movimento (parkinsonismo) — Movimento
lento, músculos rígidos, tremor e andar arrastado
Problemas
cognitivos — Confusão, falta de atenção, problemas
visuais-espaciais e perda de memória
Dificuldades do sono –
distúrbio comportamental do sono REM e realização de sonhos
durante o sono
Problemas emocionais – Depressão, ansiedade e
apatia
Uma vez que a demência se desenvolve em alguém com
doença de Parkinson (resultando em PDD), não há diferenças
clínicas ou biológicas que possam distingui-la de forma confiável
da demência com corpos de Lewy.
Diagnosticando a Demência
do Corpo de Lewy
Diagnosticar LBD pode ser um desafio. A
demência com corpos de Lewy é mais frequentemente diagnosticada
como doença de Alzheimer. A maior dificuldade no diagnóstico da
demência por corpos de Lewy é o diagnóstico precoce e a
diferenciação da doença de Alzheimer. No PDD, o principal desafio
é a identificação oportuna do comprometimento cognitivo em
indivíduos com doença de Parkinson.
Para fazer um
diagnóstico, os médicos usarão questionários específicos de
entrevista clínica, escalas de classificação e testes
laboratoriais (incluindo neuroimagem, como ressonância magnética e
PET). Exames neurológicos e físicos também serão necessários.
Técnicas de imagem podem ser particularmente úteis ao tentar
distinguir LBD da doença de Parkinson. Avaliações cuidadosas e
precisas e planos de manejo apropriados são componentes necessários
para o diagnóstico de doenças do corpo de Lewy.
Gerenciamento
de sintomas
Várias estratégias de tratamento demonstraram
clinicamente melhorar os sintomas da LBD. Algumas dessas escolhas são
medicamentos e outras são opções baseadas em terapia.
Inibidores
da Colinesterase
Embora os inibidores da colinesterase não
possam curar a demência, eles podem ajudar a retardar o processo e
melhorar os sintomas de alguns indivíduos. Os inibidores da
colinesterase ajudam a aumentar a quantidade de substâncias químicas
importantes chamadas neurotransmissores no cérebro, que podem ajudar
na memória e no funcionamento diário. Em um estudo, pessoas com
demência com corpos de Lewy que foram tratadas com a droga
rivastigmina tiveram melhor humor, maior atenção e diminuição das
alucinações. Os efeitos colaterais geralmente incluem náuseas,
vômitos e redução do apetite.
Antagonistas de
N-metil-D-aspartato
Em outra classe de medicamentos chamados
antagonistas de N-metil-D-aspartato, a memantina demonstrou melhorar
a atenção e a memória em pessoas com demência com corpos de Lewy
e PDD.
Medicamentos para outros sintomas de
demência
Pessoas com LBD podem frequentemente experimentar um
distúrbio do sono chamado distúrbio comportamental do sono com
movimentos rápidos dos olhos. Isso às vezes pode ser tratado com
sedativos como clonazepam ou com melatonina (um hormônio que ajuda a
dormir). Outros sintomas mais graves de LBD, incluindo níveis
flutuantes de alerta (zoning out), alucinações, agitação,
confusão grave e delírio podem ser difíceis de tratar. Os médicos
devem primeiro descartar causas subjacentes, como infecção ou
outros medicamentos que podem estar desencadeando esses sintomas. Se
não for possível encontrar uma causa tratável, os médicos podem
usar uma dose baixa do medicamento antipsicótico atípico quetiapina
para tratar esses sintomas. No entanto, pessoas com LBD não devem
receber antipsicóticos típicos (como haloperidol) ou antipsicóticos
atípicos de alta potência (como olanzapina), pois as pessoas com
LBD são muito sensíveis a esses medicamentos e podem desenvolver
síndrome neuroléptica maligna se os tomarem. Esta é uma condição
com risco de vida que causa febre, rigidez muscular e coração
acelerado, e pode levar à insuficiência cardíaca e renal. Converse
com seu médico sobre as opções de medicação.
Tratamentos
não farmacológicos
Muitos tratamentos não médicos podem
ajudar a melhorar a qualidade de vida de pessoas com doença de
Parkinson, demência com corpos de Lewy e PDD. Algumas dessas opções
incluem terapia cognitivo-comportamental, exercícios físicos e
fisioterapia, ouvir música e estimulação transcraniana por
corrente contínua.
Construindo uma
comunidade
MyParkinsonsTeam é a rede social para pessoas com
doença de Parkinson. No MyParkinsonsTeam, mais de 79.000 membros se
reúnem para fazer perguntas, dar conselhos e compartilhar suas
histórias com outras pessoas que entendem a vida com a doença de
Parkinson.
Você está vivendo com a doença de Parkinson?
Compartilhe sua experiência nos comentários abaixo ou inicie uma
conversa postando no MyParkinsonsTeam. Original em inglês, tradução
Google, revisão Hugo. Fonte: MyParkinsonsTeam.
Demência de corpos de Lewy: diagnóstico e tratamento
October 12, 2021 - Demência de corpos de Lewy (LBD) é um termo genérico para dois tipos de demências semelhantes: demência com corpos de Lewy (DLB) e demência da doença de Parkinson (PDD). As semelhanças entre DLB, PDD e até mesmo a doença de Alzheimer levam a desafios em seu diagnóstico e tratamento. As características marcantes do LBD são distúrbios do movimento, a presença de depósitos de proteínas cerebrais chamados corpos de Lewy e sintomas de demência, como comprometimento cognitivo.
DLB e PDD podem ser difíceis de distinguir,
principalmente em estágios posteriores. Suas semelhanças levaram
alguns pesquisadores a pensar que podem, de fato, ser manifestações
diferentes da mesma doença. Abordagens diagnósticas cuidadosas
nesses casos podem levar a um melhor tratamento dos sintomas e
qualidade de vida.
Leia sobre as causas e sintomas da demência por corpos de Lewy.
Demência de corpos de Lewy:
diagnóstico
O diagnóstico de LBD é complicado e a pesquisa
está em andamento na biologia de DLB e PDD. Compreender como elas
diferem biologicamente pode ajudar a distinguir uma doença da outra,
o que é importante quando se trata de tratamento. Uma maneira que os
pesquisadores podem distinguir DLB de PDD é observando o acúmulo ao
longo do tempo de uma proteína chamada alfa-sinucleína, um
componente dos corpos de Lewy.
Para diagnosticar
definitivamente a LBD, equipes que incluem neurologistas e outros
especialistas usam uma variedade de métodos. Primeiro, eles procuram
sinais clínicos de LBD. Os médicos usam muitos questionários e
pesquisas para medir a cognição e os sintomas de movimento de uma
pessoa, o que pode ajudar a diferenciar esses distúrbios
semelhantes.
Em seguida, varreduras cerebrais especiais,
chamadas tomografia computadorizada por emissão de fóton único
(SPECT) ou tomografia por emissão de pósitrons (PET), podem ser
usadas para encontrar áreas danificadas do cérebro que são típicas
de LBD. Essas varreduras usam moléculas especiais que se ligam a
locais no tecido cerebral chamados transportadores de dopamina. Os
transportadores de dopamina acendem nos exames SPECT e PET e ajudam a
diferenciar o LBD da doença de Alzheimer.
Diagnosticando
Demência com Corpos de Lewy
A demência com corpos de Lewy é
caracterizada por sintomas de demência que começam antes do
aparecimento dos sintomas motores (de movimento). Pesquisas sugerem
que isso ocorre porque as proteínas do corpo de Lewy começam a se
acumular no córtex cerebral, fazendo com que os sintomas cognitivos
apareçam antes dos motores. Esta é uma característica definidora
no diagnóstico de DLB, de acordo com o Manual Diagnóstico e
Estatístico de Transtornos Mentais da American Psychiatric
Association,
Além disso, pelo menos uma dessas
características clínicas principais deve estar presente para que um
diagnóstico de DLB seja feito:
Estados cognitivos
flutuantes, incluindo desatenção e alerta
Alucinações
visuais recorrentes que são muito detalhadas e
vívidas
Características do parkinsonismo (movimentos lentos,
tremores de repouso ou rigidez), com início que ocorre após o
início do declínio cognitivo
Outras características diagnósticas de DLB incluem distúrbio comportamental do sono de movimento rápido dos olhos e sensibilidade neuroléptica grave (medicação antipsicótica). A presença de sintomas motores é a chave para distinguir DLB da doença de Alzheimer, pois sintomas motores ou de movimento não estão presentes na doença de Alzheimer.
Diagnosticando a
Demência da Doença de Parkinson
A demência da doença de
Parkinson é caracterizada por sintomas de demência que ocorrem após
o início da doença de Parkinson. Um diagnóstico de PDD normalmente
consiste em um diagnóstico preexistente de doença de Parkinson, uma
doença de movimento desordenado com declínio cognitivo posterior.
As avaliações clínicas para declínio cognitivo podem incluir
testes de funcionamento executivo (planejamento, pensamento adaptável
e organização) e memória.
Biologicamente falando, os
corpos de Lewy no PDD geralmente começam em áreas do cérebro
relacionadas à função motora, como os gânglios da base. Mais
tarde, à medida que se movem para outras áreas como o córtex, o
declínio cognitivo se torna aparente.
Demência do corpo
de Lewy: tratamento
Para alguém que vive com demência, um
diagnóstico adequado é importante para sua qualidade de vida.
Confusão ou diagnóstico incorreto podem atrasar o tratamento e
causar dificuldades indevidas.
Tratando a demência com
corpos de Lewy
Um tipo de tratamento para DLB é a família de
medicamentos conhecidos como inibidores da colinesterase. Esses
medicamentos ajudam a manter os níveis normais de uma substância
química no cérebro chamada acetilcolina. O tratamento a longo prazo
de indivíduos com DLB usando uma dessas drogas, a rivastigmina –
vendida como Exelon – demonstrou cientificamente aumentar a função
cognitiva e diminuir os sintomas neuropsiquiátricos.
Outro
tipo de medicamento chamado antagonistas de N-metil-D-aspartato
(NMDA) também pode ajudar indivíduos com DLB. A droga antagonista
de NMDA Namenda (memantina) demonstrou melhorar os resultados
clínicos em comparação com placebo em indivíduos com DLB (mas não
PDD).
As drogas
antipsicóticas às vezes são usadas para tratar os sintomas da
demência, como alucinações e agitação. Para indivíduos com DLB,
no entanto, é crucial selecionar a medicação certa. Os efeitos
biológicos do DLB tornam as pessoas mais sensíveis a esses
medicamentos, de modo que certos antipsicóticos podem ser
extremamente prejudiciais.
Tratamento da Demência da
Doença de Parkinson
Medicamentos inibidores da colinesterase
também são usados para tratar indivíduos com PDD, enquanto
estudos com antagonistas de NMDA mostraram resultados mistos. Algumas
pesquisas mostraram que eles não afetam significativamente os
sintomas clínicos, enquanto outros estudos com a mesma droga
(memantina) descobrem que ajudam aqueles com PDD.
Além
dos medicamentos, a terapia cognitivo-comportamental (TCC) provou ser
útil em casos de demência. A TCC é uma forma de terapia de
conversa que se concentra no uso de habilidades, como atenção
plena, para trabalhar com emoções negativas.
O exercício
também é útil em casos de doença de Parkinson. Pode ser capaz de
ajudar aqueles com LBD também. Em um estudo de indivíduos com
doença de Parkinson, exercícios aeróbicos como corrida diminuíram
os comprometimentos cognitivos.
A musicoterapia também
tem sido utilizada em casos de demência. Em um estudo, a
musicoterapia ajudou pessoas com demência leve a moderada a relaxar
e reduziu seus sintomas de depressão. Mais pesquisas são
necessárias para examinar o papel dos tratamentos não tradicionais
para DLB e PDD.
Construindo uma
comunidade
MyParkinsonsTeam é a rede social para pessoas com
doença de Parkinson e seus entes queridos. No MyParkinsonsTeam, mais
de 79.000 membros se reúnem para fazer perguntas, dar conselhos e
compartilhar suas histórias com outras pessoas que entendem a vida
com a doença de Parkinson.
Você está vivendo com a
doença de Parkinson? Compartilhe sua experiência nos comentários
abaixo ou inicie uma conversa postando no MyParkinsonsTeam. Original
em inglês, tradução Google, revisão Hugo. Fonte:
MyParkinsonsTeam.