Objetivo: atualização nos dispositivos de “Deep Brain Stimulation” aplicáveis ao parkinson. Abordamos critérios de elegibilidade (devo ou não devo fazer? qual a época adequada?) e inovações como DBS adaptativo (aDBS). Atenção: a partir de maio/20 fui impedido arbitrariamente de compartilhar postagens com o facebook. Com isto este presente blog substituirá o doencadeparkinson PONTO blogspot.com, abrangendo a doença de forma geral.
quinta-feira, 18 de novembro de 2021
quinta-feira, 11 de novembro de 2021
Ritmo cerebral prevê resposta ao DBS para depressão severa
November 09, 2021 - O ritmo beta do cérebro prevê uma resposta rápida e robusta à estimulação cerebral profunda (DBS) para depressão grave em novas descobertas que podem ajudar a otimizar e personalizar os protocolos de tratamento de DBS, sugerem as primeiras pesquisas.
Em um pequeno estudo, os pesquisadores descobriram que a estimulação breve no momento da implantação dos eletrodos DBS induziu uma diminuição rápida e consistente na potência beta medida no local da estimulação, que se correlacionou com uma diminuição significativa e sustentada dos sintomas depressivos.
"Paciente por paciente, a magnitude da diminuição na potência beta esquerda poderia prever quão bem eles estavam uma semana depois", a investigadora do estudo Helen Mayberg, MD, diretora fundadora do Nash Family Center for Advanced Circuit Therapeutics no Mount Sinai em New York, disse ao Medscape Medical News.
O estudo foi publicado online em 3 de novembro na Translational Psychiatry.
Alvos Ótimos Identificadas
Oito adultos com depressão resistente ao tratamento foram submetidos ao registro eletrofisiológico intraoperatório no momento em que os eletrodos DBS bilaterais foram implantados no subcallosal cingulate (SCC).
Usando modelos de tractografia específicos do paciente antes da cirurgia, os pesquisadores identificaram o alvo ideal dentro do SCC para a colocação do eletrodo.
Durante a cirurgia, foram administrados 20 minutos de estimulação nos alvos definidos pela tractografia ideal, sem estimulação nas 4 semanas após a cirurgia. Local field potentials (LFPs) - sinais elétricos entre neurônios nas profundezas do cérebro - foram registrados simultaneamente durante a estimulação intraoperatória.
Uma semana após breve estimulação intra-operatória, os escores de depressão do paciente diminuíram em 45,6% na escala de avaliação de depressão de Hamilton (HDRS-17) de 17 itens.
Esta resposta antidepressiva precoce se correlacionou com uma diminuição na potência beta registrada no SCC do hemisfério esquerdo. A correlação da melhora dos sintomas com a redução do poder beta do SCC sugere que esse achado eletrofisiológico é um "biomarcador para otimização do tratamento", observam os pesquisadores.
"Este estudo mostra mudanças reproduzíveis e consistentes na leitura do cérebro durante os primeiros minutos de estimulação otimizada na sala de cirurgia em pacientes individuais", disse Mayberg em um comunicado à imprensa.
"Poucos minutos após a estimulação dentro da sala de cirurgia, houve uma mudança no ritmo cerebral beta. Os pacientes que mostraram mudanças maiores, em seguida, experimentaram maior alívio de sua depressão na semana após a cirurgia", acrescentou Allison Waters, PhD, co-autora no estudo e líder do núcleo de eletrofisiologia no Nash Center do Monte Sinai.
Parece que o declínio precoce dos sintomas depressivos é "parcialmente, mas não completamente perdido" durante o período de washout pós-operatório de um mês, observam os pesquisadores.
Além disso, ainda não se sabe se as mudanças induzidas pela estimulação intraoperatória no poder beta são preditivas de uma eventual resposta clínica sustentada ao DBS SCC como terapêutica crônica para a depressão resistente ao tratamento.
Até este ponto, no entanto, DBS SCC crônico nos locais "ideais" definidos pela tractografia levaram a uma taxa de resposta de 88% (7 de 8) após 6 meses de tratamento, eles relatam.
Um passo mais perto da psiquiatria de precisão
"Esta linha de trabalho está movendo o campo um passo mais perto da psiquiatria de precisão", disse Shaheen E. Lakhan, MD, PhD, neurologista em Newton, Massachusetts, ao Medscape Medical News.
"Fora da psiquiatria, muitas doenças têm biomarcadores mensuráveis que se correlacionam com a presença ou gravidade da doença. Por exemplo, para diabetes há hemoglobina A1c e para esclerose múltipla, as lesões cerebrais na ressonância magnética são diagnósticas e prognósticas. Infelizmente, na psiquiatria, os biomarcadores são poucos e distantes entre si", disse Lakhan, que não estava envolvido neste estudo.
"Nas últimas décadas, um fenômeno interessante ocorre com DBS para pacientes com Parkinson avançado - muitas vezes a depressão diminui e o humor melhora. Várias linhas de estudos tentaram separar se isso era principalmente para aliviar os sintomas motores do Parkinson ou [se] DBS está diretamente implicado na melhora do humor. Veja, eis que um subconjunto de pacientes com depressão resistente ao tratamento demonstra melhora nos testes de depressão padronizados ", acrescentou Lakhan.
Este estudo agora mostra que o ritmo beta - um sinal profundo no cérebro que o EEG tradicional não consegue captar - "previu quem mais tarde se beneficiaria com o DBS no momento da implantação", disse Lakhan.
"Isso é incrivelmente importante não apenas para prever a resposta ao DBS para a depressão, mas especificamente para esse biomarcador potencial (ritmo beta profundo) dentro e fora da cirurgia cerebral", disse ele ao Medscape Medical News.
“Outros testes de terapia, por exemplo, com drogas ou neuroativação digital não invasiva e modulação (DiNaMo), podem usar este biomarcador chave para otimizar seu desenvolvimento e maximizar o efeito, um dia, para um determinado indivíduo", previu Lakhan.
"O desafio continua sendo que esses sinais estão no fundo do cérebro e atualmente exigem a implantação cirúrgica de eletrodos para gravações. No entanto, tecnologias como a magnetoencefalografia (MEG), que usam um poderoso magnetismo externo, podem substituir", acrescentou.
O apoio financeiro foi fornecido pelo National Institutes of Health, a Brain Research through Advancing Innovative Neurotechnologies (BRAIN) Initiative e a Hope for Depression Research Foundation. Os dispositivos implantados usados nesta pesquisa foram doados pela Medtronic, Inc. Mayberg recebe honorários de consultoria e licenciamento do Abbott Labs. Lakhan não revelou relações financeiras relevantes.
Transl Psychiatry. Publicado online em 2 de novembro de 2021. Texto completo. Original em inglês, tradução Google, revisão Hugo. Fonte: MedScape.
terça-feira, 9 de novembro de 2021
Conheça ROSA: Robô guia cirurgia cerebral em Houston
November 9th, 2021 - Meet ROSA: Robot guides brain surgery at Houston.
quarta-feira, 27 de outubro de 2021
terça-feira, 26 de outubro de 2021
O que causa flutuações motoras na doença de Parkinson?
10/25/2021 - As flutuações motoras são ocorrências comuns em muitas pessoas com doença de Parkinson à medida que a doença progride. Os pesquisadores acham que são causados por dois motivos.
Efeito
de desgaste
Com o passar do tempo, a doença de Parkinson piora.
A capacidade das células cerebrais (neurônios) de armazenar
dopamina diminui ainda mais. Quando o nível de levodopa no sangue (o
medicamento administrado para tratar o Parkinsonismo) diminui, os
níveis de dopamina despencam e resultam no agravamento dos sintomas
de Parkinson. Este período é chamado de “períodos de folga”
(N.T.: ou estágio off).
Os medicamentos para Parkinson, como levodopa e agonistas da dopamina, perdem seu efeito com o tempo, resultando em um efeito de "desgaste". O efeito de desgaste faz com que os sintomas da doença de Parkinson voltem ou se tornem mais perceptíveis.Aumento da sensibilidade dos neurônios
À medida que a doença de
Parkinson progride, os neurônios se tornam mais sensíveis às
concentrações de levodopa no sangue, tanto maiores quanto menores.
Portanto, em concentrações mais baixas de levodopa, a pessoa
afetada tem maior probabilidade de ter momentos de inatividade. Da
mesma forma, em concentrações mais altas de levodopa, a pessoa
afetada pode apresentar movimentos involuntários anormais chamados
discinesia.
Quais são as diferentes flutuações
motoras?
Os médicos deram nomes a diferentes flutuações
motoras, como:
Desgastando (N.T.: off): O tipo mais comum
de flutuação motora. Isso acontece quando os sintomas de Parkinson
aumentam até que a próxima dose programada de levodopa seja
tomada.
Manhã de folga: os sintomas de Parkinson ocorrem logo
pela manhã, antes que a primeira dose de levodopa comece a fazer
efeito.
Parcial em: Quando uma dose de levodopa não faz efeito
completamente.
Retardado: Quando os sintomas permanecem por mais
tempo, mesmo após a ingestão de uma dose de levodopa.
Falha na
dose: Quando a dose de levodopa falha em mostrar o efeito desejado
sobre os sintomas.
Desativado imprevisível: quando os sintomas
voltam do nada, e isso não pode ser relacionado racionalmente ao
esquema de dosagem.
O que é distonia e congelamento na
doença de Parkinson?
Junto com flutuações motoras e
discinesia, algumas pessoas com doença de Parkinson apresentam
problemas com contrações musculares chamadas distonia e
congelamento.
Distonia são as contrações involuntárias
e contínuas dos músculos que resultam em movimentos repetitivos,
como torcer ou enrolar uma ou mais partes do corpo.
A
distonia pode ocorrer em vários momentos, incluindo:
Quando
o medicamento está funcionando em todo o seu potencial
Quando
os níveis de dopamina são os mais baixos
Quando o medicamento
apenas começou a exercer seu efeito
O congelamento é a
incapacidade temporária e involuntária de se mover. As pessoas
sentem que seus pés estão presos ao chão. Isso pode acontecer por
vários segundos a minutos. O fenômeno resulta da diminuição dos
níveis de dopamina.
Como as flutuações motoras
são tratadas?
As flutuações motoras afetam significativamente
a qualidade de vida das pessoas com Parkinson, limitando suas
atividades da vida diária, mobilidade e interação social. O
tratamento visa manter a pessoa em movimento e fazer com que realize
suas atividades diárias com independência.
Os médicos
podem usar qualquer uma das seguintes estratégias para ajudar as
pessoas afetadas a minimizar ou evitar flutuações motoras:
Ajuste
da dose de levodopa: O médico pode aumentar a dose ou alterar o
número de vezes que o medicamento é tomado por dia.
Apresentando
diferentes medicamentos: Adicionar diferentes medicamentos ao
medicamento atual (levodopa) pode ajudar a manter níveis
consistentes de dopamina e, assim, prevenir tempos de
inatividade.
Esses medicamentos incluem
Inibidores de
catecol-O-metiltransferase
Agonistas dopaminérgicos
Inibidores
da monoamina oxidase-B
Usando uma forma diferente do medicamento: Uma formulação de liberação controlada ou de liberação prolongada do medicamento pode ajudar a proporcionar efeitos por mais tempo. Isso diminui a necessidade de dosagem frequente.
Cirurgia: estimulação cerebral profunda e terapia duopa.
A estimulação cerebral profunda envolve o implante de eletrodos em certas áreas do cérebro e o fornecimento de estimulação elétrica.
A terapia com duopa envolve a administração de carbidopa ou levodopa em forma de gel chamada suspensão enteral. Para a suspensão enteral, os pacientes precisarão ser submetidos a uma cirurgia que envolve a realização de um pequeno orifício na parede jejunal para colocar um tubo no intestino. Original em inglês, tradução Google, revisão Hugo. Fonte: Medicinenet.
quinta-feira, 21 de outubro de 2021
sexta-feira, 8 de outubro de 2021
Pesquisa de estimulação cerebral profunda mostra resultados promissores para o tratamento da doença de Parkinson
A estimulação elétrica pulsada conduz a neuromodulação específica do tipo de célula. Crédito: Rachel Keady Keeney
OCTOBER 8, 2021 - Pesquisadores da Carnegie Mellon University descobriram uma maneira de tornar a estimulação cerebral profunda (DBS) mais precisa, resultando em efeitos terapêuticos que duram mais que o que está disponível atualmente. O trabalho, liderado por Aryn Gittis e colegas do Laboratório Gittis da CMU, avançará significativamente o estudo da doença de Parkinson.
O DBS permite que
pesquisadores e médicos usem eletrodos finos implantados no cérebro
para enviar sinais elétricos à parte do cérebro que controla o
movimento. É uma forma comprovada de ajudar a controlar os
movimentos indesejados do corpo, mas os pacientes devem receber
estimulação elétrica contínua para obter alívio dos sintomas. Se
o estimulador for desligado, os sintomas retornam
imediatamente.
Gittis, professor associado de ciências
biológicas do Mellon College of Science e docente do Instituto de
Neurociências, disse que a nova pesquisa pode mudar isso.
“Ao
encontrar uma maneira de intervir que tenha efeitos duradouros, nossa
esperança é reduzir muito o tempo de estimulação, minimizando os
efeitos colaterais e prolongando a vida útil da bateria dos
implantes.”
Gittis estabeleceu a base para esta
abordagem terapêutica em 2017, quando seu laboratório identificou
classes específicas de neurônios dentro do circuito motor do
cérebro que poderiam ser direcionados para fornecer alívio
duradouro dos sintomas motores em modelos de Parkinson. Nesse
trabalho, o laboratório usou a optogenética, técnica que usa a luz
para controlar neurônios geneticamente modificados. A optogenética,
entretanto, não pode ser usada atualmente em humanos.
Desde
então, ela vem tentando encontrar uma estratégia que seja mais
facilmente traduzida para pacientes que sofrem da doença de
Parkinson. Sua equipe obteve sucesso em ratos com um novo protocolo
DBS que usa rajadas curtas de estimulação elétrica.
“Este
é um grande avanço em relação a outros tratamentos existentes”,
disse Gittis. “Em outros protocolos de DBS, assim que você desliga
a estimulação, os sintomas voltam. Isso parece fornecer benefícios
mais duradouros - pelo menos quatro vezes mais do que o DBS
convencional.”
No novo protocolo, os pesquisadores têm
como alvo subpopulações neuronais específicas no globo pálido,
uma área do cérebro nos gânglios da base, com rajadas curtas de
estimulação elétrica. Gittis disse que os pesquisadores vêm
tentando há anos encontrar maneiras de fornecer estimulação de uma
maneira específica para o tipo de célula.
“Esse
conceito não é novo. Usamos uma abordagem "de baixo para cima"
para direcionar a especificidade do tipo de célula. Estudamos a
biologia dessas células e identificamos as entradas que as
impulsionam. Encontramos um ponto ideal que nos permitiu utilizar a
biologia subjacente”, disse ela.
Teresa Spix, a primeira
autora do artigo, disse que embora existam muitas teorias fortes, os
cientistas ainda não entendem completamente por que o DBS
funciona.
“Estamos meio que brincando com a caixa preta.
Ainda não entendemos cada peça do que está acontecendo lá, mas
nossa abordagem de curta duração parece fornecer maior alívio dos
sintomas. A mudança no padrão nos permite afetar diferencialmente
os tipos de células”, disse ela.
Spix, que defendeu seu
Ph.D. em julho, está animado com a conexão direta que essa pesquisa
tem com os estudos clínicos.
“Muitas vezes, aqueles de
nós que trabalham em laboratórios de pesquisa científica não têm
necessariamente muito contato com pacientes reais. Esta pesquisa
começou com questões de circuito muito básicas, mas levou a algo
que poderia ajudar os pacientes em um futuro próximo”, disse
Spix.
Em seguida, neurocirurgiões da Allegheny Health
Network (AHN) de Pittsburgh usarão a pesquisa de Gittis em um estudo
de segurança e tolerabilidade em humanos. Nestor Tomycz, um
cirurgião neurológico da AHN, disse que os pesquisadores começarão
em breve um estudo randomizado e duplo-cego de pacientes com doença
de Parkinson idiopática. Os pacientes serão acompanhados por 12
meses para avaliar as melhorias nos sintomas motores da doença de
Parkinson e na frequência de eventos adversos.
“Aryn
Gittis continua a fazer pesquisas espetaculares que estão elucidando
nossa compreensão da patologia dos gânglios da base nos distúrbios
do movimento. Estamos entusiasmados com o fato de sua pesquisa sobre
estimulação de explosão mostrar um potencial para melhorar o DBS,
que já é uma terapia bem estabelecida e eficaz para a doença de
Parkinson”, disse Tomycz.
Donald Whiting, o diretor
médico da AHN e um dos maiores especialistas do país no uso de DBS,
disse que o novo protocolo pode abrir portas para tratamentos
experimentais.
“Aryn está nos ajudando a destacar no
modelo animal coisas que vão mudar o futuro do que fazemos por
nossos pacientes. Na verdade, ela está ajudando a evoluir o
tratamento dos pacientes com Parkinson nas próximas décadas com sua
pesquisa”, disse Whiting.
Tomycz concordou. “Este
trabalho realmente ajudará a projetar a tecnologia futura que
estamos usando no cérebro e nos ajudará a obter melhores resultados
para esses pacientes”.
Referência: “A Neuromodulação Específica para a População Prolonga os Benefícios Terapêuticos da Estimulação Cerebral Profunda” 8 de outubro de 2021, Ciência.
DOI: 10.1126 /
science.abi7852
Outros co-autores do estudo são Shruti
Nanivadekar, Noelle Toong, Irene M. Kaplow, Brian R. Isett, Yazel
Goksen e Andreas R. Pfenning.
A pesquisa foi financiada
pela Richard King Mellon Foundation, o Lane Fellows Program, a
Michael J. Fox Foundation e o National Institutes of Health. Original
em inglês, tradução Google, revisão Hugo. Fonte: Scitechdaily. Veja também Aqui: 11 de Outubro de 2021 - Estudo usa técnica inovadora de eletroestimulação para tratamento de Parkinson.
terça-feira, 28 de setembro de 2021
sexta-feira, 17 de setembro de 2021
Controvérsias sobre estimulação cerebral profunda na doença de Parkinson inicial
17 de setembro de 2021 - Uma das grandes dúvidas sobre o tratamento da doença de Parkinson diz respeito ao momento de realizar a cirurgia de estimulação cerebral profunda (DBS, do inglês Deep Brain Stimulation). Segundo o Dr. Rubens Gisbert Cury, neurologista do grupo de distúrbios do movimento da Universidade de São Paulo (USP) e coordenador do ambulatório de DBS do Hospital das Clínicas da USP, é prematuro dizer que a estimulação cerebral profunda reduz a progressão da doença de Parkinson. “Há estudos pré-clínicos, mas ainda falta confirmação. Então, não se deve indicar estimulação cerebral profunda na fase precoce da doença”, disse ele, afirmando, entretanto, que há mudanças em relação à indicação de estimulação cerebral profunda na fase moderada da doença de Parkinson. O médico foi um dos palestrantes do painel Controvérsias na doença de Parkinson, realizado on-line no dia 06 de setembro, durante o XXIX Congresso Brasileiro de Neurologia.
Segundo o Dr. Rubens, a Food and Drug Admnistration (FDA) dos Estados Unidos liberou em 2020 um estudo multicêntrico de fase 3 sobre a estimulação cerebral profunda nos estágios iniciais da doença, o que poderá trazer mais esclarecimentos sobre tema. [1] Atualmente, os critérios de indicação para estimulação cerebral profunda em pacientes com doença de Parkinson são: ter recebido o diagnóstico há no mínimo quatro anos, resposta à levodopa de pelo menos 33% e sintomas descompensados.
“A principal indicação é no caso de complicações motoras refratárias (discinesia ou off) com muita flutuação; o segundo perfil mais indicado é em caso de tremor refratário apesar da medicação; e, por fim, para aqueles que têm intolerância medicamentosa e por isso tomam altas doses de dopaminérgicos”, informou. Trabalhos recentes indicam que o tempo médio de Parkinson indicado para cirurgia varia de 10 a 16 anos. [2]
Em geral, a cirurgia vinha sendo indicada na fase moderada para pacientes com complicações motoras avançadas, ou seja, com muita discinesia, muito off e sem alternativas terapêuticas. O Dr. Rubens disse que houve mudanças nesse ponto: a indicação passou a ser feita na fase moderada, mas diante de complicações motoras também moderadas, porque o risco cirúrgico é menor e o pós-operatório é melhor. “Não tem por que esperar até a complicação motora ficar muito grave”, afirmou. Foi constatado que esses grupos apresentam melhora na qualidade de vida. [3]
A hipersensibilização medicamentosa é outro argumento importante. [4] Ao aumentar muito a dose de medicamento em pacientes com complicações motoras há uma hipersensibilização pós-sináptica, de forma que, com a mesma dose de medicamentos, se induz muito mais discinesias e alterações comportamentais não motoras, como impulsividade e desregulação dopaminérgica. Essa hipersensibilização pós-sináptica pode ser parcialmente irreversível. “Depois da cirurgia, mesmo reduzindo os remédios, o paciente pode ter uma dificuldade no manejo medicamentoso, e a DBS entraria justamente para evitar o aumento dos medicamentos”, explicou o Dr. Rubens.
A cirurgia tem efeito por 15 a 17 anos, como foi demonstrado em um artigo recém-publicado no periódico Neurology. [5] “É óbvio que outros sintomas avançam, principalmente a parte cognitiva, mas para os sintomas que a DBS se propõe a tratar, ainda existe um controle em muito longo prazo”, afirmou o neurologista.
Parkinson é uma doença priônica?
Outra controvérsia discutida no painel foi se a doença de Parkinson seria uma doença priônica. O príon é uma proteína infecciosa, malformada, que pode se espalhar e infectar células saudáveis, causando uma autopropagação, explicou a Dra. Arlete Hilbig, que é neurologista do Centro de Doença de Parkinson e Distúrbios do Movimento da Universidade Federal de Ciências da Saúde de Porto Alegre e Irmandade da Santa Casa de Misericórdia de Porto Alegre (UFCSPA/ISCMPA). A Dra. Arlete disse que o questionamento da relação com o processo priônico começou com a identificação da alfa-sinucleína, proteína associada à doença de Parkinson, cuja propagação seria similar à do príon, de célula a célula.
“Há inconsistências em relação à propagação pela alfa-sinucleína”, afirmou a médica. O modelo não explica todos os casos clínicos e a distribuição anormal da patologia. Além disso, a proteína nem sempre segue uma conectividade neuroanatômica, e pacientes com sintomas avançados e certas formas genéticas não necessariamente têm corpos de Lewy; portanto, não têm o depósito da alfa-sinucleína. Segundo a Dra. Arlete, ainda é preciso esclarecer essas inconsistências para entendermos o desenvolvimento e a progressão da doença de Parkinson. Fonte: Medscape.
quinta-feira, 9 de setembro de 2021
A doença de Parkinson e a estimulação cerebral profunda têm um impacto na minha vida: um estudo multimodal sobre as experiências de pacientes e cuidadores familiares
quinta-feira, 2 de setembro de 2021
Uma Visão Geral da Estimulação Cerebral Profunda (DBS) para Parkinson
September 01, 2021 - A estimulação cerebral profunda (DBS) é um tratamento cirúrgico comum para os sintomas da doença de Parkinson, como rigidez, movimentos lentos e tremores.
O DBS não cura a
doença, mas pode melhorar os sintomas que o medicamento para
Parkinson não está tratando adequadamente. Isso pode resultar em
mais tempo “on” (uma duração mais longa para se sentir bem)
durante o dia.
Este artigo irá discutir como a
estimulação cerebral profunda funciona para o Parkinson, os
sintomas que ela trata, benefícios e riscos, e o que esperar após
esta cirurgia.
Como funciona a estimulação cerebral profunda para o Parkinson?
A estimulação cerebral profunda funciona modificando a atividade elétrica anormal no cérebro. Foi aprovado pela primeira vez para tremores de Parkinson em 1997 e tornou-se um tratamento estabelecido para controlar sintomas motores (relacionados ao movimento) adicionais da doença de Parkinson.
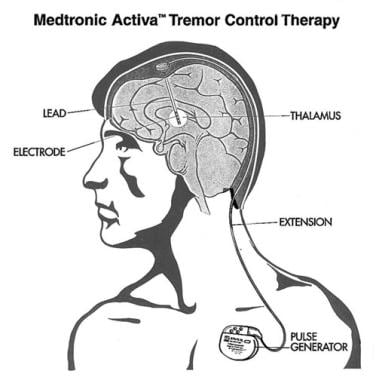
DBS envolve três componentes principais:
Leads: Leads (eletrodos) são implantados no cérebro em uma região responsável pela atividade motora (muscular).
Gerador de pulso implantável (IPG): um procedimento separado é realizado para implantar um dispositivo operado por bateria (aproximadamente do tamanho de um cronômetro) no tórax (sob a clavícula) ou no abdômen. Um IPG é semelhante a um marca-passo para o coração e foi cunhado por alguns como um "marca-passo para o cérebro".
Extensão: Um fio fino e isolado é passado por baixo da pele entre os eletrodos e o gerador de pulsos implantável para fornecer a estimulação elétrica do gerador de pulsos aos eletrodos.
A área alvo no cérebro é primeiro identificada por imagem de ressonância magnética (MRI) ou tomografia computadorizada (TC). Em seguida, os eletrodos são colocados por meio de pequenos orifícios que um cirurgião faz no crânio.
Esta é considerada uma cirurgia minimamente invasiva que é realizada na sala de cirurgia com anestesia local. Geralmente requer pernoite.
O IPG é inserido em um procedimento cirúrgico separado na sala de cirurgia, cerca de uma semana depois.
Após algumas semanas, um neurologista começa a programar a unidade. Esse processo pode levar várias semanas a meses. Quando isso for concluído, as pessoas serão capazes de gerenciar (ligar e desligar) o dispositivo com um controle remoto portátil.
Não se sabe exatamente como o DBS funciona. Acredita-se que os impulsos do gerador interfiram ou bloqueiem sinais elétricos anormais (disparo defeituoso de células nervosas) no cérebro que estão associados à doença de Parkinson.
Acredita-se que esses sinais elétricos anormais, chamados de “ruído” por alguns neurologistas, resultem da perda de dopamina nas células cerebrais que controlam o movimento.1 A dopamina é uma substância química que transmite mensagens entre os nervos.
Existem três regiões diferentes no cérebro onde os eletrodos podem ser implantados: 1
Núcleo subtalâmico
Globus pallidus internus
Núcleo ventral intermediário do tálamo
O DBS do núcleo subtalâmico e do globo pálido pode ajudar com os sintomas motores da doença de Parkinson, enquanto o DBS do núcleo intermediário ventral é feito principalmente para controlar os tremores.
Os sintomas que o DBS trata
A estimulação cerebral profunda é usada principalmente para tratar os sintomas motores (relacionados aos músculos) da doença de Parkinson, mas isso pode variar um pouco entre os diferentes locais de colocação. Os sintomas tratados incluem: 2
Movimentos lentos (bradicinesia)
Tremores
Rigidez (rigidez)
Movimentos anormais (discinesias): discinesias são frequentemente um efeito colateral de medicamentos para a doença de Parkinson e incluem movimentos involuntários, como torcer, balançar a cabeça, contorcer-se e muito mais.
DBS geralmente não é útil com problemas de caminhada ou equilíbrio, embora melhorias nos sintomas acima possam afetar indiretamente a caminhada. Também não fornece benefícios significativos para os sintomas não motores da doença de Parkinson, como alterações cognitivas, alterações de humor (como depressão ou ansiedade) ou problemas de sono.1
Os benefícios do DBS podem ser estimados observando-se como uma pessoa responde à levodopa.3 Os sintomas que respondem à levodopa freqüentemente respondem ao DBS (geralmente no mesmo grau). Mas os sintomas que não mudam com a levodopa provavelmente não melhoram com o DBS.
O DBS geralmente permite uma redução na dosagem de levodopa, que por sua vez pode resultar em menos movimentos involuntários (discinesias) e uma redução no tempo “off”. O resultado muitas vezes é a melhoria da qualidade de vida.4
Quem pode se beneficiar com a estimulação cerebral profunda?
Vários critérios podem ajudar a identificar pessoas que são boas candidatas à estimulação cerebral profunda. Isso inclui pessoas que: 3
Vivem com a doença de Parkinson há pelo menos cinco anos, embora o procedimento tenha sido aprovado para os primeiros sintomas em 2016 e agora esteja sendo avaliado para ver se oferece benefícios para pessoas no início da doença.
Têm sintomas que
não são bem controlados com medicamentos
Estão respondendo
aos medicamentos para Parkinson (levodopa): o procedimento só deve
ser feito para pessoas que estão respondendo a este tratamento, mas
os efeitos dos medicamentos flutuam durante o dia e a eficácia do
medicamento está diminuindo.
Descobrir que os sintomas não
controlados estão diminuindo sua qualidade de vida
Estão
relativamente bem cognitivamente (sem demência significativa)
No
momento, não há limite de idade definido para DBS, mas a eficácia
pode ser menor em pessoas mais velhas.5
Quem deve ter
estimulação cerebral profunda?
Se os medicamentos estão
ajudando com seus sintomas relacionados ao movimento da doença de
Parkinson, mas não os controlam completamente, você pode ser um
candidato à estimulação cerebral profunda.
Locais de
estimulação cerebral profunda e controle de sintomas
Embora a
estimulação do núcleo subtalâmico (STN) e do globo pálido (GPi)
ajude a melhorar os sintomas motores da doença de Parkinson, os
estudos encontraram algumas diferenças.
O DBS do terceiro
alvo, o núcleo intermediário ventral, pode ser benéfico para
controlar os tremores, mas não funciona tão bem no tratamento de
outros sintomas motores da doença de Parkinson.
Em um
estudo canadense, a segmentação do núcleo subtalâmico permitiu
que as pessoas reduzissem as doses de seus medicamentos em um grau
maior, enquanto a segmentação do globo pálido interno foi mais
eficaz para movimentos anormais (discinesias).6
Em outro
estudo, a estimulação cerebral profunda STN também levou a uma
maior redução nas dosagens de medicamentos. No entanto, a
estimulação GPi resultou em maior melhora na qualidade de vida e
também pareceu ajudar na fluência da fala e nos sintomas de
depressão.7
Os efeitos colaterais do DBS às vezes podem
incluir mudanças cognitivas sutis (um declínio). Outro estudo
comparou esses efeitos em relação a essas diferentes áreas.
GPi
mostrou declínios neurocognitivos menores (olhando para coisas como
atenção e memória) do que STN, embora os efeitos fossem pequenos
com ambos. Em uma nota positiva, ambos os procedimentos pareceram
reduzir os sintomas de depressão após a cirurgia.
Riscos
e efeitos colaterais da estimulação cerebral profunda
Como
qualquer cirurgia, a estimulação cerebral profunda pode ter efeitos
colaterais e acarreta riscos potenciais. Também é importante
considerar as complicações e efeitos colaterais dos medicamentos
que você toma, uma vez que suas dosagens muitas vezes podem ser
reduzidas após a cirurgia.
Embora o DBS possa causar
efeitos colaterais, também pode reduzir os efeitos colaterais dos
medicamentos.
Riscos
Os riscos da estimulação
cerebral profunda podem ser divididos em aqueles que envolvem a
cirurgia e aqueles que envolvem os dispositivos e conexões. É
importante observar que o DBS não parece causar nenhum dano
permanente significativo ao cérebro.
Além dos riscos
gerais de cirurgia e anestesia, as complicações podem
incluir:
Sangramento (hemorragia
cerebral)
Golpe
Infecção
Colocação imprecisa dos
cabos ou falta de benefício, mesmo com a colocação
adequada
Convulsões
Confusão
Dor ou inchaço no
local onde os eletrodos são implantados ou onde a bateria é
colocada
Os problemas de hardware podem incluir mau
funcionamento, erosão, migração ou fratura dos cabos ou falha da
bateria.
Em uma revisão de mais de mil pessoas que se
submeteram a DBS para distúrbios do movimento, complicações foram
incomuns.9 Embora cerca de 4% experimentaram sangramento
assintomático nos ventrículos ou córtex do cérebro, apenas 1%
apresentou sintomas de hemorragia cerebral. Outros 0,4% sofreram um
acidente vascular cerebral.
Complicações de longo prazo
relacionadas ao hardware foram observadas em menos de 2% das pessoas
e não exigiram cirurgia adicional. Também foi observado que as
complicações mais comuns poderiam ser evitadas, pelo menos em algum
grau, com planejamento e técnica cuidadosos.9
Efeitos
colaterais
Os efeitos colaterais são comuns, mas tendem a ser
relativamente leves. Eles também podem ser divididos em aqueles
relacionados à cirurgia e aqueles relacionados à estimulação.
É
digno de nota que, ao contrário de outros procedimentos cirúrgicos
para a doença de Parkinson, quaisquer efeitos colaterais que ocorram
com a estimulação podem ser revertidos simplesmente desligando o
dispositivo.
Os efeitos colaterais relacionados à
cirurgia podem incluir dor de cabeça ou piora dos sintomas
emocionais.
Os efeitos colaterais relacionados à
estimulação ocorrem em quase todas as pessoas enquanto o
dispositivo está sendo programado e esse processo pode levar várias
semanas. Isso pode incluir:
Sensações de dormência ou
formigamento (parestesias)
Contrações musculares
involuntárias, rigidez, congelamento (sensação de que seus pés
estão grudados no chão) ou a sensação de músculos sendo
puxados
Distúrbios de fala ou linguagem
Visão dupla ou
outros problemas visuais
Movimentos indesejados
(discinesias)
Tontura
Perda de equilíbrio
Mudanças
de humor (depressão, raiva, ansiedade)
Piora da marcha ou
equilíbrio com caminhada 2
O que esperar depois do DBS
A cirurgia para
implantar os eletrodos geralmente requer pernoite, enquanto o IPG é
geralmente implantado como cirurgia no mesmo dia. Durante a
recuperação, seu cirurgião conversará com você sobre os cuidados
com suas feridas, quando você pode tomar banho e quaisquer
restrições de atividades. Normalmente, é recomendado que qualquer
levantamento de peso seja evitado por algumas semanas.
Depois
de mais duas a quatro semanas, você voltará para ter seu
dispositivo programado. Esse processo continuará por várias semanas
para garantir que as configurações de estimulação sejam ideais
para controlar seus sintomas. Durante essas visitas, a você será
mostrado como ligar e desligar o dispositivo com o dispositivo
portátil e verificar o nível da bateria.
Assim que a
programação for concluída, você terá visitas regulares de
acompanhamento para verificar e ajustar a estimulação para manter o
máximo benefício para seus sintomas.
Viver com um
dispositivo DBS
As baterias costumam durar de três a cinco
anos, mas isso pode variar. As baterias recarregáveis podem durar
até 15 anos.
Existem várias precauções relacionadas a
dispositivos elétricos / magnéticos que são importantes, mas
geralmente fáceis de acomodar. Itens como telefones celulares,
computadores e eletrodomésticos geralmente não interferem no
estimulador. Mantenha o seu cartão de identificação do estimulador
à mão quando estiver fora de casa, na carteira ou na
bolsa.
Detectores de roubo
Esteja ciente de que
alguns dispositivos podem fazer com que o transmissor seja ligado ou
desligado. Isso inclui monitores de segurança (detectores de roubo)
que podem ser encontrados na biblioteca e em lojas de varejo.
Se
isso ocorrer acidentalmente, geralmente não é grave, mas pode ser
desconfortável ou resultar na piora dos seus sintomas se o
estimulador for desligado. Ao visitar lojas com esses dispositivos,
você pode pedir para ignorar o dispositivo apresentando seu cartão
de identificação do estimulador.
Eletrônicos
Domésticos
Mantenha o ímã (N.T.: não mais utilizado)
usado para ativar e desativar o estimulador a pelo menos 30
centímetros de distância de televisores, discos de computador e
cartões de crédito, pois o ímã pode danificar esses
itens.
Viagem aérea / detectores de metal
Fale
com o pessoal da checagem quando viajar de avião, pois o metal no
estimulador pode disparar o detector. Se você for solicitado a
passar por uma triagem adicional com uma varinha de detector, é
importante falar com a pessoa que está fazendo a triagem sobre o seu
estimulador.
Como o estimulador contém ímãs, segurar um
dispositivo portátil de detecção sobre o estimulador por mais de
alguns segundos pode interferir no monitoramento do dispositivo.
Outras técnicas, como uma revista, são uma opção. Novamente, é
importante ter seu cartão de identificação do estimulador com você
quando voar.
Diagnóstico Médico e Tratamento
Certos
tipos de ressonância magnética podem ser feitos com o dispositivo,
mas você sempre deve verificar com seu médico a compatibilidade do
seu dispositivo. Alternativas, como tomografia computadorizada,
geralmente são recomendadas caso você não possa fazer ressonância
magnética. O uso de terapia térmica para músculos doloridos, seja
durante a fisioterapia ou com almofada térmica, deve ser
evitado.
Durante a cirurgia, o uso de cautério (queima de
pequenos vasos sanguíneos sangrando) deve ser evitado, por isso é
importante que seus médicos estejam cientes de que você tem um
estimulador no local. Os tratamentos adicionais que podem interferir
com o dispositivo incluem ultrassom terapêutico, litotripsia (para
cálculos renais) e radioterapia.
Preocupações
eletromagnéticas ocupacionais
Devem ser evitadas
situações que impliquem a exposição a grandes campos magnéticos,
máquinas de radar ou correntes de alta tensão. Isso pode incluir
estar perto de geradores de energia elétrica, subestações
elétricas, antenas de rádio amador, soldadores de arco, torres de
transmissão e torres de comunicação de microondas.
A
maioria dessas exposições potenciais são ocupacionais, por isso é
importante conversar com seu médico sobre seu ambiente de trabalho
antes de retornar ao trabalho.
Resumo
A estimulação
cerebral profunda é um procedimento no qual dispositivos
implantáveis transmitem impulsos elétricos ao cérebro. Pode
ser usada para aliviar os sintomas motores da doença de Parkinson em
alguns pacientes. Tem alguns riscos e pode haver efeitos colaterais
leves. Muitas vezes, permite que a pessoa use menos levodopa e tenha
uma melhor qualidade de vida.
Uma palavra de Verywell
A
estimulação cerebral profunda pode resultar no controle a longo
prazo da rigidez, tremores e movimentos lentos em pessoas com doença
de Parkinson que atendem aos critérios de tratamento. Infelizmente,
o DBS não afeta a história natural (progressão) da doença, nem
controla os sintomas não motores, como alterações cognitivas ou
problemas de humor.
Pelo menos até que tenhamos melhores
tratamentos que abordem o processo subjacente da doença de
Parkinson, em vez de tratar apenas os sintomas, o DBS oferece uma
opção adicional para ajudar as pessoas a lidar com os sintomas
muito frustrantes da doença. Original em inglês, tradução Google,
revisão Hugo. Fonte: Very Well Health.
PERGUNTAS FREQUENTES
Por quanto tempo a estimulação cerebral profunda trata os sintomas da doença de Parkinson?
A estimulação cerebral profunda pode muitas vezes fornecer um benefício de longo prazo para a doença de Parkinson. Um estudo de 2021 demonstrou que a estimulação cerebral profunda STN permanece benéfica por pelo menos 15 anos.11 Um estudo de 2020 mostrou que a estimulação cerebral profunda GPi foi benéfica por pelo menos cinco anos.12
Dito isso, é importante observar que o DBS trata os sintomas e não o processo da doença subjacente. Uma vez que a doença de Parkinson é uma doença progressiva sem cura no momento, a piora geralmente é esperada ao longo do tempo, apesar do tratamento ideal.
quarta-feira, 2 de junho de 2021
Após 15 anos, a estimulação cerebral profunda ainda é eficaz em pessoas com Parkinson
2-JUN-2021 - MINNEAPOLIS - A estimulação cerebral profunda continua a ser eficaz em pessoas com doença de Parkinson 15 anos após o implante do dispositivo, de acordo com um estudo publicado em 2 de junho de 2021, na edição online da Neurology®, o jornal médico da Academia Americana de Neurologia.
Os
pesquisadores descobriram que, em comparação com antes da
estimulação cerebral profunda, os participantes do estudo
continuaram a experimentar melhora significativa nos sintomas
motores, que são sintomas que afetam o movimento, bem como uma
redução nos medicamentos 15 anos depois.
A doença de
Parkinson pode afetar progressivamente a fala, o andar e o equilíbrio
devido a uma redução gradual de uma substância química no cérebro
chamada dopamina. Os sintomas de Parkinson de rigidez muscular,
tremor e lentidão de movimento podem ser tratados com um medicamento
chamado levodopa, que restaura temporariamente a dopamina. No
entanto, esse processo de aumento e queda dos níveis de dopamina ao
longo do dia pode causar discinesia, um efeito colateral da medicação
que pode incluir torcer, balançar ou balançar a cabeça.
A
estimulação cerebral profunda controla os sintomas motores da
doença de Parkinson com eletrodos que são colocados em certas áreas
do cérebro. Os eletrodos são conectados a um dispositivo colocado
sob a pele na parte superior do tórax. O dispositivo controla os
impulsos elétricos.
"Os benefícios da estimulação
cerebral profunda parecem durar vários anos, mas não há dados
suficientes disponíveis para mostrar que esses efeitos ainda estão
presentes mais de 15 anos após a cirurgia", disse a autora do
estudo, Elena Moro, MD, PhD, da Universidade Grenoble Alpes em França
e membro da American Academy of Neurology. "Queríamos saber se
as pessoas com doença de Parkinson continuam a se beneficiar deste
tratamento. É emocionante relatar que nosso estudo descobriu que, a
longo prazo, a estimulação cerebral profunda continua a ser eficaz
em pessoas com doença de Parkinson."
Para o estudo,
os pesquisadores identificaram 51 pessoas que tiveram um dispositivo
de estimulação cerebral profunda implantado no hospital
universitário. A idade média para o diagnóstico da doença de
Parkinson foi de 40 anos. A idade média para o implante do
dispositivo foi 51. Os participantes do estudo tinham o dispositivo
em média 17 anos.
Os pesquisadores revisaram os dados de
cada participante sobre problemas de movimento, qualidade de vida,
medicação e pontuações em testes que medem a gravidade e a
progressão da doença de Parkinson.
Os pesquisadores
descobriram que, ao comparar os dados dos participantes antes de
terem um dispositivo implantado com os dados 15 anos depois, a
quantidade de tempo que os participantes experimentaram discinesia
foi reduzida em 75%.
Os pesquisadores também descobriram
que a quantidade de tempo gasto em um “estado off”, quando a
medicação não estava mais funcionando bem, foi reduzida em 59%.
Além disso, o uso de medicamentos para controlar os níveis de
dopamina foi reduzido em 51%.
Os pesquisadores descobriram
poucos efeitos colaterais de ter o estímulo por 15 anos e esses
efeitos colaterais foram na maioria controláveis.
"Nosso
estudo também descobriu que, apesar da progressão natural da doença
de Parkinson e do agravamento de alguns sintomas que se tornaram
resistentes aos medicamentos ao longo dos anos, os participantes
ainda mantiveram uma melhora geral na qualidade de vida", disse
Moro. "Estudos futuros devem continuar a examinar os benefícios
da estimulação cerebral profunda por longos períodos de tempo e em
grupos maiores de pessoas."
Uma limitação do estudo
foi que muitas das pessoas que tiveram estimulação cerebral
profunda no hospital não estavam disponíveis para o estudo 15 anos
depois, seja porque os pesquisadores não puderam mais contatá-los
ou porque eles haviam morrido. É possível que as pessoas no estudo
tenham sido mais saudáveis do que as não incluídas, o que
significa que os resultados podem não refletir totalmente a
experiência de todas as pessoas que usam a estimulação cerebral
profunda. Original em inglês, tradução Google, revisão Hugo.
Fonte: Eurekalert.
quinta-feira, 6 de maio de 2021
A cirurgia devolve a vida aos pacientes com Parkinson
May 5, 2021 - Surgery gives Parkinson's patients their lives back
Assista vídeo, áudio em inglês, no link acima.
quinta-feira, 22 de abril de 2021
sexta-feira, 26 de fevereiro de 2021
Avanços na estimulação cerebral invasiva e não invasiva na doença de Parkinson: da ciência básica às novas tecnologias
260221 - Sobre este Tópico de Pesquisa
A doença de Parkinson (DP) é a segunda
doença neurodegenerativa mais prevalente no mundo. Cerca de uma em
cada 500 pessoas são afetadas pela doença de Parkinson. Este
distúrbio neurodegenerativo leva a tremores, rigidez, dificuldade
para andar, equilíbrio e coordenação, juntamente com vários
sintomas não motores, como disautonomia, problemas cognitivos e
psiquiátricos. A doença afeta gravemente a qualidade de vida dos
pacientes e tem um grande impacto social e econômico. Atualmente,
não há cura para a DP, mas os tratamentos disponíveis ajudam a
reduzir os sintomas. Isso inclui abordagens de suporte, medicamentos,
fisioterapia e estimulação cerebral.
A estimulação
cerebral é uma das áreas da neurociência de crescimento mais
rápido, envolvendo campos neurológicos e de bioengenharia e
impactando milhares de pacientes com diversos distúrbios
neurológicos. Por meio da intervenção elétrica para modular a
função do sistema nervoso, essa tecnologia demonstrou uma melhora
dramática dos sintomas neurológicos motores e não motores e da
qualidade de vida dos humanos. Quer use técnicas invasivas ou não
invasivas, a estimulação cerebral é inerentemente não destrutiva,
reversível e, o mais importante, ajustável.
Nos últimos
anos, testemunhamos avanços científicos crescentes na compreensão
dos mecanismos neurofisiológicos de técnicas invasivas e não
invasivas e seus resultados clínicos de longo prazo em dor,
depressão, doença de Alzheimer, doença de Parkinson e outros
distúrbios do movimento. Notavelmente, a estimulação cerebral
profunda tem sido clinicamente útil para o tratamento da doença de
Parkinson em todos os estágios, melhorando os sintomas motores e não
motores. Porém, o impacto sobre os sintomas não motores parece ser
mais irregular e não investigado completamente.
Uma nova
técnica de DBS - DBS adaptativo - ganhou espaço no campo clínico e
de pesquisa. Essa nova abordagem para a estimulação cerebral
promete melhorar os efeitos colaterais altamente desafiadores da
estimulação cerebral profunda convencional, como distúrbios da
fala, distúrbios incapacitantes da marcha, congelamento da marcha e
mudanças comportamentais. Ao permitir o registro de sinais de
potencial de campo local específico do paciente através dos mesmos
eletrodos de estimulação, o DBS adaptativo pode permitir o ajuste
de estimulação cerebral automatizada no futuro, fornecendo
perspectivas para um melhor gerenciamento dos sintomas da doença de
Parkinson. Esta abordagem de circuito fechado pressupõe um profundo
reconhecimento dos biomarcadores eletrofisiológicos associados a
manifestações clínicas distintas. Caso contrário, as vantagens
deste novo sistema não terão valor. Embora essenciais, tais
habilidades estão longe de ser uma realidade na prática clínica
diária em situações do mundo real.
Finalmente, no campo
da estimulação não invasiva, novas modalidades, como estimulação
theta-burst ou estimulação associativa pareada para estimulação
magnética transcraniana (TMS), estão agora sendo propostas para
controlar vários sintomas na DP. Além disso, novos alvos para TMS e
estimulação elétrica transcraniana (TES) foram propostos, variando
do córtex pré-frontal, córtex motor à medula espinhal, com foco
em vários sintomas diferentes, como depressão, apatia, sintomas
motores e distúrbio da marcha na DP, respectivamente .
Além
disso, novas tecnologias podem oferecer diferentes modalidades de
estimulação elétrica transcraniana além da clássica estimulação
direta transcraniana (tDCS), como estimulação por corrente
alternada (tACS), estimulação transcraniana de ruído aleatório
(tRNS), tDCS pulsado, tACS modulado em amplitude (AM-tACS ) e modos
de estimulação de entrada analógica. Todas essas modalidades podem
eventualmente oferecer diferentes abordagens para a sintomatologia do
DP. Apesar disso, a literatura científica atual carece de evidências
suficientes para sua prática clínica diária.
A novidade na estimulação cerebral é encorajadora, mas ainda temos que resolver alguns problemas críticos de antemão. Em primeiro lugar, devemos esclarecer completamente seus mecanismos de ação no nível celular, seus eventos neurofisiológicos relacionados e seu impacto nas redes neuronais normais e patológicas. Além disso, não se deve ignorar os aspectos clínicos, e definições vitais devem vir antes de verificarmos sua utilidade clínica. Isso inclui a seleção correta de pacientes, o alvo cerebral para cada sintoma, a duração do tratamento e, o mais importante: a eficácia a longo prazo e seus potenciais danos.
Este tópico de pesquisa busca pesquisas
e análises originais abordando essas novas modalidades e abordagens
de estimulação cerebral para estudar e tratar os sintomas motores e
não motores da doença de Parkinson. As inscrições serão
bem-vindas nos seguintes tópicos:
1. Protocolos clínicos
e neurofisiológicos em modelos animais ou humanos usando DBS, tDCS,
tACS, rTMS, TBS, PAS adaptativos na doença de Parkinson, relativos
aos seguintes tópicos:
a. Delineamento dos mecanismos
celulares de ação e reorganização da neuroplasticidade cortical
ou estriatal.
b. Modulação da
atividade da rede neuronal patológica da DP por meio dessas
tecnologias.
2. Protocolos clínicos delineando o impacto
da estimulação cerebral invasiva e não invasiva nos sintomas não
motores da doença de Parkinson.
3. Potencial de campo
local como um biomarcador para o gerenciamento da estimulação
cerebral profunda na doença de Parkinson. Seu significado e
possíveis implicações no processo patogenético da sintomatologia
da DP.
4. Estudos de modelos computacionais que visam
predizer o impacto de cada modalidade de estimulação no resultado
clínico.
5. Estudos de conectividade funcional e
estrutural voltados para o esclarecimento dos mecanismos
fisiopatológicos e terapêuticos e dos resultados do tratamento.
6.
Desenvolvimento e eficácia de novas tecnologias de estimulação
cerebral no tratamento da DP.
Palavras-chave: doença de
Parkinson, estimulação cerebral, estimulação não invasiva, DBS
adaptativo, estimulação cerebral profunda, estimulação elétrica
transcraniana, modelo animal.
Nota importante: Todas as contribuições para este Tópico de Pesquisa devem estar dentro do escopo da seção e do periódico ao qual são enviadas, conforme definido em suas declarações de missão. A Frontiers reserva-se o direito de orientar um manuscrito fora do escopo para uma seção ou periódico mais adequado em qualquer estágio da revisão por pares. Original em inglês, tradução Google, revisão Hugo. Fonte: Frontiersin.
quarta-feira, 17 de fevereiro de 2021
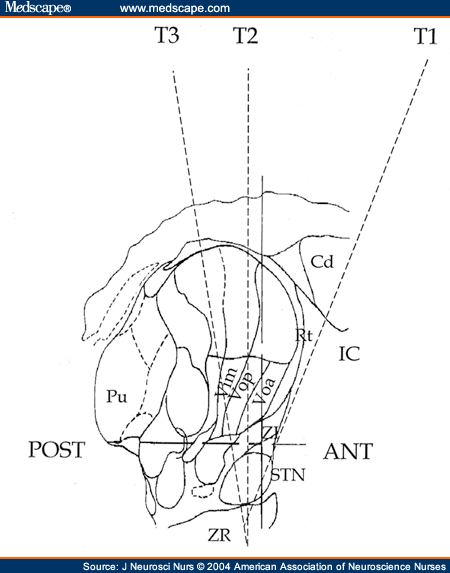
Estimulação de alta frequência do núcleo subtalâmico para o tratamento da doença de Parkinson - uma perspectiva de equipe
Wednesday, February 17, 2021 - Resumo e Introdução
A doença de Parkinson (DP) é uma doença neurodegenerativa debilitante que afeta mais de 1,2 milhão de pessoas nos Estados Unidos. Acredita-se que as toxinas genéticas e ambientais sejam fatores de risco para a aquisição da doença. A DP é caracterizada por tremores, rigidez, bradicinesia, má marcha e instabilidade postural. Esses sintomas cardinais melhoram com medicamentos como a levo-dopa (L-dopa). No entanto, com o tempo, conforme a doença progride, o paciente se torna refratário à medicação, ou a medicação produz efeitos colaterais debilitantes. Quando isso ocorre ou quando há piora dos sintomas, o tratamento neurocirúrgico é recomendado, principalmente eletrodos de estimulação cerebral profunda (DBS) implantados no núcleo subcortical subtalâmico (STN). Nos últimos 5 anos, o STN DBS ganhou aceitação e se tornou o tratamento neurocirúrgico de escolha para DP. Para alcançar o máximo de efeitos benéficos com o mínimo de efeitos adversos da cirurgia, a experiência de uma equipe integrada de médicos e enfermeiras é essencial. Uma compreensão clara dos diferentes aspectos do procedimento, incluindo os riscos e benefícios do tratamento, ajuda os enfermeiros neurocientíficos a se comunicarem com o paciente em DP e a fornecer os cuidados pré e pós-operatórios mais adequados e baseados no conhecimento.
A doença de Parkinson (DP) é uma doença neurodegenerativa que afeta mais de 1,2 milhão de pessoas nos Estados Unidos. A maioria dos pacientes tem mais de 50 anos, mas 10% têm menos de 50 anos. A etiologia da DP é multifatorial com fatores genéticos e ambientais combinados para reduzir os níveis de dopamina nos gânglios da base (Baldereschi et al., 2003; Gasser, 2001; Scott et al. ., 2001; Tsang & Soong, 2003). A doença é caracterizada por tremores, rigidez, bradicinesia, instabilidade postural e dificuldade de marcha. Alguns desses sintomas cardinais podem ser melhorados com medicamentos como a levo-dopa (L-dopa). No entanto, conforme a doença progride, o medicamento se torna menos eficaz ou produz efeitos colaterais debilitantes. O fracasso da terapia médica em fornecer alívio duradouro dos sintomas, junto com a melhora na neuroimagem e na técnica estereotáxica neurocirúrgica, levou ao ressurgimento das abordagens cirúrgicas para o tratamento da DP. Um tratamento neurocirúrgico para DP envolve a estimulação de alta frequência do núcleo subtalâmico (STN). Isso é conseguido através de um eletrodo de estimulação cerebral profunda (DBS) implantado no STN, uma pequena estrutura (10 x 10,7 x 7 mm; Bejjani et al., 2000) enterrada profundamente no subcórtex.
Este procedimento neurocirúrgico está ganhando aceitação cada vez maior. Melhora significativa nos sintomas motores é relatada, bem como uma redução significativa na medicação dopaminérgica com uma conseqüente melhora ou eliminação das discinesias induzidas por L-dopainda (Krack et al., 2003). Como esse procedimento reversível e com boa relação custo-benefício se torna o tratamento neurocirúrgico padrão de escolha para DP, os enfermeiros desempenham um papel fundamental no gerenciamento dos cuidados pré e pós-operatórios de pacientes em DP.
Este artigo revisa os aspectos pré-operatórios e pós-operatórios imediatos do STN DBS e relata nossas experiências com essa técnica. Setenta e oito cirurgias DBS STN (ou seja, 48 bilaterais simultâneas, 22 bilaterais em estágios e 8 unilaterais) foram realizadas no Presbyterian Hospital of Dallas (PHD) sem mortalidade e sem morbidade de longo prazo. Quase todos os pacientes tiveram sua escala de avaliação de DP unificada (UPDRS) reduzida em 30% em média; o medicamento foi reduzido em 30% -60%; e quatro pacientes estão completamente sem medicação. Os efeitos de longo prazo do DBS para os sintomas motores continuam positivos, mas a progressão dos sintomas não motores, particularmente os comportamentais, continua ao longo do tempo.
O grau de benefício obtido depende criticamente de uma série de fatores, como (a) selecionar o paciente ideal, (b) cronometrar a cirurgia, (c) localizar e implantar com precisão um eletrodo DBS no local alvo, (d) programar o estimulador para aliviar os sintomas motores enquanto reduz os efeitos adversos da estimulação, e (e) fornecer cuidados pós-operatórios adequados. Por meio da otimização cuidadosa de todas essas variáveis obtidas pela interação de uma equipe composta por neurocirurgião, neurologista, neurofisiologista, anestesista, enfermeiras de centro cirúrgico, enfermeiras e enfermeiras ambulatoriais, é possível obter resultados excelentes com poucos ou nenhum efeito adverso imediato. (segue…) Original em inglês, tradução Google, revisão Hugo. Fonte: Medscape.
sábado, 13 de fevereiro de 2021
quinta-feira, 10 de dezembro de 2020
Estimulação cerebral profunda para doença de Parkinson
Dec 09, 2020 - Deep Brain Stimulation for Parkinson Disease.



:max_bytes(150000):strip_icc():format(webp)/GettyImages-1094966418-09191962922845bd86e4fc9114ff8080.jpg)