Objetivo: atualização nos dispositivos de “Deep Brain Stimulation” aplicáveis ao parkinson. Abordamos critérios de elegibilidade (devo ou não devo fazer? qual a época adequada?) e inovações como DBS adaptativo (aDBS). Atenção: a partir de maio/20 fui impedido arbitrariamente de compartilhar postagens com o facebook. Com isto este presente blog substituirá o doencadeparkinson PONTO blogspot.com, abrangendo a doença de forma geral.
quarta-feira, 8 de março de 2023
O caminho para o tratamento da doença de Parkinson começa no intestino
segunda-feira, 6 de março de 2023
segunda-feira, 13 de fevereiro de 2023
O eixo microbioma-intestino-cérebro na doença de Parkinson
130223 - Evidências têm se acumulado nos últimos anos para uma relação bidirecional entre o cérebro e o intestino que desempenha um papel importante na doença de Parkinson (DP). Pesquisas recentes sugerem que o microbioma intestinal desempenha um papel fundamental nessa relação e que o eixo microbioma-intestino-cérebro pode influenciar os mecanismos fisiopatológicos envolvidos no risco e progressão da DP.1
Nas últimas duas décadas, o papel significativo dos
processos relacionados ao intestino no desenvolvimento e progressão
da DP tornou-se cada vez mais evidente.2,3 O envolvimento do sistema
gastrointestinal na DP foi reconhecido há mais de 200 anos por James
Parkinson em seu ensaio seminal sobre a 'Paralisia Agitante', onde
descreveu sintomas de constipação e um “estado desordenado do
estômago e intestinos”.4 Hoje, sabemos que a DP dá origem a uma
série de sintomas gastrointestinais e manifestações clínicas e
que estes podem preceder o início dos sintomas motores em
décadas.5,6 A constipação é uma característica prodrômica
clássica da DP e, além disso, parece predizer uma pior trajetória
da doença.6-8 A síndrome do intestino irritável é comum em
pacientes com DP e pessoas com doença inflamatória intestinal têm
um risco maior de DP do que aqueles sem.9 Vários fatores dietéticos
também foram associados ao aumento ou diminuição do risco de DP,
que, pelo menos em alguns casos, pode ser mediado pelo intestino.1
O
início e a gravidade da disfunção gastrointestinal variam entre os
pacientes, mas quase todos os pacientes com DP acabarão
experimentando pelo menos um sintoma gastrointestinal.5
Quase
todos os pacientes com DP acabarão experimentando pelo menos um
sintoma gastrointestinal.5
O eixo intestino-cérebro é uma
estrada para a comunicação intestino-cérebro
O interesse na
comunicação intestino-cérebro na DP foi despertado por estudos de
Braak e colegas em 2006, que demonstraram agregados de
alfa-sinucleína (uma marca patológica da DP) no cérebro e no
sistema nervoso entérico de indivíduos autopsiados com DP, levando
os autores a levantam a hipótese de que a DP pode começar no
intestino, possivelmente por meio de um patógeno capaz de passar
pelo revestimento epitelial gástrico.10
Desde então, estudos
em modelos animais demonstraram que a alfa-sinucleína pode de fato
se espalhar do trato gastrointestinal para o cérebro, bem como do
cérebro para o trato gastrointestinal através do nervo vago.11-13 A
comunicação bidirecional entre o sistema nervoso central e entérico
tem tornou-se conhecido como o eixo intestino-cérebro. Os principais
atores neste fluxo de informações foram propostos para incluir
inflamação intestinal (e sua associação com doenças
inflamatórias intestinais e o gene LRRK), hiperpermeabilidade
intestinal ('intestino permeável'), semeadura e propagação de
alfa-sinucleína no sistema nervoso entérico, e, mais recentemente,
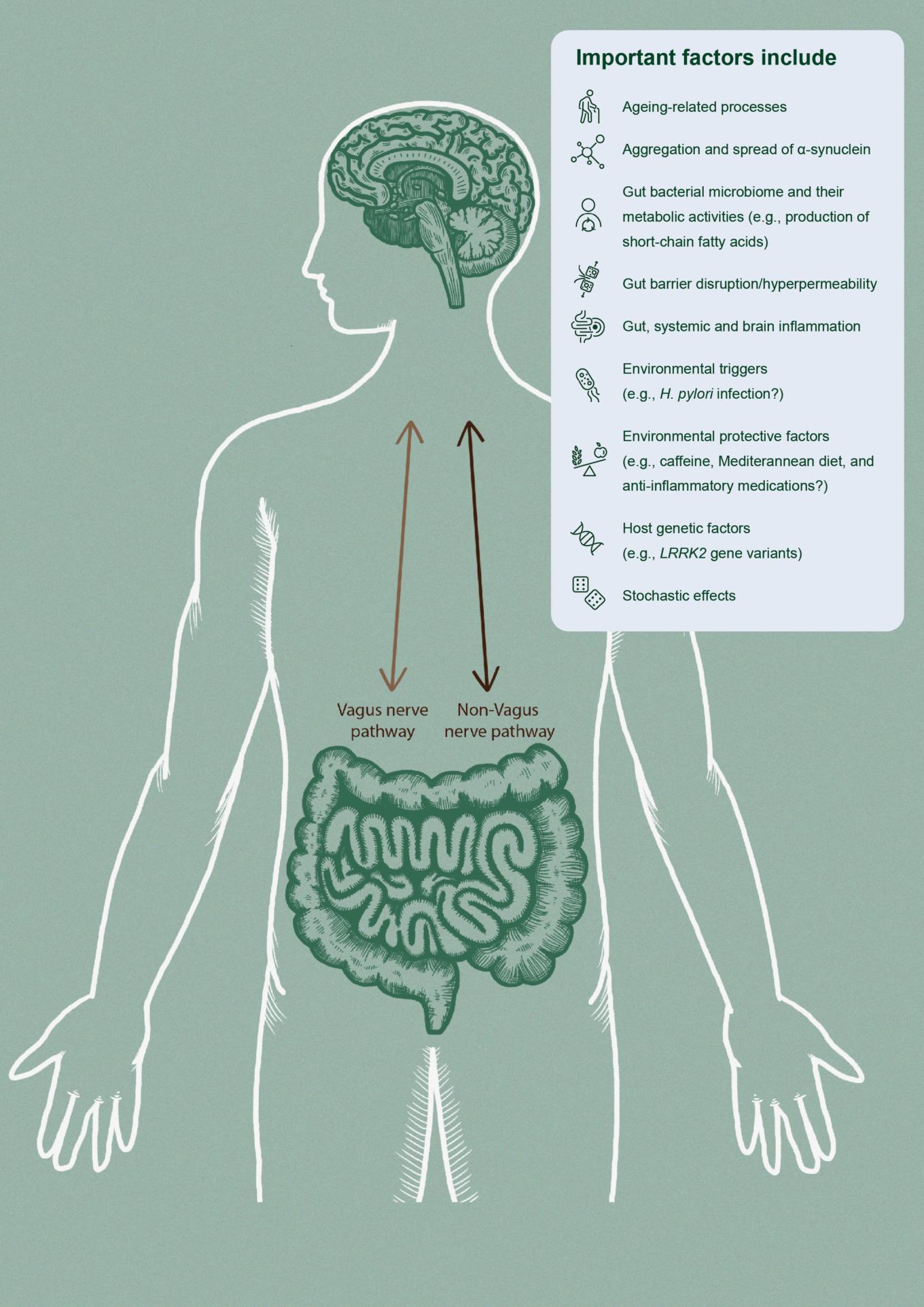
o microbioma intestinal (Figura 1).1,11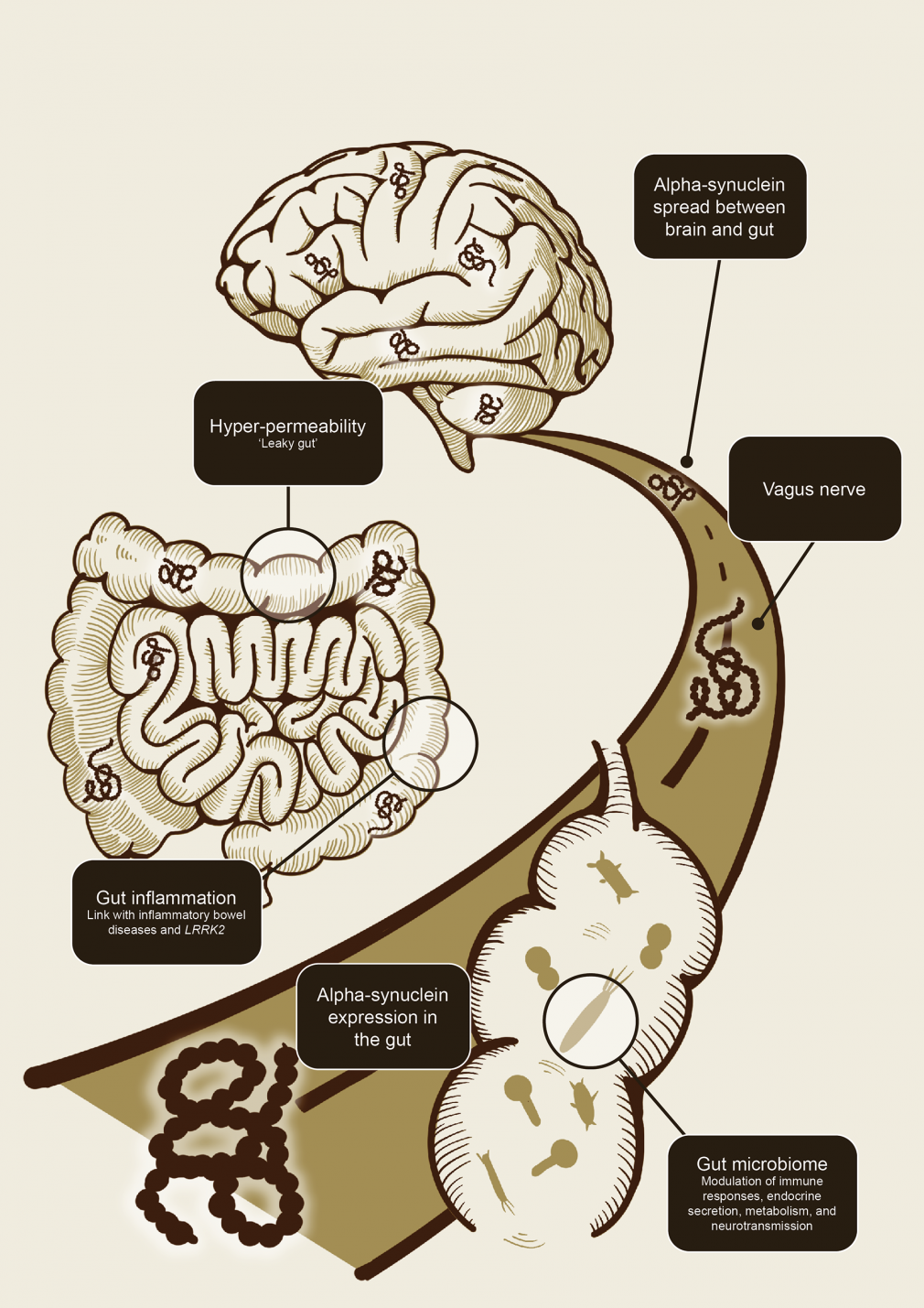 O eixo intestino-cérebro permite um fluxo bidirecional de informações entre o intestino e o cérebro.1,11-13
O eixo intestino-cérebro permite um fluxo bidirecional de informações entre o intestino e o cérebro.1,11-13
O eixo
microbioma-intestino-cérebro
Figura 1. Ilustração esquemática
de como o eixo intestino-cérebro pode contribuir para a disseminação
da patologia alfa-sinucleína (adaptado de Breen et al 2019). Foi
proposto que a inflamação intestinal e a hiperpermeabilidade e
alterações no microbioma intestinal estão associadas…
A
alfa-sinucleína, a inflamação intestinal e a permeabilidade
intestinal são elementos-chave no eixo intestino-cérebro
Tem
sido levantada a hipótese de que agregados mal dobrados de
alfa-sinucleína que se originam no sistema nervoso entérico viajam
para o cérebro via transferência transsináptica de célula a
célula semelhante a príon, embora o modo de transferência, bem
como a origem de alfa-sinucleína ainda não estão claros.11,14 Se a
DP começa no cérebro ou se começa no intestino, ou se há
fenótipos da doença tanto no intestino quanto no cérebro, é uma
área sob investigação ativa.6,15 -17
Se a DP começa no
cérebro ou se começa no intestino permanece
indeterminado.6,15-17
Em outros estudos, foi demonstrado que a
permeabilidade intestinal alterada ("intestino permeável")
e a inflamação intestinal também desempenham um papel na patologia
da DP em subconjuntos de pacientes.1,18,19
Curiosamente, alguns tipos de infecções (e subsequente inflamação da parede intestinal) mostraram induzir a expressão de alfa-sinucleína no trato gastrointestinal, o que levou à hipótese de que a expressão de alfa-sinucleína pode ser um mecanismo de defesa imune.11 Pro-sinucleína crônica. a atividade imune inflamatória é cada vez mais reconhecida como um elemento fundamental dos distúrbios neurogenerativos, incluindo a DP.19 O reconhecimento de uma conexão entre inflamação e DP foi reforçado por estudos observacionais que demonstram fortes ligações entre DP e doenças inflamatórias intestinais.18,20 Em estudos epidemiológicos e genéticos estudos, descobriu-se que pessoas com doença inflamatória intestinal tinham até 40% mais chances de desenvolver DP em comparação com aqueles sem doença inflamatória intestinal, com LRRK2 emergindo como um gene de suscetibilidade comum para ambas as doenças.18,20
O
microbioma intestinal e seu efeito na saúde do hospedeiro
Uma das
descobertas mais intrigantes relacionadas a esse campo é o papel do
microbioma intestinal na DP. Uma enorme comunidade microbiana
conhecida como microbiota reside sobre e dentro do corpo humano. Este
ecossistema invisível de micróbios está localizado em superfícies
externas e internas, como a pele, a cavidade oral e, particularmente,
dentro do trato gastrointestinal.21,22 O microbioma intestinal é
composto principalmente por bactérias, mas também inclui fungos,
vírus e protozoários , bem como seus genomas coletivos e o ambiente
que habitam.23 Esses micróbios agem como um vasto ecossistema
complexo no qual cada espécie tem o potencial de exercer diversos
efeitos sobre as espécies vizinhas.24 As estimativas mais recentes
sugerem que, para a pessoa média , células bacterianas e humanas
estão presentes em números aproximadamente iguais.25 Em uma pessoa
de referência de 70 kg, isso equivale a 38 trilhões de bactérias,
com uma massa total de cerca de 0,2 kg, a grande maioria das quais é
encontrada no intestino, particularmente no cólon .21,25
Os
microorganismos intestinais evoluíram ao longo de milhares de anos
para formar uma notável relação simbiótica com seus hospedeiros.
Em troca de alimentos por meio da ingestão dietética, os micróbios
fornecem uma variedade de funções imunológicas, digestivas e
nutricionais que são benéficas para o hospedeiro.26,27 O microbioma
e seu consórcio de genes podem ser considerados uma extensão do
repertório genético do hospedeiro para formam o que alguns agora
chamam de 'genótipo estendido'.28 Através da modificação de seu
fenótipo hospedeiro, isso pode significar que o microbioma ainda tem
o potencial de modificar a evolução humana.28
O microbioma
não é estático; é uma comunidade dinâmica que muda ao longo da
vida à medida que os indivíduos envelhecem.29,30 Diferenças
consideráveis na composição, abundância e função da microbiota
intestinal foram observadas entre indivíduos jovens e idosos em
estudos clínicos, muitas vezes demonstrando uma diminuição em
Bifidobacterium e Lactobacillus e um aumento de
Enterobacteriaceae.30,31 Essas alterações no microbioma estão
associadas a fatores como afinamento da mucosa, senescência
imunológica, mudanças na dieta e atividade física, medicamentos e
estado de saúde que ocorrem à medida que os indivíduos
envelhecem.1,32 Isso fenômeno levou à ideia de que mudanças
relacionadas à idade no microbioma intestinal podem estar associadas
à predisposição de pessoas idosas a certas doenças.31,33
Mudanças
no microbioma podem estar associadas à predisposição a certas
doenças.1,31,33
O microbioma pode ser alterado por vários
fatores, como dieta, genética, exposições ambientais, estado de
saúde e medicamentos.1 Os microrganismos intestinais também
interagem com o hospedeiro por meio de toxinas, subprodutos e
metabólitos secretados para modular as respostas imunes, secreção
endócrina, metabolismo , e neurotransmissão.34 As alterações do
microbioma podem resultar em uma mudança para uma superabundância
de bactérias associadas a um estado "não saudável" ou
patológico. Esse tipo de alteração no microbioma é geralmente
denominado disbiose e tem sido associado a uma variedade de doenças
metabólicas, gastrointestinais e neurológicas, incluindo
DP.1,20,30,31,35-37
Um papel para o microbioma intestinal na DP
Numerosos estudos examinaram o
microbioma intestinal de pacientes com DP e descobriram que ele
estava alterado em comparação com controles saudáveis.38-41 Em uma
recente análise metagenômica em larga escala do microbioma
intestinal de 490 pacientes com DP, mais de 30% dos espécies
microbianas, genes e vias testadas demonstraram alterações em
comparação com controles sem DP, retratando disbiose
generalizada.42 Tentativas de identificar os microrganismos precisos
associados à DP produziram resultados inconsistentes. No nível de
gênero, meta-análises mostraram que a abundância relativa de
bactérias anti-inflamatórias e produtoras de ácidos graxos de
cadeia curta (incluindo Blautia, Coprococcus, Roseburia, Lachnospira
e Faecalibacterium) é reduzida em pacientes com DP em comparação
com controles, enquanto os níveis de Lactobacillus, Bifidobacterium
e Akkermansia são criados. Patógenos oportunistas e bactérias
pró-inflamatórias (incluindo Alistipes, Escherichia, Bacteroides
Corynebacterium e Porphyromonas) também são enriquecidos em
pacientes com DP.34,36,43,44 Ainda não está claro se as alterações
observadas no microbioma de pacientes com DP são a ocorrência
inicial que contribui para o desenvolvimento da doença, ou se as
alterações surgem em resposta à patologia da DP; ambos são uma
possibilidade.19
Curiosamente, vários distúrbios intestinais
(incluindo infecções, disbiose, inflamação e dismotilidade), bem
como fatores dietéticos, mostraram influenciar a resposta à
medicação para DP.1 A terapêutica dirigida a micróbios está se
mostrando promissora no tratamento da DP. Estudos piloto de pequeno e
curto prazo mostraram melhorias nos sintomas motores e não motores,
como constipação e biodisponibilidade de levodopa, com intervenções
dietéticas e suplementação com probióticos/prebióticos.1 Outras
modalidades potencialmente úteis sendo testadas incluem transplante
de microbiota fecal e pequenas moléculas drogas, produtos biológicos
e metabólitos que atuam em alvos relacionados ao intestino.1
Estratégias direcionadas a patologias de DP (como agregação de
alfa-sinucleína) no sistema nervoso entérico também estão em
desenvolvimento e recentemente demonstraram sucesso em ensaios
clínicos envolvendo pacientes com DP.1,45 ,46 Em última análise,
espera-se que os avanços científicos neste campo se traduzam no uso
responsável de novas abordagens diagnósticas, prognósticas e
terapêuticas que melhorem a vida dos pacientes que vivem com DP.
Original em inglês, tradução Google, revisão Hugo. Fonte:
Neurotorium.
quinta-feira, 26 de janeiro de 2023
Grant: A terapia com microbioma pode interromper a doença de Parkinson?
A professora associada Marina Romero-Ramos, do Departamento de Biomedicina e DANDRITE, recebeu DKK 5 milhões pelo programa colaborativo da Fundação Novo Nordisk. Juntamente com a Universidade Técnica da Dinamarca, ela pode criar novos insights sobre as conexões entre a doença de Parkinson e a terapia do microbioma no intestino.
No projeto, que a Fundação Novo Nordisk está apoiando com DKK 5 milhões, os pesquisadores investigarão se o potencial anti-inflamatório e neuroprotetor da terapia avançada de microbioma pode interromper o desenvolvimento da doença. Eles farão isso combinando o conhecimento de biologia sintética e pesquisa de microbioma do laboratório de Morten O. Sommer com o profundo conhecimento dos aspectos imunológicos e neurológicos da doença de Parkinson que possui o laboratório de Marina Romero-Ramos.
Os resultados do projeto ajudarão a consolidar a terapia avançada de microbioma como uma nova abordagem no tratamento da doença de Parkinson. Original em inglês, tradução Google, revisão Hugo. Fonte: Biomed.
quarta-feira, 18 de janeiro de 2023
segunda-feira, 9 de janeiro de 2023
Bactérias intestinais inflamatórias e genes podem ser biomarcadores de Parkinson
Estudo sugere que pessoas em diferentes regiões podem compartilhar características comuns de microbioma
January 9, 2023 -Certas
bactérias intestinais pró-inflamatórias, genes e vias são
significativamente aumentadas em pessoas com doença de Parkinson em
comparação com pessoas saudáveis, enquanto as anti-inflamatórias
são significativamente reduzidas, segundo um grande estudo.
Além
disso, modelos de aprendizado de máquina baseados em 11 dessas
bactérias e seis desses genes discriminaram com precisão pessoas
com e sem Parkinson, sugerindo ainda que esses fatores possam servir
como potenciais biomarcadores da doença neurodegenerativa.
“Nossos
resultados forneceram mais informações sobre a previsão e
tratamento da DP [doença de Parkinson] com base na inflamação”,
escreveram os pesquisadores sobre seu estudo, “Micróbios
inflamatórios e genes como potenciais biomarcadores da doença de
Parkinson”, publicado em Biofilms and Microbiomes.
A
microbiota intestinal refere-se à vasta comunidade de bactérias
amigáveis, fungos e vírus que colonizam o trato gastrointestinal.
Embora essa comunidade ajude a manter uma função intestinal
equilibrada, o desequilíbrio da microbiota intestinal ou a disbiose
intestinal podem promover inflamação e desencadear ou piorar certas
condições de saúde. Sugere-se que esse desequilíbrio semeia o
intestino com aglomerados tóxicos da proteína alfa-sinucleína
antes que eles migrem para o cérebro, onde contribuem para a
neurodegeneração, uma característica do Parkinson.
A
evidência de uma conversa cruzada entre o intestino e o cérebro
através do chamado eixo intestino-cérebro está colocando a
microbiota intestinal no centro das muitas causas possíveis por trás
do Parkinson.
Pesquisadores na China levantaram a hipótese de
que pessoas com Parkinson “em diferentes países e regiões
compartilham características microbianas e metabólicas comuns”,
escreveram eles. Para testar sua hipótese, eles se basearam em dados
de pessoas em sete países.
Nove conjuntos de dados contendo
2.269 amostras (1.373 de pacientes com Parkinson e 896 de pessoas
saudáveis) foram analisados com sequenciamento 16S rRNA, uma técnica
que permite a identificação de espécies microbianas.
Além
disso, dois outros conjuntos de dados de 236 amostras (122 de
pacientes com Parkinson e 114 de pessoas saudáveis) foram avaliados
por meio do sequenciamento metagenômico shotgun, que permite o
estudo de todos os genes em todos os organismos presentes em uma
determinada amostra complexa.
Microbioma intestinal de gêmeos
com Parkinson e saudáveis é amplamente semelhante
Diferenças
entre Parkinson e bactérias intestinais saudáveis
Os resultados
mostraram que a abundância relativa de 23 grupos diferentes
(gêneros) de bactérias diferiu significativamente entre pessoas
saudáveis e aquelas com Parkinson.
Entre eles, havia cinco
gêneros de potenciais bactérias pró-inflamatórias (Streptococcus,
Bifidobacterium, Lactobacillus, Akkermansia e Desulfovibrio) que eram
significativamente mais abundantes em amostras de Parkinson em todos
os países do que em pessoas saudáveis.
Cinco outros gêneros
de bactérias (Roseburia, Faecalibacterium, Blautia, Lachnospira e
Prevotella), que são relatados como potenciais anti-inflamatórios,
foram significativamente menos abundantes nas amostras de
Parkinson.
Um estudo anterior encontrou um desequilíbrio
semelhante no microbioma intestinal de pessoas com Parkinson.
Ao
comparar a estrutura da rede da microbiota intestinal entre pessoas
com e sem Parkinson, os pesquisadores descobriram que o Prevotella
estava presente apenas na rede de pessoas saudáveis.
“Portanto,
as vias metabólicas relacionadas ao metabolismo inflamatório e os
[10] possíveis gêneros relacionados à inflamação mencionados
acima foram analisados posteriormente”, escreveram eles.
Os
pesquisadores se concentraram em genes envolvidos em quatro vias
metabólicas associadas à inflamação intestinal: ácidos graxos de
cadeia curta (SCFAs), que possuem propriedades anti-inflamatórias, e
lipopolissacarídeos, sulfeto de hidrogênio e glutamato – três
tipos de moléculas inflamatórias anteriormente ligadas ao
Parkinson.
Um total de 63 desses genes mostrou diferenças
significativas em sua atividade entre pessoas com e sem Parkinson.
Entre eles, 19 genes relacionados às vias de ácidos graxos de
cadeia curta foram sintonizados em pessoas com Parkinson versus
pessoas saudáveis. Todos os 26 genes relacionados às vias de
lipopolissacarídeo, sulfeto de hidrogênio e glutamato foram mais
ativos com Parkinson.
“Além disso, a via dos SCFAs diminuiu
significativamente, enquanto as vias do metabolismo [do sulfeto de
hidrogênio], do lipopolissacarídeo e do glutamato aumentaram na
DP”, escreveram os pesquisadores.
Os pesquisadores
levantaram a hipótese de que as mudanças observadas nas bactérias
intestinais “podem levar a uma diminuição de fatores
anti-inflamatórios (como SCFAs) e um aumento de fatores
pró-inflamatórios (como lipopolissacarídeo, [sulfeto de
hidrogênio] e glutamato), causando inflamação intestinal e danos à
barreira intestinal”.
Efeitos das alterações nas bactérias intestinais
Os defeitos da barreira intestinal
podem permitir o vazamento de micróbios e seus produtos no corpo,
promovendo a produção de moléculas inflamatórias e aglomerados
tóxicos de alfa-sinucleína, que por sua vez podem afetar a barreira
protetora natural do cérebro.
“Essas substâncias podem
atingir o cérebro através do nervo vago ou do sistema humoral e,
eventualmente, causar o mal de Parkinson”, escreveram os
pesquisadores, acrescentando que “a inflamação pode ser um futuro
alvo terapêutico” para a doença. O nervo vago é o nervo mais
longo que conecta o cérebro aos órgãos internos. O sistema humoral
refere-se aos fluidos corporais.
Os pesquisadores usaram o
aprendizado de máquina para desenvolver maneiras de prever quem pode
ter um diagnóstico de Parkinson. O aprendizado de máquina é uma
forma de inteligência artificial que usa algoritmos para analisar
dados, aprender com suas análises e, em seguida, fazer uma previsão
sobre algo.
Um modelo de aprendizado de máquina baseado em 11
gêneros bacterianos relacionados à inflamação foi capaz de
distinguir pacientes com Parkinson daqueles sem a doença com uma
precisão superior a 80%. Outro modelo, baseado em seis genes
relacionados à inflamação, identificou o Parkinson com uma
precisão superior a 90%.
“Este estudo é a maior
meta-análise do microbioma intestinal em [Parkinson] até o momento,
que forneceu pela primeira vez uma análise integrativa do gene 16S
rRNA e dados metagenômicos shotgun em [Parkinson] e uma exploração
detalhada de como as alterações no intestino composição
bacteriana e função afetam [Parkinson]”, escreveram os
pesquisadores. Original em inglês, tradução Google, revisão Hugo.
Fonte: Parkinsonsnewstoday.
terça-feira, 27 de dezembro de 2022
Os efeitos da abundância da microbiota na gravidade dos sintomas na doença de Parkinson: uma revisão sistemática
2022 Dec 8 - Resumo
Introdução: A doença de Parkinson (DP) é uma doença neurodegenerativa com uma etiopatogenia multifatorial com evidências acumuladas identificando a microbiota como um fator potencial nas fases prodrômicas iniciais da doença. Pesquisas anteriores já mostraram uma diferença significativa entre a composição da microbiota intestinal em pacientes com DP em oposição a controles saudáveis, com um número crescente de estudos correlacionando as alterações da microbiota intestinal com a apresentação clínica da doença em estágios posteriores, por meio de vários sintomas motores e não motores. Nosso objetivo nesta revisão sistemática é compor e avaliar o conhecimento atual no campo e determinar se os achados podem influenciar a prática clínica futura, bem como a terapia na DP.
Métodos: Conduzimos uma revisão sistemática de acordo com as diretrizes PRISMA por meio dos bancos de dados MEDLINE e Embase, com estudos sendo selecionados para inclusão por meio de um conjunto de critérios de inclusão e exclusão.
Resultados: 20 estudos foram incluídos nesta revisão sistemática de acordo com os critérios de inclusão e exclusão selecionados. A pesquisa resultou em 18 estudos de caso-controle, 1 estudo de caso e 1 estudo de caso prospectivo sem controles. O número total de pacientes com DP incluídos nos estudos citados nesta revisão é de 1.511.
Conclusão: A ligação entre a microbiota intestinal e a neurodegeneração é complexa e depende de vários fatores. A abundância relativa de vários táxons da microbiota no intestino mostrou consistentemente uma correlação com a gravidade dos sintomas motores e não motores. A resposta pode estar nos produtos do metabolismo da microbiota intestinal, que também foram associados à DP. Portanto, mais pesquisas são necessárias no campo, com foco na função metabólica da microbiota intestinal em relação aos sintomas motores e não motores. Original em inglês, tradução Google, revisão Hugo. Fonte: Pubmed.
segunda-feira, 26 de dezembro de 2022
INTESTINAL INFLAMATÓRIO COMO ALVO PATOLÓGICO E TERAPÊUTICO NA DOENÇA DE PARKINSON
24 September 2022 - Resumo
A doença de Parkinson (DP) continua sendo uma necessidade clínica significativa não atendida. A disbiose intestinal é uma fonte patológica e alvo terapêutico da DP. Aqui, avaliamos o papel do eixo intestino-cérebro na patologia e tratamento da DP. Camundongos adultos transgênicos (Tg) com superexpressão de α-sinucleína serviram como sujeitos e foram designados aleatoriamente para transplante de veículo ou células-tronco derivadas do sangue do cordão umbilical humano e plasma. Ensaios comportamentais e imuno-histoquímicos avaliaram os resultados funcionais após o transplante. Camundongos Tg exibiram déficits típicos de motilidade motora e intestinal, níveis elevados de α-sinucleína e depleção dopaminérgica, acompanhados por disbiose intestinal caracterizada por regulação positiva da microbiota e citocinas associadas à inflamação no intestino e no cérebro. Em contraste, os camundongos Tg transplantados apresentaram melhora dos déficits motores, melhor preservação dos neurônios dopaminérgicos nigrais e regulação negativa da α-sinucleína e da microbiota e citocinas relevantes para a inflamação no intestino e no cérebro. Estudos in vitro paralelos revelaram que células SH-SY5Y dopaminérgicas cultivadas expostas a homogenatos de intestino disbiótico derivado de camundongo Tg exibiram viabilidade celular significativamente reduzida e sinais inflamatórios elevados em comparação com homogenatos intestinais derivados de camundongos de tipo selvagem. Além disso, o tratamento com células-tronco derivadas do sangue do cordão umbilical humano e plasma melhorou a viabilidade celular e diminuiu a inflamação em células SH-SY5Y expostas ao intestino disbiótico. O transplante intravenoso de células-tronco/progenitoras derivadas do sangue do cordão umbilical humano e plasma reduziu a microbiota inflamatória e a citocina, e amorteceu a sobrecarga de α-sinucleína no intestino e no cérebro de camundongos Tg adultos com superexpressão de α-sinucleína. Nossas descobertas avançam o eixo intestino-cérebro como uma origem patológica chave, bem como um alvo terapêutico robusto para a DP. (segue...) Original em inglês, tradução Google, revisão Hugo. Fonte: Nature.
quarta-feira, 16 de novembro de 2022
sexta-feira, 21 de outubro de 2022
Alterações histomorfológicas e moleculares intestinais em pacientes com doença de Parkinson
2022 Oct 20 - Resumo
Introdução: Alterações na
composição da microbiota intestinal, inflamação entérica,
deficiências da barreira epitelial intestinal (BEI) e do sistema
neuroimune entérico têm sido relatadas em pacientes com doença de
Parkinson (DP) e podem contribuir para o aparecimento de sintomas
neurológicos e gastrointestinais. No entanto, sua interação mútua
raramente foi investigada. Este estudo avaliou, de forma integrada,
alterações na composição da microbiota fecal, alterações
morfofuncionais da barreira da mucosa colônica e alterações de
marcadores inflamatórios no sangue e nas fezes de pacientes com
DP.
Métodos: 19 pacientes com DP e 19 indivíduos
assintomáticos foram incluídos. Foram avaliados os níveis de
proteína ligante de lipopolissacarídeos sanguíneos (LBP, marcador
de permeabilidade intestinal alterada) e interleucina-1β (IL-1β),
bem como IL-1β fecal e fator de necrose tumoral (TNF). A análise da
microbiota intestinal foi realizada. Mucinas epiteliais, fibras de
colágeno, células gliais positivas para Claudin-1 e S-100 como
marcadores de comprometimento da barreira intestinal e remodelação
da mucosa foram avaliadas em amostras de mucosa colônica coletadas
durante a colonoscopia.
Resultados: A análise da microbiota
fecal revelou uma diferença significativa na diversidade α em
pacientes com DP em comparação com os controles, enquanto não
foram encontradas diferenças na diversidade beta. Comparados aos
controles, os pacientes com DP apresentaram um aumento significativo
na lombalgia plasmática, bem como nos níveis fecais de TNF e IL-1β.
A análise histológica mostrou diminuição da expressão de mucinas
epiteliais neutras e claudina-1, e aumento da expressão de mucinas
ácidas, fibras colágenas e células gliais S-100
positivas.
Conclusões: Os pacientes com DP são
caracterizados por inflamação intestinal e aumento da
permeabilidade do BEI, além de remodelação da barreira da mucosa
colônica, associada a alterações na composição da microbiota
intestinal. Original em inglês, tradução Google, revisão Hugo.
Fonte: Pub Med.
segunda-feira, 3 de outubro de 2022
Terapia modificadora da doença orientada para o intestino para a doença de Parkinson
2022 Sep 28 - Resumo
Estudos de neuropatologia mostraram que a característica patognomônica da doença de Parkinson (DP), um dos distúrbios neurodegenerativos mais comuns, pode começar no sistema nervoso entérico intestinal e depois se espalhar para os neurônios dopaminérgicos centrais através do eixo intestino-cérebro. Com o advento do sequenciamento metagenômico e da análise metabolômica, uma infinidade de evidências revelou diferentes microbiomas intestinais e metabólitos intestinais em pacientes com DP em comparação com controles não afetados. Atualmente, embora os tratamentos dopaminérgicos e a estimulação cerebral profunda possam fornecer alguns benefícios sintomáticos para os sintomas motores da doença, seu uso a longo prazo é problemático. Falta uma terapia direcionada ao mecanismo para interromper a neurodegeneração. As alterações microambientais intestinais recentemente observadas nos estágios iniciais da doença desempenham um papel vital na patogênese da DP. Os pacientes cuja doença começa no intestino podem se beneficiar mais de intervenções que visam os microambientes intestinais. Nesta revisão, resumiremos os estudos atuais que demonstram os papéis multifuncionais da microbiota intestinal no eixo intestino-cérebro da DP e as evidências atualmente disponíveis para direcionar a microbiota intestinal como uma nova abordagem para potencial terapia modificadora da doença na DP. Original em inglês, tradução Google, revisão Hugo. Fonte: Pubmed.
quarta-feira, 31 de agosto de 2022
Intercâmbio de pesquisa alemão para beneficiar a pesquisa de Parkinson
30 August 2022 - Uma estudante de doutorado em Aberdeen recebeu mais de £ 8.000 para permitir uma visita de intercâmbio de pesquisa que aprofundará sua pesquisa sobre a doença de Parkinson (DP).
Inga
Schmidt, membro de pós-graduação dos grupos de pesquisa da
professora Bettina Platt e do professor Gernot Riedel, visitará o
grupo de pesquisa Schäfer na Universidade de Ciências Aplicadas
Kaiserslautern (UASK) em Zweibrücken, enquanto Stephanie Rommel,
estudante da UASK, visitará Aberdeen como parte do arranjo.
O
projeto de Inga se concentra nos mecanismos de gravidade da doença,
enquanto Stephanie estuda o papel do intestino na doença de
Parkinson.
Os grupos de pesquisa correspondentes em cada
universidade têm uma ampla experiência na pesquisa de distúrbios
neurodegenerativos, como a doença de Alzheimer e a doença de
Parkinson. A pesquisa do grupo Platt/Riedel em Aberdeen se concentra
no cérebro, enquanto o grupo Schäfer na UASK se concentra no papel
do intestino nessas doenças. Portanto, o projeto proposto permitirá
que as duas equipes estudem modelos da doença a partir de dois
ângulos diferentes, mas complementares, e entendam melhor como o
chamado eixo intestino-cérebro contribui para o início e a
progressão da doença.
Estou muito satisfeito por ter
garantido este prêmio, que não apenas me beneficiará como
pesquisador em início de carreira, mas também os dois grupos de
pesquisa em Aberdeen e Zweibrücken, que poderão combinar seus
conhecimentos para contribuir para um estudo mais abrangente da
doença de Parkinson ."
O principal objetivo deste prêmio
é oferecer aos pesquisadores em início de carreira experiência em
outros laboratórios e aprender novas técnicas adicionais que podem
ser úteis para sua carreira. Além disso, a visita pode estabelecer
a base para uma nova colaboração formal entre as duas instituições
e o compartilhamento de dados, conhecimentos, técnicas e
recursos.
O financiamento para o prêmio é resultado de uma
receita fiscal extra no estado alemão de Rheinland-Pfalz gerada pela
BioNTech - a start-up que trabalhou com a Pfizer em uma das
principais vacinas contra a Covid. O prêmio foi criado com o
objetivo de reinvestir esse sucesso de pesquisa em novos progressos
científicos.
Inga disse: “Estou muito feliz por ter
garantido este prêmio, que não só me beneficiará como pesquisador
em início de carreira, mas também os dois grupos de pesquisa em
Aberdeen e Zweibrücken, que poderão combinar seus conhecimentos
para contribuir para um estudo abrangente da doença de
Parkinson”.
A professora Bettina Platt acrescentou: "Esta
é uma oportunidade bem-vinda para ECRs e ampliação de nossa rede
de pesquisa em geral, mas também para mim pessoalmente, pois posso
reconectar minha atual casa e local de trabalho com Rheinland-Pfalz -
o lugar onde cresci e estudei para minha graduação em Biologia na
Universidade de Mainz em 1994.” Original em inglês, tradução
Google, revisão Hugo. Fonte: Abdn.
quarta-feira, 10 de agosto de 2022
A relação entre a doença de Parkinson e as doenças gastrointestinais
10 August 2022 - The relationship between Parkinson’s disease and gastrointestinal diseases.
Um número crescente de estudos forneceu evidências para a hipótese de que a patogênese da doença de Parkinson (DP) pode derivar do intestino. Em primeiro lugar, a patologia de Lewy pode ser induzida no sistema nervoso entérico (ENS) e ser transportada para o sistema nervoso central (SNC) através do nervo vago. Em segundo lugar, a composição alterada da microbiota intestinal causa um desequilíbrio entre metabólitos microbianos benéficos e deletérios que interagem com o aumento da permeabilidade intestinal e a inflamação intestinal, bem como a inflamação sistêmica. O estado inflamatório ativado então afeta o SNC e promove a patologia da DP. Diante dos achados acima mencionados, os pesquisadores começam a prestar atenção à conexão entre DP e doenças gastrointestinais, incluindo síndrome do intestino irritável, doença inflamatória intestinal (DII), colite microscópica (MC), infecções gastrointestinais, neoplasias gastrointestinais e doença diverticular do cólon (CDD). ). Esta revisão enfoca a associação entre DP e doenças gastrointestinais, bem como a patogênese da DP no intestino.
Introdução
A doença de Parkinson (DP) é a segunda doença neurodegenerativa progressiva mais prevalente após a doença de Alzheimer. A incidência de DP, aumentando com a idade, é mais alta em pessoas com cerca de 80 anos (Ascherio e Schwarzschild, 2016). A DP apresenta os sintomas motores clássicos de tremor de repouso, rigidez muscular, bradicinesia e comprometimento postural e de marcha (Cacabelos, 2017). Sintomas não motores, incluindo olfato prejudicado, constipação, depressão, sonolência diurna excessiva e distúrbio comportamental do sono de movimento rápido dos olhos (DCR) geralmente ocorrem no período prodrômico da DP, antes do início dos sintomas motores primários. Neste período, as principais características da patologia da DP já podem ser identificadas (Klingelhoefer e Reichmann, 2015). As características patológicas da DP são a perda de neurônios dopaminérgicos na substância negra pars compacta (SNpc), juntamente com outras partes do cérebro, e a formação de corpos de Lewy, compostos principalmente por uma proteína anormalmente dobrada chamada α-sinucleína, nos neurônios do sistema nervoso central (SNC) e sistema nervoso periférico, como o sistema nervoso entérico (ENS). Acredita-se que a patologia de Lewy se desenvolva após 6 estágios. Nos estágios iniciais antes do início dos sintomas motores, os corpos de Lewy podem ser encontrados no sistema nervoso periférico, relacionados aos sintomas não motores. Além disso, formas patológicas de agregados de α-sinucleína além dos corpos de Lewy também são prejudiciais aos neurônios (Kalia e Lang, 2015). A neuroinflamação também desempenha um papel importante na patologia da DP. A gliose reativa causada por astrócitos ativados e a microgliose resultante da ativação microglial são identificadas nas áreas de neurodegeneração na DP (Phani et al., 2012). Há um número crescente de estudos que sustentam que a patologia acima mencionada no cérebro se origina do trato gastrointestinal. Este artigo tem como objetivo revisar os papéis que o intestino desempenha na patogênese da DP e a associação entre DP e doenças gastrointestinais, bem como os possíveis mecanismos subjacentes para revelar novos insights sobre a etiologia e fisiopatologia da DP, explorar o diagnóstico periférico precoce da DP para intervenção e facilitar a identificação e o manejo oportunos de comorbidades gastrointestinais. Original em inglês, tradução Google, revisão Hugo.
quarta-feira, 20 de julho de 2022
Microbiota intestinal em gêmeos monozigóticos discordantes para a doença de Parkinson
2022 Jul 19 - Resumo - As diferenças na microbiota intestinal entre pacientes com doença de Parkinson (DP) e controles parecem depender de múltiplos fatores de confusão – frequentemente não medidos. Gêmeos monozigóticos oferecem um modelo único para controlar vários fatores responsáveis pela variação interpessoal na microbiota intestinal. Amostras fecais de 20 pares de gêmeos monozigóticos (N=40) discordantes para DP foram estudadas (análise de shotgun metagenômica). A análise de dados pareados detectou diferenças mínimas na abundância de táxons bacterianos em nível de espécie (Bacteroides pectinophilus [P=0,037], Bifidobacterium pseudocatenulatum [P=0,050] e Bifidobacterium catenulatum [P=0,025]) e nas vias metabólicas previstas (biossíntese primária de ácidos biliares [ P=0,037]). Estudos adicionais são necessários para entender o papel da microbiota intestinal na patogênese da DP. Este artigo está protegido por direitos autorais. Todos os direitos reservados. original em inglês, tradução Google, revisão Hugo. Fonte: Pubmed.
quarta-feira, 13 de julho de 2022
Nova esperança para o tratamento da doença de Parkinson: visando a microbiota intestinal
13 July 2022 - Resumo - Pode haver mais de 10 milhões de casos confirmados de doença de Parkinson (DP) em todo o mundo até 2040. No entanto, a patogênese da DP ainda não está clara. A saúde do hospedeiro está intimamente relacionada à microbiota intestinal, que é afetada por fatores como idade, dieta e exercício. Estudos recentes descobriram que a microbiota intestinal pode desempenhar papéis fundamentais na progressão de uma ampla gama de doenças, incluindo a DP. Alterações na abundância de bactérias intestinais, como Helicobacter pylori, Enterococcus faecalis e Desulfovibrio, podem estar envolvidas na patogênese da DP ou interferir na terapia da DP. A microbiota intestinal e o cérebro distal atuam um sobre o outro através de um eixo intestino-cérebro composto pelo sistema nervoso, sistema endócrino e sistema imunológico. Aqui, esta revisão se concentrou no entendimento atual da conexão entre a doença de Parkinson e a microbiota intestinal, para fornecer potenciais alvos terapêuticos para a DP. (segue..., em inglês) Fonte: Wiley.
quinta-feira, 24 de março de 2022
quinta-feira, 17 de março de 2022
Parkinson: como o desequilíbrio na flora intestinal pode favorecer o surgimento da doença
Pesquisas brasileiras explicam mecanismo e o impacto das bactérias boas e ruins no desenvolvimento do distúrbio
17/03/22 - O conflito entre as bactérias patogênicas e benéficas no intestino, pode favorecer o surgimento da doença de Parkinson.
As bactérias que vivem em nosso intestino podem influenciar no desenvolvimento e na progressão de distúrbios neurodegenerativos, mostram evidências científicas. Dois estudos brasileiros recentes comprovam essa relação e descrevem como o desequilíbrio da flora intestinal, o conflito entre as bactérias patogênicas e benéficas no intestino (processo chamado de disbiose), pode favorecer o surgimento da doença de Parkinson.
Um dos trabalhos foi conduzido por pesquisadores ligados ao Laboratório Nacional de Biociências (LNBio), que integra o complexo do Centro Nacional de Pesquisa em Energia e Materiais (CNPEM), em Campinas, e apoiado pela Fapesp. Parte dos resultados foi publicado em fevereiro, no periódico iScience. O segundo artigo foi divulgado este mês na revista Scientific Reports.
Vários trabalhos recentes relataram consistentemente a existência de disbiose intestinal em portadores de Parkinson esporádico (casos em que não há um fator genético envolvido), reportando uma maior abundância da espécie bacteriana Akkermansia muciniphila em amostras fecais desses pacientes, quando comparados ao grupo-controle. Segundo o coordenador da pesquisa brasileira, Matheus de Castro Fonseca, o diagnóstico de Parkinson costuma ocorrer tardiamente, mas é possível observar sinais do distúrbio precocemente no sistema nervoso entérico, que controla a motilidade gastrointestinal.
"Foi recentemente descrito que células específicas do epitélio intestinal, chamadas de células enteroendócrinas, possuem muitas propriedades semelhantes às dos neurônios, incluindo a expressão da proteína α-sinucleína [αSyn], cuja agregação está sabidamente relacionada com a doença de Parkinson e com outras doenças neurodegenerativas. Por estarem em contato direto com o lúmen intestinal – isto é, o espaço interior dos intestinos – e se conectarem por sinapse com os neurônios entéricos, as células enteroendócrinas formam um circuito neural entre o trato gastrointestinal e o sistema nervoso entérico, sendo assim um possível ator-chave no surgimento da doença de Parkinson no intestino", disse Fonseca à Agência Fapesp.
Com esses conhecimentos, o grupo de pesquisadores brasileiros buscou entender se os produtos secretados pela bactéria Akkermansia muciniphila poderiam iniciar a agregação da α-sinucleína nas células enteroendócrinas. E se a αSyn agregada nessas células poderia, então, migrar para terminações nervosas periféricas do sistema nervoso entérico.
Eles descobriram que a disbiose intestinal pode levar ao aumento de espécies de bactérias que, eventualmente, contribuem para a agregação da αSyn nos intestinos. E que essa proteína pode então migrar para o sistema nervoso central, configurando um possível mecanismo de surgimento da doença de Parkinson esporádica. Fonte: Folha de Pernambuco. Veja mais aqui: Study reveals how gut imbalance can lead to Parkinson’s disease.
quarta-feira, 16 de março de 2022
Eixo cérebro-intestino-microbiota na doença de Parkinson: uma revisão histórica e perspectiva futura
1 June 2022 - Resumo
A doença de Parkinson (DP) é a segunda doença degenerativa mais comum do sistema nervoso central (SNC) depois da doença de Alzheimer. Além dos sintomas motores típicos, as manifestações clínicas dos pacientes com DP incluem sintomas gastrointestinais, que precedem inclusive os sintomas motores. Pesquisas recentes descobriram que a microbiota intestinal regula a interação axial cérebro-intestino através de mecanismos imunológicos, endócrinos e neurais diretos, apoiando a hipótese de que o processo patológico da DP se espalha do intestino para o cérebro. Neste artigo de revisão, destacamos os achados marcantes no campo da DP, com atenção especial ao eixo cérebro-intestino-microbiota. Resumimos as alterações e seus efeitos clínicos na microbiota intestinal e nos metabólitos observados na DP. A microbiota intestinal pode conter alvos apropriados para a prevenção e tratamento da DP. Estudos clínicos de coorte sugerem que certos micróbios intestinais têm efeitos protetores ou patogênicos na progressão da DP. Uma melhor compreensão da interação entre o eixo intestino-cérebro, a microbiota intestinal e a DP tem o potencial de levar a novas abordagens diagnósticas e terapêuticas. Experimentos em animais sugerem que o transplante de microbiota fecal (FMT - fecal microbiota transplantation) é útil para o tratamento da DP, e espera-se que a FMT seja um tratamento eficaz para a DP no futuro. Original em inglês, tradução Google, revisão Hugo. Fonte: Sciencedirect.
quarta-feira, 23 de fevereiro de 2022
4D Pharma autorizada para iniciar o teste de fase I da doença de Parkinson de ativos bioterapêuticos
A empresa prevê iniciar um estudo de Fase I em pacientes com doença de Parkinson no meio do ano.
February 23,
2022 - A 4D Pharma garantiu a aprovação da Food and Drug
Administration (FDA) dos EUA para iniciar um ensaio clínico de Fase
I para seus dois bioterapêuticos vivos (LBPs - live biotherapeutics)
para tratar a doença de Parkinson.
A empresa antecipa o
início do primeiro ensaio clínico de Fase I em humanos dos LBPs
chamados MRx0005 e MRx0029 em pacientes com doença de Parkinson no
meio do ano.
O estudo randomizado, multicêntrico,
controlado por placebo e duplo-cego analisará a segurança e a
tolerabilidade de MRx0005 ou MRx0029 em diferentes braços de
pacientes com doença de Parkinson.
Além da segurança, o
estudo analisará biomarcadores ligados aos mecanismos de ação dos
LBPs candidatos.
Entregues oralmente, os LBPs são cepas
únicas de bactérias observadas no intestino humano
saudável.
MRx0005 e MRx0029 estão sendo desenvolvidos
para tratar doenças neurodegenerativas, como a doença de Parkinson,
através do eixo intestino-cérebro.
Descobertos usando a
plataforma MicroRx da 4D pharma, eles demonstraram diminuir a
neuroinflamação, incluindo a inflamação causada pela α-sinucleína
e prevenir a morte de neurônios induzida pelo estresse oxidativo em
estudos pré-clínicos.
In vivo, MRx0005 mostrou regular
as moléculas neuroativas e a expressão de seus receptores. Também
poderia oferecer proteção contra a perda de metabólitos de
dopamina no cérebro de camundongos com síndrome parkinsoniana
induzida.
Verificou-se que o MRx0029 induz a diferenciação
do fenótipo neuronal dopaminérgico in vitro e oferece proteção
contra a perda de neurônios dopaminérgicos no modelo animal da
doença de Parkinson.
A 4D pharma formou um Conselho
Consultivo de Pacientes (PAB) composto por pacientes de Parkinson em
parceria com o Parkinson's UK.
O PAB é apoiado pelo
Parkinson's UK e oferece à 4D Pharma uma perspectiva centrada no
paciente, à medida que desenvolve seus novos LBPs em ensaios
clínicos para o tratamento de doenças neurodegenerativas, como o
Parkinson.
O diretor científico da 4D pharma, Dr. Alex
Stevenson, disse: “Acreditamos que MRx0005 e MRx0029 são os
primeiros produtos bioterapêuticos vivos para Parkinson a entrar na
clínica.
“Acreditamos que nossos LBPs MRx0005 e
MRx0029, cada um com diferentes mecanismos de ação dignos de
investigação, oferecem uma oportunidade única de atender às altas
necessidades não atendidas daqueles que vivem com a doença de
Parkinson”.
Em janeiro de 2020, a empresa iniciou um
teste para analisar a eficácia clínica inicial do MRx0518 mais
radioterapia pré-operatória para tratar câncer de pâncreas
ressecável. Original em inglês, tradução Google, revisão Hugo.
Fonte: Clinicaltrialsarena.
terça-feira, 22 de fevereiro de 2022
Alterações do microbioma intestinal em amostras fecais de pacientes com doença de Parkinson virgens de tratamento
2022.02.18 - Resumo
Alterações da microbiota intestinal na doença de Parkinson (DP) foram encontradas em vários estudos e são sugeridas para contribuir para a patogênese da DP. No entanto, os resultados anteriores não puderam ser ajustados adequadamente para um potencial efeito de confusão da medicação para DP e duração da doença, pois quase todos os participantes da DP já estavam usando medicação dopaminérgica e foram incluídos vários anos após o diagnóstico. Aqui, a composição do microbioma intestinal de indivíduos com DP de novo sem tratamento prévio foi avaliada em comparação com controles saudáveis (HC) em duas grandes coortes de caso-controle independentes (n = 136 e 56 DP, n = 85 e 87 HC), usando 16S- sequenciamento de amostras fecais. Variáveis relevantes como lotes técnicos, dieta e constipação foram avaliadas quanto aos seus potenciais efeitos. A composição geral do microbioma intestinal diferiu entre DP e HC em ambas as coortes, sugerindo que as alterações do microbioma intestinal já estão presentes em indivíduos com DP de novo no momento do diagnóstico, sem o possível efeito de confusão da medicação dopaminérgica. Embora nenhum táxon diferencialmente abundante pudesse ser replicado em ambas as coortes, vários táxons produtores de ácidos graxos de cadeia curta (SCFA) diminuíram na DP em ambas as coortes. Em particular, vários táxons pertencentes à família Lachnospiraceae foram diminuídos em abundância. Menos diferenças taxonômicas foram encontradas em comparação com estudos anteriores, indicando tamanhos de efeito menores na DP de novo. Original em inglês, tradução Google, revisão Hugo. Fonte: MedRxiv.